
- •Министерство образования, науки, молодёжи и спорта украины
- •Оглавление
- •3.1 Общий анализ термодинамических процессов в реальном газе 38–39
- •Введение
- •1. Термодинамические процессы в идеальном газе
- •1.2. Политропное расширение, изобарное сжатие и изохорный подвод теплоты
- •1.3. Изохорный подвод теплоты, изобарное расширение и политропное сжатие
- •1.4. Адиабатное сжатие, изохорный подвод теплоты, изобарное и политропное расширение
- •2. Расчет и исследование термодинамических циклов двигателей внутреннег сгорания и газотурбинных установок
- •2.1. Термодинамический цикл двс со смешанным подводом теплоты
- •2.2. Термодинамические циклы газотурбинных установок
- •2.2.1. Простой цикл гту
- •2.2.2. Цикл с регенерацией теплоты
- •2.2.3. Цикл с двухступенчатым сжатием и промежуточным охлаждением воздуха
- •2.2.4. Цикл с двухступенчатым сжатием и промежуточным охлаждением воздуха и регенерацией теплоты
- •3. Расчет термодинамических процессов в реальном газе
- •3.1. Общий анализ термодинамических процессов в реальном газе
- •3.2. Изохорный процесс
- •3.3. Изобарный процесс
- •3.4. Изотермический процесс
- •3.5 Изоэнтропный процесс
- •3.6. Процесс дросселирования
- •3.7. Процесс течения
- •4. Расчет и исследование термодинамических циклов паротурбинных установок
- •4.1. Установка, работающая по циклу Ренкина
- •4.2. Паротурбинная установка с промежуточным перегревом пара
- •4.3. Установки с регенеративным подогревом питательной воды
- •4.3.1. Пту с регенеративным подогревом питательной воды в подогревателе смесительного типа
- •4.3.2. Пту с регенеративным подогревом питательной воды в подогревателе поверхностного типа
- •4.3.3. Пту с промежуточным перегревом пара и регенеративным подогревом питательной воды в поверхностном и смесительном подогревателях
- •4.3.4. Исследование влияния последовательности использования типов регенеративных подогревателей на эффективность пту
- •5. Термодинамика влажного воздуха
- •5.1. Основные понятия, определения и соотношения, характеризующие термодинамические свойства влажного воздуха
- •5.2. Примеры расчета процессов тепломассообмена во влажном воздухе
- •6. Методические указания по выполнению лабораторных работ
- •Изотермического процесса.
- •Контрольные вопросы
- •Контрольные вопросы
- •Образец
Введение
Настоящее учебное пособие содержит примеры решения задач, рассматриваемых на практических занятиях и включаемых в домашние задания по дисциплинам «Техническая термодинамика» и «Термодинамика», изучаемым студентами судомеханического факультета ОНМУ. Оно дополняет учебные пособия [1, 2], в которых также рассматриваются термодинамические процессы и циклы в идеальном и реальном газах. Поскольку в [1, 2] подробно рассмотрена теория этих процессов и циклов, в данном пособии она изложена лишь в минимально необходимом объеме.
Содержание настоящего пособия охватывает все разделы указанных выше дисциплин. В пособии подробно рассматриваются особенности расчета и анализа термодинамических процессов и циклов двигателей внутреннего сгорания, газотурбинных и паротурбинных установок. Приведены примеры решения задач тепломассообмена во влажном воздухе. В заключительной главе пособия приведены методические указания по выполнению лабораторных работ предусмотренных программами двух упомянутых дисциплин.
Знания, приобретенные студентами-судомеханиками при изучении данного пособия, будут способствовать активному их участию в практических занятиях и успешному выполнению домашних заданий. Пособие будет полезно также студентам других специальностей, изучающих основы теплотехники.
Авторы будут признательны за предложения и замечания, направленные на совершенствование и дополнение настоящего пособия.
1. Термодинамические процессы в идеальном газе
Общий анализ термодинамических процессов в идеальном газе
Целью расчета и исследования любого термодинамического процесса является определение термических параметров рабочего тела в начале и конце процесса, а также полученной (затраченной) работы и теплоты, подведенной (отведенной) в исследуемом процессе.
Для этого необходимо знать:
— уравнение состояние рабочего тела (молекулярную массу идеального газа);
— уравнение внутренней энергии (количество атомов в молекуле газа);
— уравнение процесса в одной из систем координат (p,v; p,T или T,v);
— состояние рабочего тела в начале процесса (два независимых параметра, либо величины, из которых их можно определить);
— значение одного из изменяющихся параметров в конце процесса (либо величину, из которой его можно рассчитать).
Выбор тех или иных исходных данных обусловлен характером процесса либо решаемой задачи. Например, могут быть заданы параметры рабочего тела в одном из его состояний и значения теплоты либо работы процесса, а требуется определить параметры в другом состоянии.
Ниже приводятся примеры расчета и анализа термодинамических процессов, используемых в технике. Поскольку чаще всего используется совокупность термодинамических процессов, задачи составлены так, чтобы учащийся с самого начала осваивал методику построения и расчета такой совокупности.
Для облегчения восприятия приводимых ниже расчетов и анализа термодинамических процессов в идеальном газе в табл.1 приведены соотношения
Таблица 1. Аналитические соотношения между термическими параметрами состояния идеального газа в термодинамических процессах
|
Процесс |
Уравнение процесса в координатах p,v |
Соотношения между Параметрами |
|
изохорный |
|
|
|
изобарный |
|
|
|
изотермический |
|
|
|
адиабатный |
|
|
|
политропный |
(может принимать значение от -∞ до +∞) |
|
Таблица 2. Соотношения для расчета теплоты и работы процессов
|
Процесс |
Теплота |
Деформационная работа |
|
изохорный |
|
|
|
изобарный |
|
|
|
изотермический |
|
|
|
адиабатный |
|
|
|
политропный |
|
|
между изменяющимися в них термическими параметрами состояния, а в табл. 2 — формулы для расчета теплоты и работы процессов.
На рис. 1.1. изображена совокупность политропных процессов расширения, исходящих из одной точки. Соотношения между внутренней энергией, теплотой и работой политропных процессов расширения, протекающих в трёх зонах, отмеченных на рисунке, представлены в табл. 3.
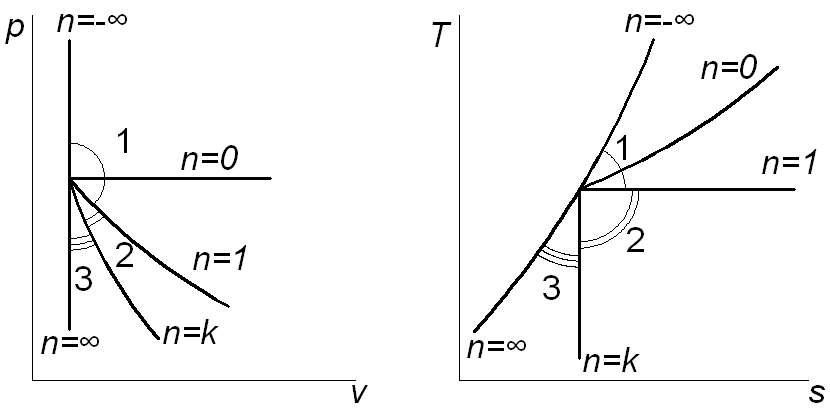
Рис. 1.1. Совокупность политропных процессов расширения в координатах p,v и T,s.
Таблица 3. Соотношения между внутренней энергией, теплотой и работой в политропных процессах расширения
|
№ зоны |
Интервал изменения п |
dT |
du= =сvdT |
δq= =Tds |
с= =δq/dT |
Соотношение между энергетическими эффектами |
|
1 |
|
|
|
|
|
Подводимая q идёт на совер- шение l и на увеличение u |
|
2 |
|
|
|
|
|
Работа l совершается за счёт подвода q и уменьшения u |
|
3 |
|
|
|
|
|
За счёт уменьшения u получается работа l и отводится q |

 с
ростом Т
растет р,
и уменьшается v.
с
ростом Т
растет р,
и уменьшается v. с
ростом Т
растет р,
и уменьшается v.
с
ростом Т
растет р,
и уменьшается v.
