
- •Лекция 8
- •План
- •8.1. Общая характеристика оксосоединений
- •Классификация альдегидов
- •Непредельные альдегиды
- •Ароматические альдегиды
- •Алифатические кетоны
- •Смешанные жирноароматические и ароматические кетоны
- •Реакционные центры в молекулах альдегидов и кетонов
- •Атом углерода карбонильной группы является электрофильным центром и представляет собой удобный центр для
- •Легкость нуклеофильной атаки
- •Схема механизма реакции нуклеофильного присоединения к карбонильным соединениям
- •Реакции АN в ряду альдегидов
- •Гидраты альдегидов и кетонов в свободном виде выделить, как правило, не удается, т.к.
- •Возможно образование стабильного гидрата – нингидрина, который используется для обнаружения аминокислот, пептидов, белков
- •2) Реакция ацетализации
- •Механизм реакции ацетализации
- •Механизм реакции ацетализации на примере образования ацеталей
- •Схема реакции гидролиза ацеталей
- •Механизм реакции гидролиза
- •Если альдегидная и спиртовая группы находятся в одной молекуле, то за счет внутримолекулярной
- •Образование циклического полуацеталя
- •3) Присоединение тиолов
- •4) Реакции присоединения- отщепления
- •1 стадия – нуклеофильное присоединение по карбонильной группе
- •2 стадия – отщепление воды
- •Механизм реакции
- •Аналогично взаимодействуют и производные аминов – гидроксиламин, гидразин, фенилгидразины и т.д. Одной из
- •Схема реакции получения оксима ацетона
- •Схема реакции с фенилгидразином
- •Большое значение в биологическом плане имеет реакция карбонильных соединений (альдегидов и кетонов) с
- •Имины являются промежуточными продуктами в некоторых ферментативных реакциях, при синтезе аминов из альдегидов
- •Схема реакции взаимодействия карбонильных соединений с аммиаком in vivo
- •Взаимодействие аммиака с альдегидами может осложняться возможной циклизацией. Так, из формальдегида А.М. Бутлеров
- •5) Реакция присоединения синильной кислоты (НСN)
- •Механизм реакции
- •6) Реакция альдольной конденсации
- •Механизм реакции альдольной конденсации
- •II стадия
- •Реакция альдольной конденсации часто сопровождается дальнейшим отщеплением молекулы воды с образованием α,β-ненасыщенных карбонильных
- •Кротоновая конденсация
- •Реакция альдольной конденсации возможна только для тех карбонильных соединений, в молекулах
- •В реакцию альдольной конденсации могут вступать также две молекулы различных альдегидов, кетонов
- •Реакция альдольной
- •Механизм реакции альдольной конденсации
- •II стадия
- •Реакция альдольной конденсации, а также обратная ей реакция - альдольное расщепление в клетках
- •Реакция альдольной конденсации
- •Образование лимонной кислоты in vivo
- •COOH
- •Альдольная конденсация протекает в клетках растений в процессе фотосинтеза при взаимодействии фосфорилированного диоксиацетона
- •7) Реакция Канниццаро-Тищенко (ОВР
- •Механизм реакции
- •В реакцию Канниццаро- Тищенко вступают альдегиды, не имеющие водородного атома у α-углеродного атома,
- •Общая формула альдегидов, вступающих в реакцию Канниццаро-Тищенко
- •Спасибо за внимание

Смешанные жирноароматические и ароматические кетоны
CH3 |
|
C |
|
|
|
Метилфенил кетон, |
||
|
|
|
|
|||||
|
||||||||
|
|
|
|
|
|
|
|
ацетофенон |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
||
C Дифенилкетон
O
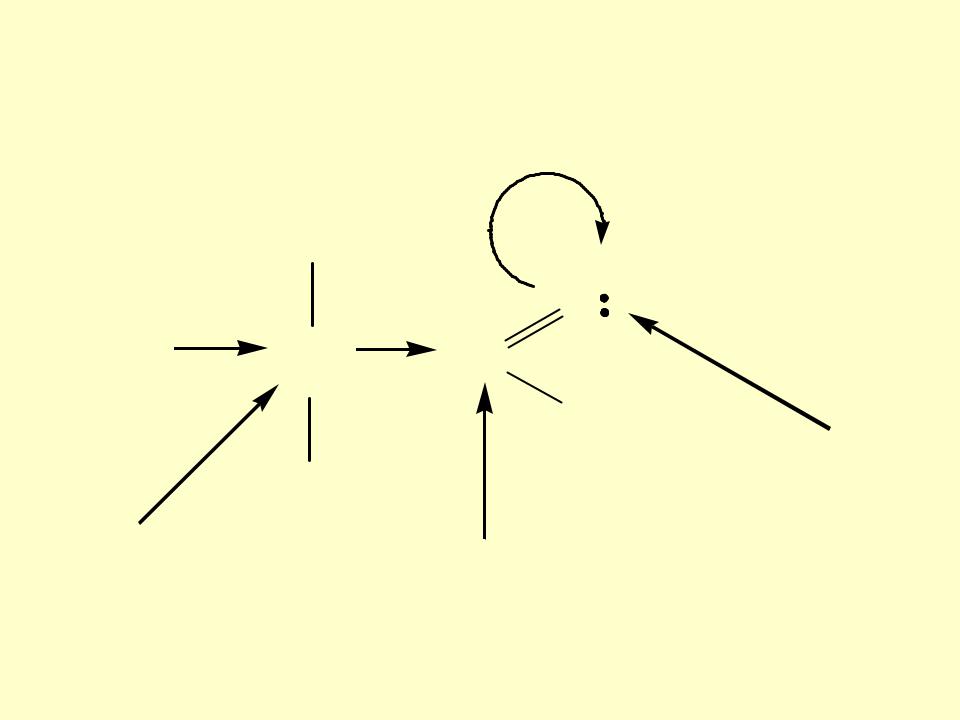
Реакционные центры в молекулах альдегидов и кетонов
|
H |
|
|
.. |
|
|
|
|
|
||
H |
' |
+ |
+ |
O |
|
C |
C |
|
|
||
|
|
|
|
R |
|
|
H |
|
|
|
ОСНОВНЫЙ ЦЕНТР |
|
|
|
|
|
НУКЛЕОФИЛЬНЫЙ |
СН -КИСЛОТНЫЙ |
ЭЛЕКТРОФИЛЬНЫЙ |
||||
|
ЦЕНТР |
ЦЕНТР |
|
|
|

Атом углерода карбонильной группы является электрофильным центром и представляет собой удобный центр для атаки нуклеофилом

Легкость нуклеофильной атаки
зависит:
1)от величины эффективного положительного заряда на карбонильном атоме углерода
2)от пространственной доступности атома углерода в карбонильной группе
3)от кислотно-основных свойств среды

|
+ |
O |
H |
'+ |
O |
R |
''+ |
|
O |
R |
''' |
|
|
O |
||
CCl3 - C |
> |
|
C |
> |
C |
|
> |
C+ |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
H |
|
|
|
H |
|
|
|
|
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
> |
'+ > |
|
'' |
|
''' |
|
|
|
|
|
|
||
|
|
+ > |
+ |
|
|
|
|
|
|
|||||||
Уменьшение эффективности положительного заряда
Уменьшение склонности к реакциям АN

H |
|
O < |
R |
|
|
R |
|
|
|
|
C |
|
C |
|
O < |
C |
|
O |
|
|
|||||||||
|
|||||||||
|
|
||||||||
|
|
||||||||
|
|
|
|||||||
H |
|
|
|
||||||
|
|
H |
|
|
R |
|
|
||
|
|
|
|
|
|
|
|
|
|
Увеличение пространственной затрудненности
Легче вступают в реакции АN альдегиды, а из них – формальдегид.

Схема механизма реакции нуклеофильного присоединения к карбонильным соединениям
|
|
|
R |
|
R |
|
O - + EY |
Y - .... C |
|
R' |
C |
O |
||
|
|
|
|
|
|
|
|
R |
|
Переходное состояние

R |
E+ |
R |
||
|
- O - |
|
|
|
|
|
|
||
Y - C |
|
Y - C - O E |
||
|
||||
R R
Продукт реакции

Реакции АN в ряду альдегидов
икетонов
1)Реакция гидратации
R |
- |
+ HOH |
R |
OH |
C+= O |
R' |
C |
||
R ' |
|
|
OH |
|
гидратыальдегидо
икетонов

Гидраты альдегидов и кетонов в свободном виде выделить, как правило, не удается, т.к. равновесие этой реакции сдвинуто влево. Однако трихлоруксусный альдегид можно прогидратировать

|
Cl |
|
Cl |
OH |
Cl |
|
O |
|
|
C C |
+ HOH |
Cl |
C C H |
|
|
Cl |
H |
Cl |
OH |
|
|
|||
|
хлораль |
|
|
хлораль |
|
трихлоруксусный |
|
гидрат |
|
|
альдегид |
|
|
|
Хлораль гидрат используется в медицине в качестве успокаивающего, снотворного средства
