
- •ОГЛАВЛЕНИЕ
- •Введение
- •Используемые единицы измерений и основные константы
- •1.1. Предпосылки возникновения волновой механики
- •1.1.2. Теория строения атома Бора
- •1.1.3. Корпускулярно-волновой дуализм свойств материи
- •1.1.4. Принцип неопределенности
- •1.2. Волновая (квантовая) механика
- •1.3. Квантово-механическая модель атома
- •1.3.1. Основное состояние атома водорода
- •1.3.2. Радиальное распределение электронной плотности. Электронная орбиталь
- •1.3.4. Многоэлектронные атомы
- •1.3.5. Электронные конфигурации многоэлектронных атомов
- •1.3.6.Связь периодического закона со строением атома
- •1.3.7.Физико-химические характеристики атома
- •2.1. Основные характеристики химической связи. Классификация моделей описания химической связи
- •2.2. Ковалентная химическая связь
- •2.2.1. Метод валентных связей (ВС)
- •2.2.3. Геометрия простейших молекул. Гибридизация АО
- •2.2.4. Донорно-акцепторный механизм образования ковалентной связи
- •2.3. Полярность связи. Дипольный момент молекулы
- •3.1. Агрегатные состояния
- •3.3.1.Основные понятия о строении кристаллов
- •Библиографический список
E, [ |
|
h2 |
] |
|
|
8m a2 |
|
||||
12 |
|
|
|
[2,2,2] – невырожденное состояние |
|
11 |
|
|
|
[3,1,1] [1,3,1] [1,1,3] |
|
9 |
|
|
|
[2,2,1] [2,1,2] [1,2,2] |
трехкратное |
|
|
|
|
|
вырождение |
6 |
|
|
|
[1,1,2] [1,2,1] [2,1,1] |
|
3 |
|
|
|
[1,1,1] - невырожденное состояние |
|
|
|
|
|||
0
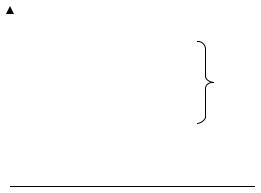
Рис. 1.5. Энергетическая диаграмма электрона в трехмерном потенциальном ящике: [nx, ny, nz] – набор квантовых чисел, соответствующий данному энергетическому состоянию
В кубическом потенциальном ящике почти все энергетические состояния в той или иной степени вырождены. Степень вырождения - это число вариантов наборов квантовых чисел (число волновых функций), при помощи которых можно описать данное энергетическое состояние. Снятие вырождения является важной проблемой квантово-механического описания системы. В случае трехмерного потенциального ящика вырождение снимается частично (a=b≠c) или полностью (a≠b≠c) при изменении параметров ящика. В реальных системах проблема снятия вырождения является более сложной проблемой.
Энергетическое состояние электрона в кулоновском поле ядра достаточно близко соответствует ситуации нахождения электрона в трехмерном потенциальном ящике. Поэтому все закономерности, которые были получены, а главное дискретность энергетических состояний, распространяются и на атом.
1.3. Квантово-механическая модель атома
1.3.1. Основное состояние атома водорода
Атом водорода представляет собой систему, состоящую из положительно заряженного ядра (протон – единичный положительный заряд +e) и одного электрона (единичный отрицательный заряд –e), то есть электрон находится в кулоновском поле положительного заряда (рис. 1.6).
25
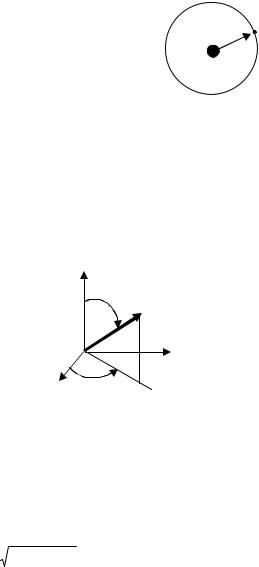
Потенциальная энергия точечного заряда в кулоновском поле определяется выражением
|
|
|
|
|
V = − |
k e2 |
|
|
|
|
|
−e |
||
|
|
|
|
|
|
r |
, |
|
|
|
||||
|
|
|
|
|
|
|
|
+e |
r |
|||||
где e – единичный электрический заряд; r |
|
|
||||||||||||
– расстояние между электроном и ядром; |
|
|
||||||||||||
k = |
|
|
1 |
– константа в законе Кулона. |
|
|
||||||||
|
4πε0 |
Рис. 1.6. Атом водорода |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||
Тогда уравнение Шредингера для ато- |
||||||||||||||
ма водорода принимает вид |
|
|
|
|
||||||||||
|
|
2 |
Ψ(x, y, z) + |
8π2m |
(E |
+ |
k e2 |
) Ψ(x, y, z) = 0 |
|
|
||||
|
|
h2 |
|
r |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Поскольку кулоновское поле сферически симметричное, для упрощения решения целесообразно заменить декартову систему координат полярной, в которой в качестве трех координат используются радиус-вектор r и два угла: θ (тета – угол между радиус-вектором и осью z) и ϕ (фи– угол междупроекциейрадиус-вектора на плоскость xy иосьюx) (рис. 1.7).
z
θ →r
y
ϕ
x
Рис. 1.7. Связь между декартовыми (x,y,z) и сферическими координатами (r,θ,ϕ):
x= r sinϑ cosϕ, y = r sinϑ sinϕ, z = r cosϑ
Вобщем виде волновая функция в полярных координатах является функцией трех переменных: Ψ(r, ϑ, ϕ) . Поскольку единственный электрон
атома водорода находится в сферически симметричном поле ядра, следует ожидать, что решением, описывающим основное (не возбужденное) состояние атома водорода, будет сферически симметричная функция, не зависящая от углов Ψ(r) .
Учитывая, что r = x2 + y2 + z2 , можно произвести замену перемен-
ных в уравнении Шредингера. Для этого проводятся следующие математические преобразования:
26

|
|
|
|
|
|
|
|
|
|
|
|
2Ψ(x,y,z) = |
∂2Ψ |
+ ∂2Ψ |
|
+ |
∂2Ψ |
, |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂x2 |
|
|
∂y2 |
|
|
|
∂z2 |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂2Ψ(r) |
= |
∂ |
( |
∂Ψ(r) |
|
) |
, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂x2 |
|
|
|
|
∂x |
|
∂x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂Ψ(r) |
|
= |
∂Ψ(r) |
|
|
∂r |
|
|
, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂x |
|
|
|
|
|
|
∂x |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂r |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
∂r |
|
= |
∂ x2 + y2 + z2 |
= |
|
1 |
|
|
|
|
|
|
|
|
2x |
|
|
|
|
|
= |
|
x |
, |
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
∂x |
|
|
|
|
∂x |
|
|
|
|
|
|
|
|
2 |
|
x |
2 |
|
+ y |
2 |
|
+z |
2 |
|
r |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
∂Ψ(r) |
= |
|
∂Ψ(r) |
|
∂r |
= |
|
x |
|
|
|
∂Ψ |
, |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
∂x |
|
|
|
|
∂x |
|
r |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂r |
|
|
|
|
|
|
|
|
|
∂r |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
∂2Ψ(r) |
= |
|
|
∂ |
( |
∂Ψ(r) |
) |
|
= |
|
1 |
|
|
∂Ψ(r) |
− |
|
x2 |
|
|
∂Ψ(r) |
+ |
x2 |
|
∂2Ψ(r) |
. |
|
|
|
|||||||||||||||||||||
|
|
|
∂x2 |
|
∂x |
|
∂x |
|
|
|
r |
|
∂r |
|
|
r |
3 |
|
|
∂r |
r2 |
∂r2 |
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
Проведя аналогичные преобразования для координат y и z, просумми- |
|||||||||||||||||||||||||||||||||||||||||||||||||
руем три полученных выражения: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
2 |
Ψ(x,y,z) = |
3 |
|
∂Ψ(r) |
− |
|
x |
2 + y2 + z2 |
|
∂Ψ(r) |
+ |
|
x2 |
+ y2 + z2 |
|
∂2Ψ(r) |
= |
∂2Ψ(r) |
+ |
2 |
|
∂Ψ(r) |
||||||||||||||||||||||||||||
|
r |
∂r |
|
|
|
|
r3 |
|
|
|
|
|
∂r |
|
|
|
|
|
r 2 |
|
|
|
|
|
|
|
∂r 2 |
|
∂r 2 |
r |
∂r |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
Таким образом, уравнение Шредингера в полярных координатах для основного состояния атома водорода [Ψ(r)] приобретает следующий вид:
∂2Ψ(r) |
|
2 |
|
∂Ψ(r) |
|
8π2 |
m |
|
k e2 |
|
|
+ |
|
|
|
+ |
|
|
(E + |
|
) Ψ(r) = 0 . |
∂r2 |
r |
∂r |
h |
2 |
|
|||||
|
|
|
|
r |
||||||
Решить уравнение Шредингера значит найти набор возможных волновых функций электрона и соответствующих им значений энергий.
Это уравнение, как и любое дифференциальное уравнение, имеет бесчисленное множество решений, но физический смысл имеют лишь некоторые из них. В данном случае волновая функция описывает реальную физическую систему – электрон в атоме водорода – и связана с вероятностью его нахождения в определенной области пространства, поэтому она должна:
-быть однозначной – вероятность нахождения электрона в элементарном объеме пространства однозначна;
-непрерывной;
-конечной – ни в одной из точек пространства не равна бесконечности;
-убывать до нуля при увеличении расстояния между электроном и ядром.
Для сферически симметричного кулоновского поля одной из функций, удовлетворяющих перечисленным условиям, является функция вида
27

Ψ(r) = A e−a r ,
где А – нормирующий коэффициент, а – постоянная величина, определяемая в ходе решения.
Для решения поставленной задачи первую и вторую производные предложенной волновой функции подставляют в уравнение Шредингера, определяют параметр а и значение энергии:
∂Ψ(r) |
= −A a |
e−a r , |
|
|
|
|
|
|
|
|
∂Ψ2 (r) = A a2 e−a r , |
|||||||||||||||||||||||||
|
|
∂r |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂r2 |
|
|
|
|
|
|
|
|
|
|
|
A a |
2 |
e |
−a r |
− |
2 |
A |
a e |
−a r |
+ |
|
|
8π2 |
m |
(E + |
|
k e2 |
|
) A e |
−a r |
= 0 . |
||||||||||||||||
|
|
|
r |
|
|
|
|
h2 |
|
|
|
|
r |
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Поскольку Ψ(r) = A e−a r ≠ 0 , то |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
a |
2 |
− |
2 a |
|
+ |
8π2 |
m |
|
E + |
8π2 m |
|
|
|
k e |
2 |
= 0 , |
|
|
|||||||||||||||
|
|
|
|
|
|
r |
|
|
h |
2 |
|
|
|
|
h2 |
|
|
r |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
a |
2 |
|
|
8π2 |
m |
E = |
1 |
|
|
a − |
8π2 |
m k e2 |
|
|
||||||||||||||||||
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
(2 |
|
|
|
|
|
|
|
) . |
|
|
||||||||||
|
|
|
|
|
|
h |
2 |
|
|
r |
|
|
|
|
|
h2 |
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Данное уравнение должно быть справедливым при любых значениях переменной r. А это возможно только в том случае, если левая часть равенства и выражение в скобках в правой части одновременно равны нулю:
a |
2 |
+ |
8π |
2 m |
E = 0 |
, |
||
|
h2 |
|||||||
|
|
|
|
|
|
|
||
2 a − |
8π2 |
m k e2 |
|
|||||
|
|
|
|
= 0 . |
||||
|
|
h2 |
|
|||||
|
|
|
|
|
|
|
|
|
Из второго уравнения определяют постоянную величину а:
a = 4π2 m k e2 . h2
Определив а, из первого уравнения определяют значение энергии электрона:
E = − 2 π2 m k 2 e4 h 2
Вычисление значения энергии основного состояния электрона в атоме водорода дает величину –13,6 эВ, которая хорошо совпадает с экспериментально определенной энергией ионизации. Полученное значение также совпадает с энергией электрона, находящегося на первой орбите (n=1) атома водорода по теории Бора.
28
