- •2.Литературный обзор
- •2.1. Строение, физические, химические и взрывчатые свойства
- •2.1.1. Строение даднэ
- •2.1.2. Физические свойства
- •2.1.3.Спектральные характеристики даднэ
- •2.1.4. Химические свойства даднэ
- •2.1.5. Термическое разложение даднэ
- •2.1.6. Взрывчатые свойства даднэ
- •2.2. Синтез и получение даднэ
- •2.2.1. Синтез даднэ из 2-метилимидазола [2]
- •2.2.2. Синтез даднэ из ацетамидина через 2-метокси-2-метил-4,5-имидазолидиндион (ммид) [20]
- •2.2.3. Синтез даднэ из 2-метил-4,6-пиримидиндиона
- •2.2.4. Полузаводское производство
- •2.2.5. Перекристаллизация даднэ
- •2.3. Применение даднэ
2.1.4. Химические свойства даднэ
1,1-диамино-2,2-динитроэтилен является слабым основанием. Значение рКа для ДАДНЭ составляет 10,6, и при рН 11-13 в водных растворах это соединение преимущественно существует в форме соли.
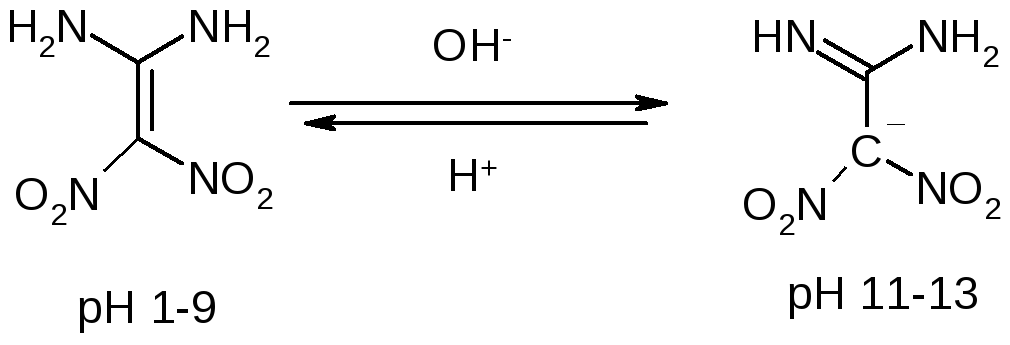
При повышенных температурах в водном растворе КОН протекает разложение и образуется калиевая соль динитрометана с выходом более 75%. В эксперименте, где 3 г ДАДНЭ смешали с раствором 5,9 г КОН в 50 мл воды и нагревали 3 часа при 800С, калиевая соль ДАДНЭ была получена с выходом 87%[5].
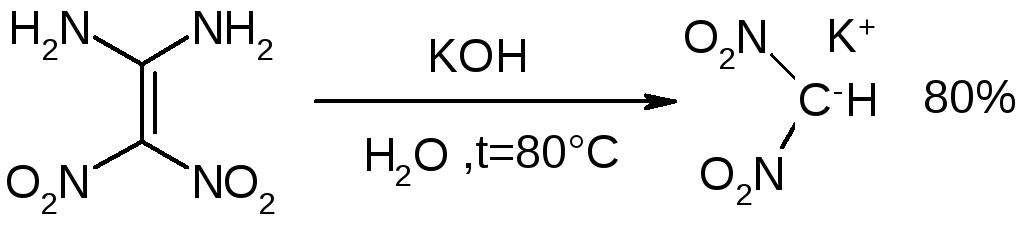
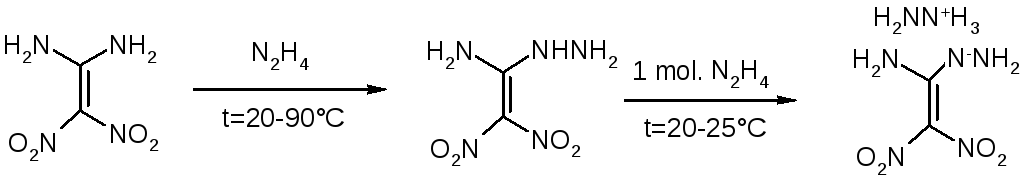
При действии на него раствора гидразина при температуре 20 – 900С происходит замещение одной из аминогрупп и образуется 1-амино-1-гидразо-2,2-динитроэтилен, который при взаимодействии с эквивалентным количеством гидразина при комнатной температуре образует неустойчивую соль; аналогичная реакция протекает и с рядом алифатических аминов [12]. В ряде случаев происходит замещение только одной аминогруппы (3-аминопентан, бензиламин и ряд других); с низшими аминами (1-аминобутан, 2-аминоэтанол и др) образуется смесь продуктов моно- и дитрансаминирования.
При взаимодействии с 1,2-этилендиамином и 1,3-пропилендиамином в среде ДМСО при 100.°С происходит циклизация с образованием пергидропроизводных имидазола и пиримидина с выходами 71 % и 74 %[13].
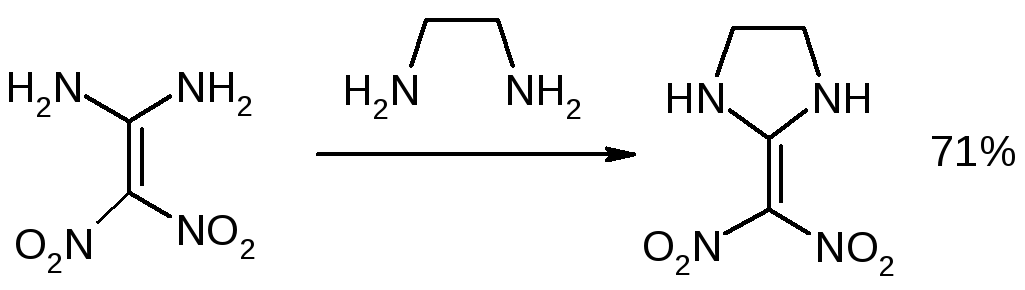
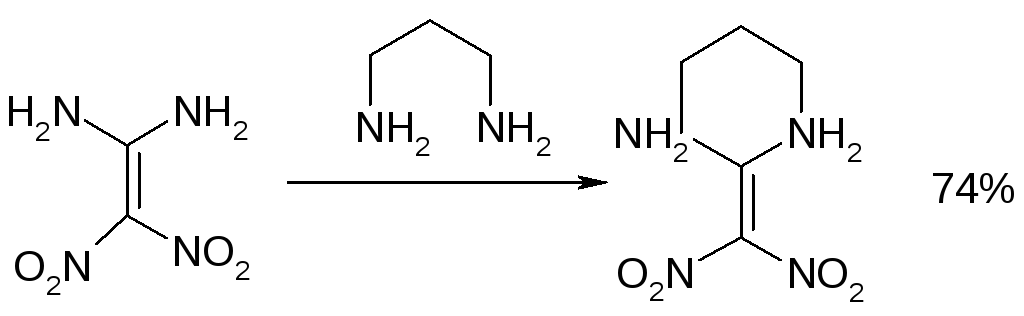
В отсутствие растворителя может происходить замещение не только амино, но и нитрогрупп с образованием 2-имидазолидин-2-илиден-2Н- имидазола [13].

Реакция с гуанидином в метаноле при 20°С приводит к образованию соли , которая при подкислении разрушается [5,13].

При взаимодействии ДАДНЭ c дибромэтаном в сухом ДМФА в присутствии гидрида лития был получен 2-(динитрометилен)-тетрагидро имидазол [2].
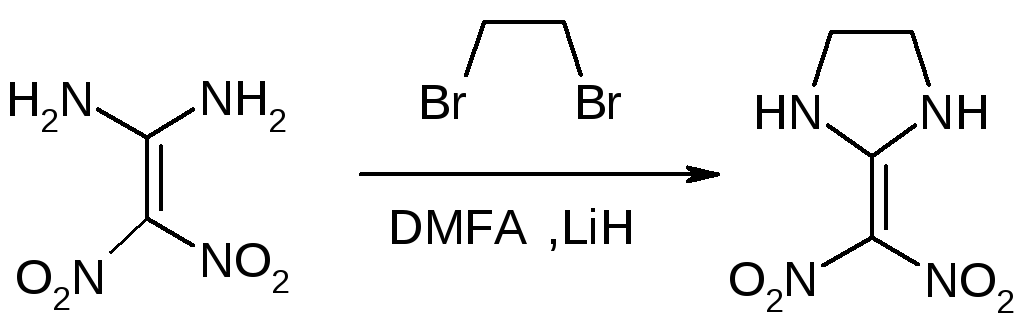
2.1.5. Термическое разложение даднэ
При изучении кинетики термического разложения ДАДНЭ было установлено, что разложение со значительными скоростями начинается только при температуре выше 2000С. В ранних работах были получены завышенные по сравнению с другими нитросоединениями энергии активации [14]. Было показано, что энергия активации, измеренная методом ДСК, равна 234 кДж/моль и обнаружено сильное влияние размера частиц на этот процесс.
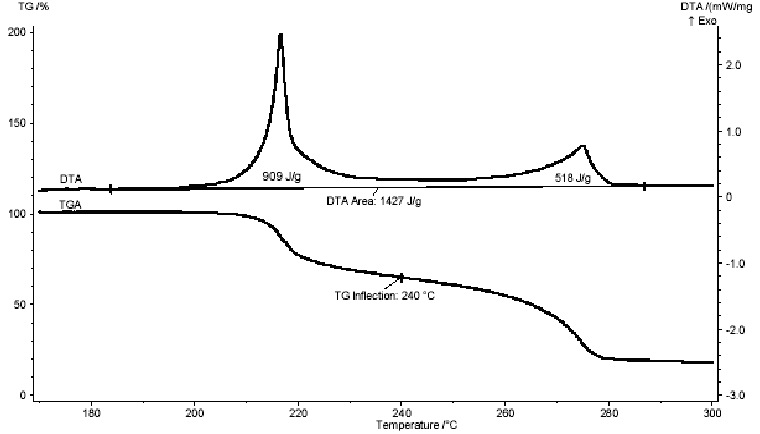
Подробное исследование методами ДТА – TГA проведено в Германии [15], типичные кривые представлены на рис.2.4. При нагревании со скоростью 5 К/мин разложение становится заметным около 210°C и заканчивается взрывом. При скорости нагрева 1 K/min ДАДНЭ наблюдается два экзотермических этапа: на первом, в районе 2200С выделяется больше тепла, но имеется меньшая потеря массы (38 %), чем на втором, в районе 2700С (45%-ая потеря массы). Наличие 2-х пиков отмечается и в ряде других работ, причем положение первого пика в районе 205-2300С определялось скоростью нагревания, степенью очистки продукта и рядом других факторов.
Рис.2.4. Кривые ТГА и ДТА в области разложения ДАДНЭ
Для определения кинетических характеристик процесса были проведены изотермические опыты при температурах 185 –2000С. Механизм разложения предложено описывать как сумму двух параллельных процессов А --- B и C----D, где А и С –различные формы ДАДНЭ. Для описания этих реакций предложены уравнения:
для 1-ой - dα/dt = k (1-α)n * ( 1-α *a),
для 2-ой - dα/dt = k (1-α)n.
В этих уравнениях α –степень превращения, измеряемая как потеря массы (или выделение тепла) в данный момент, отнесенная к общей потере массы (или выделению тепла) на стадии. Основные параметры представлены в табл. 2.6.
Таблица 2.6
Основные кинетические параметры двухстадийного разложения FOX 7
|
Параметр |
1-ая стадия |
2-ая стадия |
|
Предэкспонент |
1,015* 1023 |
2,305* 1026 |
|
Энергия активации, кДж/моль |
250,1 |
304,5 |
|
Порядок реакции |
2.853 |
0,462 |
|
Степень превращения на стадии, % |
41,2 |
42,1 |
|
Тепловыделение, Дж/г |
909 |
518 |
В [16] приводится энергия активации равная 243 кДж/мол.
При стандартной пробе на стабильность после 48 часов при 1000С объем выделившихся газов менее 0,1 мл/г.
Температура вспышки 215 – 2230С.
Исследования, проведенные в РХТУ им. Д.И.Менделеева, по изучению горения и термического разложения ДАДНЭ в изотермических условиях [17] привели авторов к заключению, что в этих процессах большую роль может играть превращение основной формы соединения в аци-форму с последующим разложением последней (с отщеплением азотной кислоты). Параллельное протекание процессов изомеризации и разложения может являться одной из причин завышенного значения энергии активации при распаде ДАДНЭ.
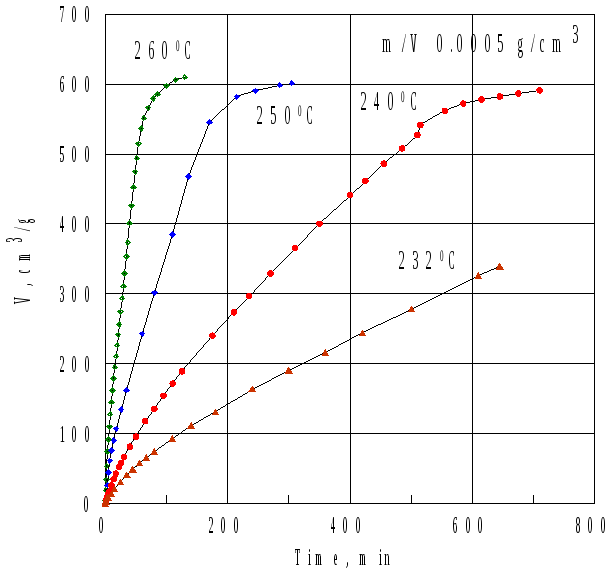
В ходе этих исследований была обнаружена еще одна особенность термического разложения ДАДНЭ. Как видно из рис. 2.5, кривые накопления газообразных продуктов имеют насыщающийся характер, т.е. чем ниже температура, тем меньшая степень разложения достигается в процессе. При этом было установлено, что твердый остаток после опытов по данным физико-химических методов анализа идентичен исходному ДАДНЭ.
|
|
Рис.2.5 Влияние температуры на объем выделившихся газов при разложении ДАДНЭ |
Для выдержанных образцов изменяется и характер газовыделения, что подтверждается рис.2.6. Энергия активации близка к указанной выше 232-241 кДж/моль.
|
|
Рис.2.6. Влияние температуры на разложение термически обработанного ДАДНЭt |
При повторном нагревании образцов, выдержанных при температуре 210 – 2200С, на кривых ДСК первый экзотермический пик исчезает, и разложение начинается вблизи 2700С.
Следует отметить, что если термостатированный продукт перекристаллизовать из ацетонитрила, он снова ведет себя как нетермостатированный продукт.
Для объяснения этого феномена (исходный, перекристаллизованный и термостатированный ДАДНЭ имеют одинаковые рентгеновские-, ИК- и ЯМР-спектры) авторы работы [15] допускают, что технический продукт содержит аморфную и кристаллическую формы, и при низкой температуре (210-2300С) происходит разложение аморфной формы.
Аналогичные результаты получены и в [15]. Степень разложения после термостатирования при 210-2150С в течение часа составила около 35%. Полученный продукт на ДСК разлагается выше 2700С. Авторы предполагают, что при термостатировании образуется продукт преобразования двух молекул ДАДНЭ, так как при нагревании образца от 20 до 4000 С эндотермические пики не зафиксированы.
В 2004 г в Швеции было проведено подробное исследование влияния качества перекристаллизованного технического ДАДНЭ на его термические свойства [18]. Перекристаллизацию проводили из ацетонитрила, -бутиролактона (БЛ), водных смесей N-метилпирролидона (50: 50 по объему) и диметилформамида (75:25 по объему), максимальная температура в во всех системах , кроме ацетонитрила, 950С, в последнем 700С, скорость охлаждения 0,2 – 0,020С в минуту. Кроме того, кристаллы , полученные из бутиролактама были перенесены в насыщенный раствор и оставлены на длительное время, что позволило получить крупные кристаллы. Кристаллы из ацетонитрилa, N-метилпирролидона и мелкие кристаллы из БЛ имели двумерную ромбическую форму , крупные кристаллы трехмерную ромбическую форму, а из ДМФА –форму параллелепипеда. Крупные кристаллы из БЛ и из ДМФА имели более гладкую поверхность.
Сведения о среднем размере полученных кристаллов представлены в таблице 2.7.
Таблица 2.7.
|
Растворитель |
Размер частиц, мкм |
|
N-метилпирролидон/вода |
250 –400 |
|
-бутиролактон (после дополнительной обработки) |
<500 |
|
-бутиролактон |
50 –185 |
|
Диметилформамид/вода |
50 – 110 |
|
Ацетонитрил |
<50 |
Природа растворителя оказывает заметное влияние на поведение ДАДНЭ при термическом воздействии. При изучении распада методом ДСК для всех очищенных продуктов наблюдается эндотермичный пик в области 115-1200С, который идентифицируется как первый модификационный переход, и вблизи 1600С (кроме продукта из ацетонитрила) второй модификационный переход. В области выше 2200С наблюдается два экзотермических пика, в ходе которых в газообразные продукты превращается более 80% исходного материала.
В циклических опытах с интервалом температур 3-1950С температура эндотермического пика при нагревании сохраняет свое значение, но температура экзотермического пика при охлаждении на 15-200 ниже. Эндотермический пик при 1600 при нагревании сохраняется, но соответствующий ему экзотермический пик при охлаждении не наблюдается.