
- •Лекция № 15
- ••Аминокислоты —
- •Кислотно-основные свойства аминокислот
- •СООН СООН
- •Зеркало Венеры (1898), Edward Burne-Jones
- •Классификации аминокислот, исходя из количества карбокси- и аминогрупп (примеры)
- •Классификация аминокислот по степени полярности боковых цепей
- •Неполярные ароматические, гидрокси- и серосодержащие аминокислоты
- •Неполярные амино- и иминокислоты
- •полярные заряженные аминокислоты:
- •Основные аминокислоты, имеющие дополнительные амино- группы, которые несут с собой в растворах положительный
- •Нейтральные аминокислоты – представляют собой амидные производные аспарагиновой и глутаминовой кислот (Asn, Gln)
- •Образование дипептидов
- •СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ
- •ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ
- •Классификация пептидов
- •Дипептиды, полипептиды
- •СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ
- •СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ
- •СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ
- •Эпиталон – гормон шишковидной железы
- •Гормоны гипофиза
- •СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ
- •СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ
- •• Белки-рецепторы (опиоидные)
- •Пептиды, определяющие пищевое поведение человека
- •• Лептины
- ••Ангиотензин I декапептид - синтезируется в печени. В мембране кровеносных сосудов, особенно в
- •СТРОЕНИЕ НЕКОТОРЫХ ПЕПТИДОВ
- •Токсические пептиды
- •Токсические пептиды
- •Сывороточный фактор тимуса - нанопептид
- •Грамицидин S - антибиотик, оказывающим бактериостатическое и бактерицидное действие на стрептококки, стафилококки, пневмококки,
- •Грамицидин А обладает свойством образовывать ионселективный трансмембранный канал, не уступающий по характеристикам белковым
- •Валиномицин представляет собой полипептид, повышающий проницаемость мембраны для ионов калия. Во внутренней полярной
- •Актиномицин D (Дактиномицин) – один из группы противоопухолевых антибиотиков. Подавляет точки роста, вызывает
- •Антимикробные пептиды – возможная альтернатива традиционным антибиотикикам
- •Белки- наиболее распространенные биополимеры
- •Протеомика
- •Функции белков
- •Структурообразующие функции. Структурные белки
- •Система белков цитоскелета эритроцита
- •Первичная структура белка - это последователь-ность расположения амино- кислотных остатков в полипептидной цепи,
- •Вторичная структура белка - это упорядоченное строение полипептидных цепей, обусловленное образованием водородных связей
- •ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ
- •ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ
- •Третичная структура белка - расположение элементов вторичной структуры (альфа- спиралей) в пространстве относительно
- •Что же заставляет белки сворачиваться?
- •Третичная структура полностью задается первичной структурой белка
- •ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ
- •ИОННЫЕ ВЗАИМОДЕЙСТВИЯ ПРИ ОБРАЗОВАНИИ ТРЕТИЧНОЙ СТРУКТУРЫ ПОЛИПЕПТИДОВ И БЕЛКОВ
- •Механизм образования
- •• Структура инсулина (дисульфидные мостики между цепями)
- •Образование водородных связей между карбонильной и амидной группами
- •Белок при попадании в водный раствор принимает ту конформацию, в которой он должен
- •ПРИОННЫЕ БЕЛКИ
- •У людей есть аналог болезни коровьего бешенства. Это заболевание куру.
- •Серповидно-клеточная анемия как
- •РНК-полимераза
- •ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ
- •Первичная структура белка аполипопротеина Е, он занимается транспортом холестерина.
- •Известна мутация в этом белке, которая меняет заряд одной аминокислоты. В результате меняются
- ••Функция аполипопротеида заключается в переносе липидов и холестерина.
- •Структуры белка
- •Кристаллы различных белков, выращенные на космической станции «Мир» и во время полётов шаттлов
- •Расшифровка белка- крайне трудоемкий процесс. На расшифровку гемоглобина потребовалось 26 лет.

ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ
(Вторичная структура – β-складчатые структуры)

Третичная структура белка - расположение элементов вторичной структуры (альфа- спиралей) в пространстве относительно друг друга (пространственная конформация полипептида) (формирование глобулы)

Что же заставляет белки сворачиваться?
•Гидрофобные взаимодействия. Существуют полярные и неполярные аминокислоты. В водном окружении гидрофобные (неполярные) аминокислоты прячутся внутрь спирали, образуя структуру с минимальной потенциальной энергией.
•Ионные взаимодействия. Заряженные разноименные остатки аминокислотные остатки притягиваются друг к другу, а разноименные – отталкиваюися. Наличие гидрофобных или заряженных участков в полипептидной цепи, определяет то, как белок свернется.
•Ковалентные связи между остатками двух цистеинов (дисульфидные мостики), образующиеся а счет окисления аминокислоты цистеина.
•Водородные связи. Участвуют все аминокислоты, имеющие гидроксильные, амидные или карбоксильные группы.

Третичная структура полностью задается первичной структурой белка
Определяющими являются гидрофобные взаимодействия аминокислот в силу их многочисленности. Гидрофобное ядро существует у большинства белков.
На поверхности третичной структуры белка находятся, как правило –SH – группы цистеина.
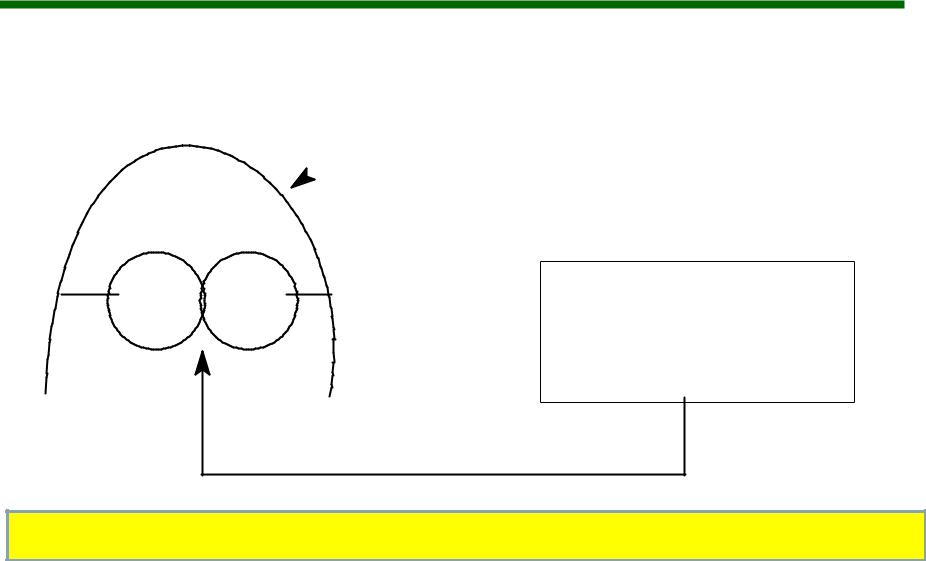
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ ПОЛИПЕПТИДОВ И БЕЛКОВ
(Третичная структура)
Полипептидная  цепь
цепь
CH3 CH3 |
Гидрофобное |
|
взаимодействие |
Ala Ala |
|
НЕПОЛЯРНЫЕ ФРАГМЕНТЫ МОЛЕКУЛЫ ПРЯЧУТСЯ ВНУТРЬ ГЛОБУЛЫ

ИОННЫЕ ВЗАИМОДЕЙСТВИЯ ПРИ ОБРАЗОВАНИИ ТРЕТИЧНОЙ СТРУКТУРЫ ПОЛИПЕПТИДОВ И БЕЛКОВ
(Третичная структура)
CH |
COO- |
+NH |
C NH (CH ) |
2 |
2 |
2 3 |
|
|
|
|
NH2 |
Asp |
|
Arg |
|
Ионная связь

Механизм образования
дисульфидных мостиков при окислении остатков цистеина

• Структура инсулина (дисульфидные мостики между цепями)

Образование водородных связей между карбонильной и амидной группами

