
Тесты в ЭМИРСе / ВСЕ ТЕСТЫ ПО ХИМИИ
.docxВопрос: Сколько миллилитров воды необходимо прибавить к 200 мл 2М раствора азотной кислоты, чтобы получить 1н раствор? 1. 200 мл 2. 100 мл 3. 400 мл 4. 50 мл 5. 150 мл Ответ: 3 Неправильно!
Вопрос: Вычислить молярность 20% раствора хлорида цинка, плотность которого 1,136 г/мл. 1. 0,174М 2. 3,48М 3. 1,74М 4. 0,348М 5. 0,522М Ответ: 3 Правильно!
Вопрос: На нейтрализацию 40 мл 2М раствора серной кислоты израсходовано 20 мл раствора гидроксида натрия. Определить нормальность раствора NaOH. 1. 4 н 2. 2 н 3. 8 н 4. 1 н 5. 5 н Ответ: 3 Правильно!
тест "Строение атома, химическая связь"
Вопрос: Укажите, какие значения принимает спиновое квантовое число, если главное квантовое число равно 5, а орбитальное 3: 1. 0,1,2,3,4 2. 0,1,2,3 3. -3,-2,-1,0,+1,+2,+3 4. +1/2,-1/2 5. -3,0,+3 Ответ: 4 Правильно!
Вопрос: Укажите расположение подуровней 3d 4f 5s 6p в порядке возрастания их емкости: 1. 3d 4f 5s 6p 2. 3d 5s 4f 6p 3. 3d 6p 5s 4f 4. 5s 6p 3d 4f 5. 4f 3d 6p 5s Ответ: 2 Неправильно!
Вопрос: Укажите, какому принципу подчиняется последовательность заполнения уровней и подуровней: 1. принципу Паули 2. принципу Гейзенберга 3. правилу Хунда 4. правилам Клечковского 5. уравнению де-Бройля Ответ: 4 Правильно!
Вопрос: Укажите электронную формулу, соответствующую атому в стационарном состоянии: 1. …3s23p43d1 2. …4s13d104p2 3. …4p65s24d2 4. …4p65s14d105p2 5. …2s12p1 Ответ: 3 Правильно!
Вопрос: Укажите положение ( № группы, подгруппу и № периода) в таблице Д.И.Менделеева элемента, у которого на 4р-подуровне есть 2 неспаренных электрона: 1. Ш период IVА группа 2. IV период VIA группа 3. V период IVА группа 4. III период IVВ группа 5. V период IVВ группа Ответ: 2 Правильно!
Вопрос: Валентными электронами у р-элементов являются: 1. р-электроны внешнего энергетического уровня 2. s- электроны внешнего уровня 3. s- и р-электроны внешнего энергетического уровня 4. s- электроны внешнего и d-электроны предвнешнего уровня Ответ: 3 Правильно!
Вопрос: В молекуле______ образуются σ - связи путем перекрывания s - и p орбиталей 1. BCl3 2. H2Se 3. Cl2 4. Na2S Ответ: 3 Неправильно!
Вопрос: Расположите связи в порядке возрастания их энергии: а) K-Br, б) K-F, в) K-Cl, г) K-I 1. а, б, в, г 2. б, в, а, г 3. г, б, а, в 4. г, а, в, б Ответ: 3 Неправильно!
Вопрос: Дипольный момент молекулы ______ равен нулю 1. H2O 2. PCl5 3. AsCl3 4. PCl3 Ответ: 2 Правильно!
Вопрос: В молекуле __________угол между связями равен 180°: 1. SiCl2 2. BeCl2 3. GeCl2 4. SiH4 Ответ: 2 Правильно!
Вопрос: sp2- гибридизация в молекуле 1. CS2 2. C2H2 3. C2H4 4. CO2 Ответ: 3 Правильно!
Вопрос: Наибольшей степенью ковалентности обладает связь ______ 1. Na-Br 2. Na-Cl 3. Na-I 4. Na-F Ответ: 3 Правильно!
Вопрос: Молекулярную кристаллическую решетку образует 1. алмаз 2. никель 3. хлор 4. фторид калия KF Ответ: 1 Неправильно!
тест "Классификация неорганических соединений для МП,ЭКТ, ЭТМО"
Вопрос: Укажите формулы амфотерных оксидов 1. ZnO 2. Na2O 3. Al2O3 4. CO2 5. N2O Ответ: 1,3 Правильно!
Вопрос: Укажите формулу несолеобразующего оксида 1. H2O 2. Na2O2 3. PbO2 4. Cl2O7 5. SiO Ответ: 5 Правильно!
Вопрос: Укажите оксид, реагирующий с Na2O. 1. MgO 2. BaO 3. CO 4. CO2 5. SiO Ответ: 4 Правильно!
Вопрос: Укажите формулу ортоборной кислоты. 1. HBO2 2. H3BO3 3. H4B2O7 4. HBO3 5. H2BO4 Ответ: 2 Правильно!
Вопрос: Укажите название солей ортомышьяковой кислоты. 1. арсениды 2. ортоарсениты 3. метаарсенаты 4. арсениты 5. арсенаты Ответ: 5 Правильно!
Вопрос: Укажите схему суммарной диссоциации сернистой кислоты. 1. H2SO4 ⇄ 2H+ + SO42- 2. H2SO4 ⇄ H+ + HSO4- 3. H2SO3 ⇄ 2H+ + SO32- 4. H2S ⇄ H+ + HS- 5. H2S ⇄ 2H+ + S2- Ответ: 3 Правильно!
Вопрос: Укажите вещество, при добавлении которого усиливается диссоциация ортоборной кислоты. 1. Na2SO4 2. H2SO4 3. KOH 4. KNO3 5. HNO3 Ответ: 3 Правильно!
Вопрос: Укажите группу формул, соответствующих следующим солям: метафосфат кальция; сульфид никеля (II); сульфит хрома (III) 1. K3PO4; NiSO3; Cr2S3 2. NiSO4; Cr2(SO3)3; KPO3 3. Ca(PO3)2; NiS; Cr2(SO3)3 4. Ca(PO2)2; NiSO3; Cr2(SO4)3 5. KPO2; Ni(HS)2; Cr(NO3)3 Ответ: 3 Правильно!
Вопрос:
Укажите
формулу сернистой
кислоты
1.  2.
2.  3.
3. 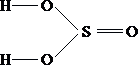 4.
4. 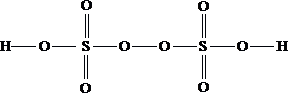 5.
5.  Ответ: 3
Правильно!
Ответ: 3
Правильно!
Вопрос: Укажите формулу смешанной соли 1. K2SO4 2. KAl(SO4)2 3. CaClNO3 4. CaOHNO3 5. Ca(HS)2 Ответ: 3 Правильно!
Вопрос: Укажите формулу кислой соли 1. NaHSO3 2. KAl(SO4)2 3. Cr(OH)2NO3 4. [Zn(NH3)4]SO4 5. Na2SO4 Ответ: 1 Правильно!
Вопрос: Укажите формулу основной соли 1. [Ag(NH3)2]Cl 2. [Al(OH)2]2SO4 3. Na2CrO4 4. Mg(HSe)2 5. KAl(SO4)2 Ответ: 2 Правильно!
Вопрос:
Укажите
реакцию, в результате которой можно
получить основную соль.
1. ![]() 2.
2. ![]() 3.
3. ![]() 4.
H3PO4 + KOH →
5.
4.
H3PO4 + KOH →
5. ![]() Ответ: 3
Правильно!
Ответ: 3
Правильно!
Вопрос:
Укажите
реакцию, в результате которой можно
получить кислую
соль
1. ![]() 2.
2. ![]() 3.
3. ![]() 4.
4. ![]() Ответ: 1,4
Правильно!
Ответ: 1,4
Правильно!
Вопрос: Укажите формулу гидросульфида меди (II) 1. (CuOH)2SO4 2. Cu(HSO4)2 3. Cr2S3 4. Cu(HS)2 5. KCr(SO4)2 Ответ: 4 Правильно!
Вопрос: Для последовательного осуществления превращений по схеме AlСl3 → Al(OH)3 → Na3AlO3 → Al(OH)2 Cl → AlCl3 необходимы вещества____ 1. NH4F; H2О; NaF; НCl 2. NaOH; H2О; HCl(избыт);Al2O3 3. NaClO4; NH4Сl; H2О; HCl(нед.) 4. NaOH; NaOH(избыт.); HCl(недост.); HCl(избыт) Ответ: 4 Правильно!
Вопрос: С помощью какого реагента можно отличить в растворах NaCl и Na3PO4 1. HNO3 2. K2SO4 3. AgNO3 4. NaOH 5. H2SO4 Ответ: 3 Правильно!
тест "Окислительно-восстановительные реакции"
Вопрос: Степень окисления окислителя в ОВР 1. повышается 2. понижается 3. не изменяется Ответ: 2 Правильно!
Вопрос: С увеличением электроотрицательности восстановительные свойства __________ 1. ослабевают 2. усиливаются 3. не изменяются Ответ: 1 Правильно!
Вопрос: Из приведенных примеров наиболее сильным восстановителем является 1. Hg 2. Ca 3. Ge 4. Pb 5. S Ответ: 1 Неправильно!
Вопрос: Молекулы NH3 в ОВР могут быть ________ 1. и окислителями и восстановителями 2. только восстановителями 3. только окислителями Ответ: 2 Правильно!
Вопрос: Превращение _________ соответствует процессу восстановления 1. MnO2 → MnO42- 2. I- → I2 3. Pb2+ → PbO32- 4. S2- → S 5. MnO4- → Mn2+ Ответ: 5 Правильно!
Вопрос: В реакции KMnO4 + MnSO4 + H2O → MnO2 восстановителем является ________ 1. KMnO4 2. MnSO4 3. H2O 4. MnO2 Ответ: 2 Правильно!
Вопрос: Окислительно-восстановительная реакция PCl5 → PCl3 + Cl2 относится к типу _______ 1. внутримолекулярного ОВ 2. диспропорционирования 3. межмолекулярного ОВР Ответ: 1 Правильно!
Вопрос: В реакции Si + KOH + H2O → H20 + SiO32- участвует ______ электронов 1. 6 2. 3 3. 8 4. 4 5. 2 Ответ: 4 Правильно!
тест "Электролитическая диссоциация и физические свойства растворов"
Вопрос: Константа диссоциации слабого однокислотного основания равна Kдисс = 1•10–6. Определить рH 0,01н раствора 1. 4 2. 2 3. 6 4. 10 5. 14 Ответ: 2 Неправильно!
Вопрос: Определить эффективную концентрацию ионов Сl– в 0,25н растворе СаСl2, если кажущаяся степень диссоциации СаСl2 равна 72% 1. 0,36 моль-ион/л 2. 0,72 моль-ион/л 3. 0,18 моль-ион/л 4. 1,8 моль-ион/л 5. 3,6 моль-ион/л Ответ: 3 Правильно!
Вопрос: Степень диссоциации циановодородной кислоты HCN в 0,1н растворе при 18ºС равна 0,007%. Определить Кдисс кислоты при данной температуре. 1. 4,9·10–10 2. 4,9·10–6 3. 7·10–4 4. 7·10–5 Ответ: 1 Правильно!
Вопрос: Определить молярную концентрацию раствора HCN, pOH которого составляет 12, а степень диссоциации 2,5%. 1. 0,4 моль/л 2. 4·10–7 моль/л 3. 4 моль/л 4. 1,6 моль/л 5. 1,6·10–2 моль/л Ответ: 1 Правильно!
Вопрос: Вычислить концентрацию ионов [S2–] в моль/л в насыщенном растворе FeS если ПРFeS = 3,7·10–19. 1. 6·10–10 моль/л 2. 5,3·10–8 моль/л 3. 3,4 ·10–8 мольг/л 4. 1,9 ·10–8 моль/л Ответ: 1 Правильно!
Вопрос: Имеются 2 моляльные растворы CH3COOH, H2SO4, HCl, C6H12O6. Расположите их в порядке возрастания температуры кипения. 1. CH3COOH,C6H12O6, HCl,H2SO4 2. C6H12O6, CH3COOH, HCl, H2SO4 3. H2SO4, HCl,C6H12O6, CH3COOH 4. H2SO4, HCl, CH3COOH, C6H12O6 5. HCl, H2SO4, CH3COOH,C6H12O6 Ответ: 2 Правильно!
Вопрос: Определить температуру кипения раствора, содержащего 29 г йодида аммония NH4I (μ = 145) в 250 г ацетона, если известно что Ткипения чистого ацетона = 56 °С, а эбуллиоскопическая константа Кэб = 1,5. 1. 56,12°С 2. 57,2°С 3. 57,74°С 4. 54,8°С 5. 55,88°С Ответ: 1 Неправильно!
Вопрос: Раствор, содержащий 3,04 г камфоры C10H16O в 100 г бензола, кипит при 80,714°С, температура кипения бензола 80,2°С. Вычислить эбуллиоскопическую константу бензола. 1. 5,14 2. 1,28 3. 3,4 4. 2,57 5. 0,26 Ответ: 4 Правильно!
Вопрос: Кажущаяся степень диссоциации ZnSО4 в 0,1 н растворе равна 40%. Определить осмотическое давление этого раствора при 0°С. 1. 204,7 кПа 2. 406,3 кПа 3. 158,8 кПа 4. 318,2 кПа 5. 638,3 кПа Ответ: 4 Неправильно!
Вопрос: Определить давление пара раствора, содержащего 2,5 г гидроксида натрия в 90 г воды при 100°С, если кажущаяся степень диссоциации NaОН в этом растворе равна 80%? 1. 101,3 кПа 2. 757,5 кПа 3. 762,5 кПа 4. 98,8 кПа 5. 103,8 кПа Ответ: 4 Правильно!
тест "Электрохимия"
Вопрос: Система, состоящая двух электродов первого рода, соединенных во внешней и внутренней цепях, называется _________ 1. аккумулятором 2. двойным электрическим слоем 3. гальваническим элементом 4. электролизером Ответ: 3 Правильно!
Вопрос: Электродный потенциал магния, опущенного в 0,1М раствор его соли, равен ______ В 1. −2,33 2. +2,39 3. +2,66 4. −2,39 Ответ: 4 Правильно!
Вопрос: При замене 0,1М раствора на 1М в гальваническом элементе Ag/AgNO3(0,01M)//AgNO3(0,1M)/Ag величина ЭДС_________ 1. не изменится 2. увеличится в 10 раз 3. уменьшится в 2 раза 4. увеличится в 2 раза Ответ: 3 Неправильно!
Вопрос: В гальваническом элементе _____ медь является анодом: 1. Cu /CuSO4 //SnCl2/Sn 2. Cu /CuSO4 //Pb(NO3)2/Pb 3. Ni/NiSO4//CuSO4/Cu 4. Cu /CuSO4 //AgNO3/Ag Ответ: 4 Правильно!
Вопрос: Реакция MnO4− + Fe2+ ↔ MnO2 +Fe3+ в нейтральном водном растворе___ 1. протекает в прямом направлении 2. протекает в обратном направлении 3. находится в состоянии равновесия 4. невозможна ни при каких условиях Ответ: 2 Правильно!
Вопрос: Катодным по отношению к покрываемому металлу является покрытие 1. цинк покрыт медью 2. железо – хромом 3. железо – никелем 4. медь – цинком Ответ: 1,3 Правильно!
Вопрос: Уравнения процессов электрохимической коррозии железа в контакте с оловом в кислой среде ______ 1. Fe – 3ē → Fe3+ 2H+ + 2ē → H2↑ 2. H2 – 2ē → 2H+ Sn2+ + 2ē → Sn 3. Fe – 2ē → Fe2+ 2H+ + 2ē → H2↑ 4. Fe – 2ē → Fe2+ Sn2+ + 2ē → Sn Ответ: 3 Правильно!
Вопрос: При электролизе раствора смеси солей последним выделится на катоде _________ 1. K 2. Cr 3. Hg 4. Pb Ответ: 2 Правильно!
Вопрос: При электролизе водного раствора KBr на медном аноде протекает процесс _______ 1. 2Br− → Br2 + 2ē 2. 2H2O → O2 + 4H+ + 4ē 3. Cu → Cu2+ + 2ē 4. 4OH− → O2 + 2H2O + 4ē Ответ: 1 Неправильно!
Вопрос: Объем кислорода (н.у.), выделившегося при пропускании через водный раствор H2SO4 тока силой 3А в течение 40 мин составил ____л. 1. 0,836 2. 0,03 3. 0,418 4. 1,67 Ответ: 3 Правильно!
тест "Комплексные соединения "
Вопрос: Осадок не образуется при добавлении раствора AgNO3 к раствору 1. [Cr(H2O)6]Cl3 2. [Cr(H2O)5Cl]Cl2 3. [Cr(H2O)4Cl2]Cl 4. [Cr(H2O)3Cl3] Ответ: 1 Неправильно!
Вопрос: Величина и знак заряда комплексного иона [Cr+3(NH3)3(CN)2SO4]х равны 1. 1+ 2. 3+ 3. 1- 4. 3- Ответ: 3 Правильно!
Вопрос: Соединение [Cu(NH3)4](OH)2 относится к классу 1. кислот 2. солей 3. оснований 4. аммиакатов Ответ: 4,3 Правильно!
Вопрос: Из соединений [Cu(NH3)4]SO4 или CuSO4 большая степень гидролиза характерна для 1. [Cu(NH3)4]SO4 2. CuSO4 3. одинакова 4. обе соли не гидролизуются Ответ: 2 Правильно!
Вопрос: Самым устойчивым комплексным ионом из представленных является 1. [Co(NH3)6]3+, Kн ≈ 10-36 2. [Cu(NH3)4]2+, Kн ≈ 10-14 3. [Cd(CN)4]2-, Kн ≈ 10-17 4. [Ag(NH3)2]+, Kн ≈ 10-3 Ответ: 1 Правильно!
Вопрос: Комплексный ион [Ag(NH3)2]+ имеет __________ форму 1. линейную 2. тетраэдрическую 3. квадратную 4. октаэдрическую Ответ: 1 Правильно!
Вопрос: Концентрация ионов золота в 1 моль/л растворе соли K[Au(CN)2], если Кн = 1•10-39, составляет_______ 1. 2,9•10-12 2. 6,3•10-14 3. 2,2•10-16 4. 5,8•10-10 Ответ: 3 Неправильно!
тест "Комплексные соединения "
Вопрос: Осадок образуется при добавлении раствора Na2SO4 к раствору 1. K[Al(OH)4] 2. [Cu(NH3)4]SO4 3. Na2[Hg(CN)4] 4. Ba[Cu(CN)4] Ответ: 1 Неправильно!
Вопрос: Величина и знак заряда комплексного иона [Cr+3(H2O)2(OH)2Br2]х равны 1. 0 2. 1+ 3. 1- 4. 3+ Ответ: 2 Неправильно!
Вопрос: Соединение Na2[Zn(OH)4] относится к классу 1. кислот 2. солей 3. оснований 4. гидроксокомплексов Ответ: 4,2 Правильно!
Вопрос: Из соединений [Ni(NH3)4]Cl2 и NiCl2 большая степень гидролиза характерна для 1. [Ni(NH3)4]Cl2 2. NiCl2 3. одинакова 4. обе соли не гидролизуются Ответ: 2 Правильно!
Вопрос: Самым устойчивым комплексным ионом из представленных является 1. [Au(CN)2]-, Kн ≈ 10-39 2. [Cu(CN)4]2-, Kн ≈ 10-28 3. [Hg(CN)4]2-, Kн ≈ 10-41 4. [Cd(CN)4]2-, Kн ≈ 10-17 Ответ: 3 Правильно!
Вопрос: Комплексный ион [Cu(CN)4]2- имеет __________ форму 1. линейную 2. тетраэдрическую 3. квадратную 4. октаэдрическую Ответ: 2 Правильно!
Вопрос: Концентрация ионов золота в 1 моль/л растворе соли K[Au(CN)2], если Кн = 1•10-39, составляет_______ 1. 2,9•10-12 2. 6,3•10-14 3. 2,2•10-16 4. 5,8•10-10 Ответ: 1 Неправильно!
тест "Комплексные соединения "
Вопрос: Осадок образуется при добавлении раствора AgNO3 к раствору 1. [Pt(NH3)2Cl2] 2. Na[AgBr2] 3. [Co(NH3)5Cl][PtCl6] 4. [Cd(NH3)4]Cl2 Ответ: 4 Правильно!
Вопрос: Координационное число комплексообразователя равно 2 в соединении 1. [Pt(NH3)2Cl2] 2. [Ag(NH3)2]Cl 3. K[Au(S2O3)2] 4. [Cu(H2O)2(NH3)2]Cl2 Ответ: 2 Правильно!
Вопрос: Соединение H2[SiF6] относится к классу 1. кислот 2. солей 3. оснований 4. ацидокомплексов Ответ: 4,1 Правильно!
Вопрос: Из соединений [Ni(NH3)4](OH)2 и Ni(OH)2 более сильным основанием является 1. оба слабые 2. оба сильные 3. Ni(OH)2 4. [Ni(NH3)4](OH)2 Ответ: 4 Правильно!
Вопрос: Самым устойчивым комплексным ионом из представленных является 1. [Zn(NH3)4]2+, Kн ≈ 10-10 2. [Co(NH3)6]3+, Kн ≈ 10-36 3. [Cu(NH3)4]2+, Kн ≈ 10-14 4. [Ag(NH3)2]+, Kн ≈ 10-3 Ответ: 2 Правильно!
Вопрос: Комплексный ион [Au(CN)2]- имеет __________ форму 1. линейную 2. тетраэдрическую 3. квадратную 4. октаэдрическую Ответ: 1 Правильно!
Вопрос: Концентрация ионов CN- в 1 моль/л растворе соли K[Au(CN)2], если Кн = 1•10-39, составляет_______ 1. 2,9•10-14 2. 1,45•10-12 3. 1,26•10-13 4. 5,85•10-14 Ответ: 4 Неправильно!
