
- •Контрольные вопросы к экзамену учебной дисциплины «Биохимия»
- •2.Уровни структурной организации белков: первичная, вторичная, третичная, четвертичная, домены, надмолекулярные структуры
- •3. Связь свойств, функций и активности белков с их структурной организацией (специфичность, видовая принадлежность, эффект узнавания, динамичность, эффект кооперативного взаимодействия).
- •4. Факторы повреждения структуры и функции белков, роль повреждений в патогенезе заболеваний. Протеинопатии.
- •5. Первичная структура белков. Зависимость свойств и функций белков от их первичной структуры. Изменения первичной структуры, протеинопатии.
- •6. Роль протеомики в оценке патологических состояний
- •7.Миоглобин и гемоглобин. Конформационные изменения и кооперативные взаимодействия субъединиц гемоглобина. Эффект Бора. Роль 2,3 –бифосфоглицерата.
- •9. Кинетика ферментативных реакций. Уравнение Михаэлиса – Ментона. Преобразование Лайнуивера – Бэрка
- •10. Строение ферментов. Кофакторы и коферменты. Активный центр, строение, функции, связь со специфичностью действия ферментов. Возможность изменения специфичности (трансформация).
- •11. Международная классификация и номенклатура ферментов. Шифр ферментов. Классификация ферментов по их локализации в органах и клетках (компартментализация).
- •12. Ингибирование активности ферментов: обратимые, необратимые, конкурентные, неконкурентное. Принцип применения лекарственных препаратов, основанный на ингибировании ферментов (примеры).
- •1. Конкурентное ингибирование
- •2. Неконкурентное ингибирование
- •1. Специфические и неспецифические
- •2. Необратимые ингибиторы ферментов как
- •13. Изоферменты. Особенности строения и функционирования (рассмотреть на примере лдг). Значение определения изоферментного спектра ферментов в диагностике заболеваний.
- •14. Аллостерическая регуляция. Ингибирование по принципу обратной связи.
- •15. Регуляция активности и количества ферментов (аллостерическая, регуляция путем фосфорилирования и дефосфорилирования, ограниченного протеолиза проферментов)
- •16. Первичные и вторичные ферментопатии. Биохимические механизмы развития патологий. Примеры заболеваний.
- •17. Энзимодиагностика и энзимотерапия. Ингибиторы ферментов как лекарственные препараты
- •18. Зависимость скорости ферментативных реакций от температуры, рН, концентрации субстратов (индукция и репрессия ферментов). Индукция к лекарственным веществам.
- •19. Кофакторы и коферменты. Водорастворимые витамины, как предшественники коферментов. Металлоферменты и ферменты, активируемые металлами
- •1. Роль металлов в присоединении субстрата
- •2. Роль металлов в стабилизации третичной
- •3. Роль металлов в ферментативном
- •4. Роль металлов в регуляции активности
- •1. Механизм "пинг-понг"
- •2. Последовательный механизм
- •Модуль II. Введение в обмен веществ. Биологическое окисление
- •20. Основные пищевые вещества. Суточная потребность. Незаменимые факторы питания
- •21.Переваривание основных пищевых веществ (жиров, белков, углеводов), ферменты пищеварительных соков. Наследственная непереносимость пищевых веществ.
- •22. Витамины. Классификация, функции. Алиментарные и вторичные авитаминозы и гиповитаминозы, их следствия, подходы к профилактике.
- •1. Образование и роль соляной кислоты
- •2.Механизм активации пепсина
- •3.Возрастные особенности переваривания белков в желудке
- •4. Нарушения переваривания белков в желудке
- •1. Активация панкреатических ферментов
- •2. Специфичность действия протеаз
- •24. Биологическое окисление. Особенности, функции. Макроэргические соединения. Синтез атф. Аэробный и субстратный типы окислительного фосфорилирования Превращение метаболической энергии в тепло.
- •25. Характеристика мультиферментных комплексов цепи переноса электронов. Структурная организация дыхательной цепи, ее функции (энергетическая, терморегуляторная) и место в системе дыхания
- •28. Микросомальное окисление, его организация, биологическая роль, связь с условиями внешней среды. Возможные побочные эффекты.
- •30. Механизм защиты от токсического действия кислорода. Антиоксидантная система
- •2. Антиоксидантная система
- •32. Нарушения энергетического обмена, причины. Гипоэнергетические (энергодефицитные) состояния, их причины и последствия.
- •Гипоэнергетические состояния
- •33. Окислительное декарбоксилирование пировиноградной кислоты. Строение пируватдегидрогеназного комплекса, роль витамина в-1
- •34. Цикл лимонной кислоты (цикл Кребса), последовательность реакций, характеристика окислительных ферментов, связь с цепью переноса электронов, энергетическая и пластическая функции.
- •Модуль III. Обмен и функции углеводов
- •35. Метаболизм фруктозы и галактозы, связь с онтогенезом. Галактоземия, фруктозурия.
- •36. Основные углеводы пищи. Общая схема источников и путей расходования глюкозы в организме.
- •37. Гликолиз, последовательность реакций, связь с общими путями катаболизма (полное аэробное окисление глюкозы). Физиологическая роль процесса.
- •38. Анаэробное окисление глюкозы (анаэробный гликолиз), последовательность реакций, физиологическое значение, регуляция. Судьба молочной кислоты.
- •39. Метаболизм фруктозы и галактозы, связь с онтогенезом. Галактоземия, фруктозурия.
- •40. Пентозофосфатный путь превращения глюкозы, окислительные реакции, энергетическая функция, образование восстановительных эквивалентов и рибозы.
- •41. Глюконеогенез. Ключевые реакции, роль пирувата, лактата, аминокислот. Значение процесса, регуляция. Роль биотина.
- •42. Синтез и распад гликогена: биологическое значение процесса. Зависимость от ритма питания. Регуляция. Гликогенозы и агликогенозы.
- •43. Поддержание физиологического уровня глюкозы в крови. Цикл Кори и глюкозо-аланиновый цикл.
- •44. Гипо- и гипергликемия, почечный порог для глюкозы, глюкозурия. Толерантность к глюкозе.
- •45. Особенности обмена глюкозы в различных тканях (мышцы, эритроциты, мозг, жировая ткань, печень). Зависимость путей использования глюкоза от ритма и характера питания.
- •Модуль IV. Структура, функция и обмен липидов. Биологические мембраны, строение, функции
- •47. Повреждение мембран, связь с развитием болезней. Основные повреждающие факторы. Перекисное окисление липидов (пол). Роль неблагоприятной экологической обстановки в активации этого процесса.
- •49. Ненасыщенные и полиненасыщенные (пнжк) жирные кислоты. Зависимость их концентрации от питания. W-3 и w-6 жирные кислоты как предшественники синтеза эйкозаноидов, простагландинов и лейкотриенов.
- •50. Транспортные липопротеины крови, особенности строения, функции. Апобелки. Роль липопротеинлипазы и лецитин-холестерин-ацилтрансферазы (лхат).
- •51.Метаболизм плазменных липопротеинов. Атерогенные и антиатерогенные липопротеины. Дислипопротеинемии, гиперлипопротеинемии. Атеросклероз. Коэффициент атерогенности.
- •52. Различия синтеза триацилглицеринов (таг) в печени и жировой ткани. Взаимопревращение глицерофосфолипидов. Жировое перерождение печени. Липотропные факторы.
- •53. Депонирование и мобилизация жиров, биологическая роль процессов, зависимость от ритма питания и физической нагрузки. Гормональная регуляция липолиза и липогенеза.
- •55. Синтез и использование кетоновых тел. Гиперкетонемия, кетонурия, ацидоз при сахарном диабете и голодании.
- •56. Синтез и функции холестерина. Образование мевалоновой кислоты. Регуляция процесса, гмг-КоА-редуктаза. Транспорт и выведение холестерина из организма.
- •57. Обмен полиненасыщенных жирных кислот. Образование эйкозаноидов, строение, номенклатура, биосинтез, биологическая роль.
- •58. Желчь, желчные кислоты (первичные и вторичные). Желчные мицеллы их образование и роль Применение хенодезоксихолевой кислоты для лечения болезни.
- •59.Синтез жирных кислот, пальмитат синтетазный комплекс, строение, последовательность реакций. Источники восстановительных эквивалентов. Микросомальная система удлинения жирных кислот.
- •Модуль V. Обмен белков и аминокислот
- •2. Оксидаза l-аминокислот
- •3. Оксидаза d-аминокислот
- •3. Биологическое значение трансаминирования
- •2. Органоспецифичные аминотрансферазы ант и act
- •1. Реакции синтеза мочевины
- •2. Энергетический баланс процесса
- •3. Биологическая роль орнитинового цикла
- •Модуль VI. Обмен и функции нуклеиновых кислот. Матричные биосинтезы.
- •Модуль VII. Гормоны. Гормональная регуляция метаболических процессов
- •81. Гормоны поджелудочной железы. Строение, образование, механизм действия инсулина и глюкагона.
- •82. Кальций и фосфор. Биологические функции, распределение в организме. Регуляция обмена, участие паратгормона, кальцитонина и активных форм витамина d.
- •83. Гормоны коры надпочечников: минерало - и глюкокортикоиды. Строение, синтез. Влияние на водно-солевой обмен, обмен белков, липидов и углеводов.
- •84. Йодсодержащие гормоны, строение, биосинтез, Влияние на обмен веществ. Изменения обмена при гипертиреозе и гипотиреозе.
- •85. Адреналин. Строение, биосинтез, биологическая роль.
- •86. Гормоны передней доли гипофиза, строение, место в системе регуляции. Биологическая роль.
- •87. Гормоны задней доли гипофиза (вазопрессин и окситоцин), строение, биологическая роль.
- •88. Половые гормоны: мужские и женские, влияние на обмен веществ.
- •89. Гипер- и гипопродукция гормонов (разобрать на примерах гормонов щитовидной железы, надпочечников). Модуль VIII. Биохимия крови и мочи
- •90. Общий белок и белковый спектр плазмы крови. Альбумины и глобулины их функции, гипо - и гиперпротеинемия, диспротеинемии, парапротеинемии.
- •92.Каликреин-кининовая система, синтез кининов, биологическая роль.
- •93. Форменные элементы крови. Особенности метаболизма в эритроцитах и лейкоцитах. Биохимические механизмы, обеспечивающие резистентность эритроцита.
- •94. Синтез гема и гемоглобина. Регуляция этих процессов. Вариации первичной структуры и свойств гемоглобина. Гемоглобинопатии.
- •95. Железо. Транспорт, депонирование, функции, обмен. Нарушения обмена: железодефицитная анемия, гемосидероз, гемохроматоз.
- •96.Дыхательная функция крови. Молекулярные механизмы газообмена в легких и тканях. Факторы, влияющие на насыщение гемоглобина кислородом. Карбоксигемоглобин, метгемоглобин.
- •97.Ферменты крови «собственные» и поступающие при повреждении клеток. Диагностическая ценность анализа белков и ферментов крови
- •98. Белки и ферменты крови. Белки «острой фазы». Физиологически активные пептиды (кининовая система).
- •99. Распад гема, образование, обезвреживание и выделение билирубина. Конъюгированный и неконъюгированный билирубин. Гипербилирубинемии.
- •100. Виды желтух (гемолитическая, паренхиматозная, обтурационная, новорожденных). Диагностическое значение определения билирубина в крови и моче.
- •101. Буферные системы крови: бикарбонатная, фосфатная, белковая, гемоглобиновая. Причины развития и формы ацидоза и алкалоза. Возможные последствия этих отклонений.
- •102. Состав мочи. Нормальные и патологические компоненты. Исследование мочи с целью диагностики болезней.
- •103. Клиническое значение биохимического анализа крови (белки, ферменты, глюкоза, мочевина, железо, кальций и др.).
- •Модуль iх. Биохимии отдельных органов и тканей: соединительной, мышечной, нервной
- •113. Биохимические основы проведения нервного импульса. Роль ферментов, медиаторов, атф, мембранных белков, кальция, калия и натрия.
2. Энергетический баланс процесса
В реакциях орнитинового цикла расходуются четыре макроэргических связи трёх молекул
484

Рис. 9-17. Цикл регенерации аспартата, сопряжённый с орнитиновым циклом.
АТФ на каждый оборот цикла. Однако процесс превращения аминокислот в безазотистые остатки и мочевину имеет пути компенсации энергозатрат:
при включении фумарата в ЦТК на стадии дегидрирования малата образуется NADH, который обеспечивает синтез 3 молекул АТФ (рис. 9-18);
при окислительном дезаминировании глу-тамата в разных органах также образуется NADH, соответственно - ещё 3 молекулы АТФ.
Затраты энергии происходят также и при трансмембранном переносе веществ, связанном с синтезом и экскрецией мочевины (рис. 9-18). Первые две реакции орнитинового цикла происходят в митохондриях, а последующие три - в цитозоле. Цитруллин, образующийся в митохондрии, должен быть перенесён в цитозоль, а орнитин, образующийся в цитозоле, необходимо транспортировать в митохондрию. Кроме того, в почках перенос мочевины из крови в мочу происходит путём активного транспорта за счёт градиента ионов натрия, создаваемого К+,Nа+-АТФ-азой, что тоже сопряжено с энергозатратами.
Полный набор ферментов орнитинового цикла есть только в гепатоцитах. Отдельные же ферменты орнитинового цикла обнаруживаются не только в печени, но и в других клетках. В энтероцитах, например, имеется карбамоилфосфат-синтетаза I и орнитинкарбамоилтрансфераза, следовательно, может синтезироваться цитруллин. В почках обнаружены аргининосукцинатсинтетаза и аргининосукцинатлиаза. Цитруллин, образовавшийся в энтероцитах, может поступать в почки и превращаться там в аргинин, который переносится в печень и гидролизуется аргиназой. Активность этих рассеянных по разным органам ферментов значительно ниже, чем в печени.
3. Биологическая роль орнитинового цикла
Кребса-Гензелейта
Орнитиновый цикл в печени выполняет 2 функции:
превращение азота аминокислот в мочевину, которая экскретируется и предотвращает накопление токсичных продуктов, главным образом аммиака;
синтез аргинина и пополнение его фонда в организме.
Регуляторные стадии процесса - синтез карбамоилфосфата, синтез цитруллина и заключительная стадия, катализируемая аргиназой. Эффективность работы орнитинового цикла при нормальном питании человека и умеренных физических нагрузках составляет примерно 60% его мощности. Запас мощности необходим для избежания гипераммониемии при изменениях количества белка в пище. Увеличение скорости синтеза мочевины происходит при длительной физической работе или длительном голодании, которое сопровождается распадом тканевых белков. Некоторые патологические состояния, характеризующиеся интенсивным распадом белков

Рис. 9-18. Взаимосвязь орнитинового цикла и общего пути катаболизма. Фумарат, образующийся в результате расщепления аргининосукцината, превращается в малат, который затем переносится в митохондрии, включается в ЦТК и дегидрируется с образованием оксалоацетата. Эта реакция сопровождается выделением 3 молекул АТФ, которые и компенсируют затраты энергии на синтез одной молекулы мочевины.
тканей (сахарный диабет и др.), также сопровождаются активацией орнитинового цикла. При избыточном белковом питании количество ферментов орнитинового цикла в печени увеличивается, что приводит к интенсификации синтеза мочевины.
66.2
Гипераммониемия -Повышенное содержание свободных ионов аммония в крови; врожденные формы Г. (связаны с тяжелой умственной отсталостью и др. симптомами) обусловлены дефицитом ферментов орнитин-транскарбамилазы печени (ген OTC локализован на участке p21.1 Х-хромосомы) или карбамоилфосфатсинтетазы (ген CPS1 локализован на коротком плече хромосомы 2).
Гипераммониемия — это нарушение обмена веществ, проявляющееся в недостаточности цикла ферментов мочевины, приводящее к отравлению организма аммиаком. Аммиак является токсичным соединением, находящимся в крови в относительно небольших концентрациях (11,0—32,0 мкмоль/л). Симптомы аммиачного отравления проявляются при превышении этих пределов всего в 2—3 раза. Предельно допустимый уровень аммиака в крови 60 мкмоль/л. При повышении концентрации аммиака (гипераммониемия) до предельных величин может наступить кома и смерть. При хронической гипераммониемии развивается умственная отсталость. Транзиторной гипераммониемией называется также пограничное состояние, присущее новорожденным детям в период адаптации к внеутробной жизни, проявляющееся обычно на вторые—третьи сутки жизни. Этот вид гипераммониемии встречается чаще всего у недоношенных детей с задержкой внутриутробного развития, с частотой до пятидесяти процентов рождений, однако иногда регистрируется и у доношенных малышей. Часть детей не проявляет симптоматики клинической картины гипераммониемии: признаки угнетения центральной нервной системы(вялость, понижение мышечного тонуса, приступы апноэ, ослабленная реакция зрачков на свет, отказ от еды, ступор и кома), а также расстройства дыхательной функции, желтуха, судороги и обезвоживание. Причиной, вызывающей гипераммониемию, называют кислородное голодание, или гипоксию, во время беременности и в процессе родов.
Приобретённые формы
Приобретённая (вторичная) гипераммониемия развивается вследствие заболеваний печени и вирусных инфекций. В крайне тяжёлых случаях она проявляется как тошнота, рвота, судороги, нечленораздельная речь, затуманивание зрения, тремор, нарушение координации движений. Наследственные формы
Наследственные формы гипераммониемии вызваны генетическим дефектом любого из пяти ферментов синтеза мочевины. Соответственно ферменту заболевание делится на пять типов. Первичными признаками гипераммониемий являются сонливость, отказ от пищи, рвота, беспокойство, судороги, нарушение координации движений, тахипноэ, дыхательныйалкалоз. Могут развиться печёночная недостаточность, лёгочные и внутричерепные кровоизлияния.
Наиболее частой является гипераммониемия типа II, связанная с недостатком орнитин-карбамоилтрансферазы. Заболевание рецессивно, сцеплено с Х-хромосомой. У матери также наблюдается гипераммониемия и отвращение к белковым продуктам. При полном дефекте фермента наследственные гипераммониемии имеют раннее начало (в период до 48 часов после рождения).
Лабораторным критерием заболевания является накопление глутамина (в 20 и более раз) и аммиака в крови, ликворе и моче.
Основа лечения гипераммониемий сводится к ограничению белка в диете, уже это позволяет предотвратить многие нарушения мозговой деятельности.
Причины Гипераммониемии:
Токсичность аммиака обусловлена следующими обстоятельствами:
1. Связывание аммиака при синтезе глутамата вызывает отток α-кетоглутарата из цикла трикарбоновых кислот, при этом понижается образование энергии АТФ и ухудшается деятельность клеток.
2. Ионы аммония NH4+ вызывают защелачивание плазмы крови. При этом повышается сродство гемоглобина к кислороду (эффект Бора), гемоглобин не отдает кислород в капиллярах, в результате наступает гипоксия клеток.
3. Накопление свободного иона NH4+ в цитозоле влияет на мембранный потенциал и работу внутриклеточных ферментов — он конкурирует с ионными насосами для Na+ и K+.
4. Продукт связывания аммиака с глутаминовой кислотой — глутамин — является осмотически активным веществом. Это приводит к задержке воды в клетках и их набуханию, что вызывает отёк тканей. В случае нервной ткани это может вызвать отёк мозга, кому и смерть.
Гипераммониемия
Нарушение реакций обезвреживания аммиака может вызвать повышение содержания аммиака в крови - гипераммониемию, что оказывает токсическое действие на организм. Причинами гипераммониемии могут выступать как генетический дефект ферментов орнитинового цикла в печени, так и вторичное поражение печени в результате цирроза, гепатита и других заболеваний. Известны пять наследственных заболеваний, обусловленных дефектом пяти ферментов орнитинового цикла (табл. 9-4).
В литературе описаны случаи всех этих довольно редких энзимопатий, среди которых отмечено больше всего случаев гипераммониемии II типа.
Нарушение орнитинового цикла наблюдается при гепатитах различной этиологии и некоторых других вирусных заболеваниях. Например, установлено, что вирусы гриппа и других острых респираторных вирусных инфекций снижают активность карбамоилфосфатсинтетазы I. При циррозе и других заболеваниях печени также часто наблюдают гипераммониемию.
Снижение активности какого-либо фермента синтеза мочевины приводит к накоплению в крови субстрата данного фермента и его предшественников. Так, при дефекте аргининосук-цинатсинтетазы повышается содержание цитруллина (цитруллинемия); при дефекте аргиназы - концентрация аргинина, аргининосукцината, цитруллина и т.д. При гипераммониемиях I и II типа вследствие дефекта орнитинкарбамоилтрансферазы происходит накопление карбамоилфосфата в митохондриях и выход его в цитозоль. Это вызывает увеличение скорости синтеза пиримидиновых нуклеотидов (вследствие активации карбамоилфосфатсинтетазы II), что приводит к накоплению оротата, уридина и урацила и выведению их с мочой. Содержание всех метаболитов повышается, и состояние больных ухудшается при увеличении количества белков в пище. Тяжесть течения заболевания зависит также от степени снижения активности ферментов.
Все нарушения орнитинового цикла приводят к значительному повышению в крови концентрации аммиака, глутамина и аланина.
Гипераммониемия сопровождается появлением следующих симптомов:
тошнота, повторяющаяся рвота;
головокружение, судороги;
потеря сознания, отёк мозга (в тяжёлых случаях);
отставание умственного развития (при хронической врождённой форме).
Таблица 9-4. Наследственные нарушения орнитинового цикла и основные их проявления
|
Заболевание |
Дефект фермента |
Тип наследования |
Клинические проявления |
Метаболиты | |
|
кровь |
моча | ||||
|
Гиперам- мониемия, тип I |
Карбамоил- фосфат- синтетаза I |
Аутосомно- рецессивный |
В течение 24-48 ч после рождения кома, смерть |
Глн Ала NH3 |
Оротат |
|
Гиперам- мониемия, тип II |
Орнитин- карбамоил- трансфераза |
Сцепленный с Х-хромосомой |
Гипотония, снижение толерантности к белкам |
Глн Ала NH3 |
Оротат |
|
Цитрул- линемия |
Аргинино- сукцинат- синтетаза |
Аутосомно- рецессивный |
Гипераммониемия тяжёлая у новорождённых. У взрослых - после белковой нагрузки |
Цитруллин NH3 |
Цитруллин |
|
Аргинино- сукцина- турия |
Аргинино- сукцинат- лиаза |
Аутосомно-рецессивный |
Гипераммонимия, атаксия, судороги, выпадение волос |
Аргини- носукцинат NH3 |
Аргини- носукци- нат, Глн, Ала, Лиз |
|
Гиперар- гининемия |
Аргиназа |
Аутосомно-рецессивный |
Гипераргининемия |
Apr NH3 |
Apr Лиз Орнитин |
Все симптомы гипераммониемии - проявление действия аммиака на ЦНС (см. выше подраздел IV, Б).
Для диагностики различных типов гипераммониемии производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, акгивности фермента в биоптатах печени.
Основной диагностический признак - повышение концентрации аммиака в крови. Содержание аммиака в крови может достигать 6000 мкмоль/л (в норме - 60 мкмоль/л). Однако в большинстве хронических случаев уровень аммиака может повышаться только после белковой нагрузки или в течение острых осложнённых заболеваний.
Лечение больных с различными дефектами орнитинового цикла в основном направлено на снижение концентрации аммиака в крови за счёт малобелковой диеты, введения кетоаналогов аминокислот в рацион и стимуляцию выведения аммиака в обход нарушенных реакций:
путём связывания и выведения NH3 в составе фенилацетилглутамина и гишгуровой кислоты;
повышением концентрации промежуточных метаболитов цикла (аргинина, цитруллина, глутамата), образующихся вне блокируемых реакций (рис. 9-19).
Вводимый больным с дефектом карбамоил-фосфатсинтетазы I в качестве пищевой добавки фенилацетат в результате его конъюгации с глутамином образует фенилацетилглутамин, который экскретируется почками. Состояние больных при этом улучшается, так как происходит активация синтеза глутамина и снижение концентрации аммиака в крови (рис. 9-19, А).
Аналогичное действие оказывает введение бензоата, который связывает молекулу глицина. Образующаяся пшпуровая кислота выводится с мочой (рис. 9-19, Б). В составе гиппурата происходит выделение азота из организма. Недостаток глицина компенсируется либо путём синтеза его из серина, либо за счёт образования из NH3 и СО2 в реакции, катализируемой глицинсинтетазой. При этом образование глицина сопровождается связыванием одной молекулы аммиака.
При гипераммониемии II типа (дефект орнитинкарбамоилтрансферазы) введение больших доз цитруллина стимулирует синтез мочевины из аспартата (рис. 9-19, В), что также приводит к вьшедению азота из организма. Введение больших доз аргинина при аргининосукцинатурии (дефект аргининосукцинатлиазы) стимулирует регенерацию орнитина и выведение азота в составе цитруллина и аргининосукцината.
67. Декарбоксилирование аминокислот. Биогенные амины, образование, биологическая роль, и инактивация. Роль витамина В6.
Декарбоксилирование аминокислот.
Процесс отщепление карбоксильной группы в виде СО2 называется декарбоксилированием и приводит к образованию биогенных аминов, которые оказывают фармакологическое действие на физиологические функции человека.
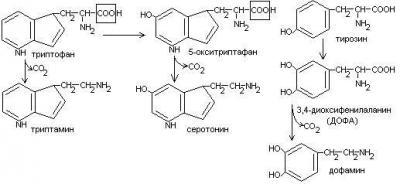
Серотонин обладает сосудосуживающим действием, участвует в регуляции артериального давления, t тела, дыхания, медиатор нервных процессов.
Дофамин- предшественник катехоламинов.

гистидин гистамин
Гистамин обладает сосудорасширяющим действием. Он образуется в области воспаления, участвует в развитии аллергических реакций.
НООС-(СН2)2-СН-СООH →СН2-СН2-СН2-СООН
| |
глутамат NH2 NH2 γ аминомасляная кислота (ГАМК)
ГАМК является тормозным медиатором. В лечебной практике используется при лечении эпилепсии (резкое сокращение частоты припадков).
Орнитин декарбоксилируясь дает диамин – путресцин, а лизин – кадаверин.
СН2-СН2-СН2-СН-СООН →СН2-СН2-СН2-СН2-NH2;
| | |
NH2 NH2 NH2
CH2-CH2-CH2-CH2-CH-COOH → СН2-СН2-СН2-СН2-CH2-NH2
| | |
NH2 NH2 NH2
В организме биогенные амины подвергаются реакции окислительного дезаминирования с образованием альдегидов и аммиака. Процесс осуществляется при участии моноаминооксидаз.
Схематически механизм трансдезаминирования можно представит так:

68. Метионин. Реакции метилирования. Роль фолиевой кислоты, витамина В12. Значение реакций, примеры.
69. Обмен фенилаланина и тирозина. Образование биологически активных соединений. Фенилкетонурия. Алкаптонурия, альбинизм.
