
- •5. Биологические функции и классификация белков.
- •6. Значение и специфичность действия ферментов.
- •7. Строение фермента.
- •8. Активный центр.
- •9. Определение активности ферментов.
- •10. Локализация ферментов в клетке, маркёрные и органоспецифические ферменты.
- •11. Механизм действия ферментов.
- •12 . Кинетика ферментативных реакций.
- •13. Регуляция активности ферментов.
- •14. Ингибирование ферментов.
- •15 . Номенклатура и классификация. Изоферменты. Изменение активности в энтогенезе.
- •15 . Энзимопатия.
- •16. Обмен веществ. Ката- и анаболизм .
- •17.Биологическое окисление.
- •18. Природа макроэргичности атф.
- •19. Цикл кребса.
- •20 . Тканевое дыхание.
- •21 . Дыхательная цепь.
- •22. Механизм сопряжения окислительного фосфорилирования.
- •23 . Термогенез.
- •24 . Микросомальная дыхательная цепь.
- •25 . Перекисное окисление и антиоксидантная защита.
- •26 . Углеводы и их переваривание.
- •1) Гиалуроновая кислота.
- •2) Кондратин – сульфат
- •3) Гепарин
- •27 . Биологические функции углеводов.
- •28 . Переваривание углеводов .
- •Галактоза
- •Фруктоза
- •29 . Пути метаболизма глюкозы.
- •30 . Синтез и распад гликогена.
- •31.Гликогенозы.
- •32 . Гликогенолиз и гликолиз.
- •33. Механизм гликолитической оксидоредукции. Субстратное фосфорилирование.
- •34 . Спиртовое брожение и метаболизм этанола.
- •34.Эробный распад глюкозы. Окислительное декарбоксилиро -
- •35. Глюконеогенез.
- •36. Гипо - и гипергликемия.
- •37.Регуляция уровня глюкозы в крови.
- •38. Сахарный диабет.
- •39. Липиды . Строение , классификация , биологическая роль .
- •40.Переваривание и всасывание липидов .
- •41. Ресинтез липидов в стенке кишечника .
- •42 . Метаболизм липидов .
- •45. Пути обмена ацетил-КоА . Обмен кетоновых тел .
- •46. Биосинтез триглицеридов.
- •47. Интеграция углеводного и липидного обмена .
- •48. Белковый обмен.
- •49. Состав желудочного сока. Механизм секреции hCl .
- •9. Ряд аминокислот, имеющих диагностическое значение .
- •50. Панкреатический сок.
- •51. Кишечный сок.
- •1.Энтерокиназа .
- •9. Фосфолипаза и липаза .
- •52 . Переваривание белков .
- •53. Гниение белков в толстом кишечнике .
- •54. Механизм всасывания аминокислот и пути их утилизации .
- •55.Трансаминирование аминокислот .
- •56. Токсичность аммиака и пути его обезвреживания .
- •57. Биосинтез мочевины .
- •58. Цикл кребса-гензеляйта .
- •59. Пути вступления аминокислот в цтк .
- •60. Декарбоксилирование аминокислот .
- •61.Метаболизм серина и глицина .
- •62. Нарушение обмена глицина .
- •63. Обмен серосодержащих аминокислот и триптофана.
- •64. Метаболизм триптофана.
- •65. Обмен фенилаланина и тирозина.
- •66. Обмен гистидина, глутамина, аспарагина, пролина.
- •67. Интеграция углеводного, белкового и липидного обмена.
- •72. Распад пуриновых нуклеотидов. Подагра.
- •73. Синтез и распад пиримидиновых оснований.
60. Декарбоксилирование аминокислот .
Общая схема процесса декарбоксилирования :
 R – CH – COOH R –
CH2
– NH2
+ CO2
R – CH – COOH R –
CH2
– NH2
+ CO2
|
NH2
В животных организмах открыто 4 типа декарбоксилирования :
1. а-декарбоксилирование ( отщепление СОО-группы , стоящей по соседству с а-углеродным атомом ) . Продукты – СО2 и биогенные амины .
a
 R – CH –
COOH R
– CH2
– NH2
R – CH –
COOH R
– CH2
– NH2
| - CO2
NH2
2.w-декарбоксилирование ( характерно для микробов ). Таким путём из АСП образуется а-аланин .
 HOOC – CH2
– CH – COOH CH3
– CH – COOH
HOOC – CH2
– CH – COOH CH3
– CH – COOH
| - CO2 |
NH2 NH2
аспартат аланин
3. Декарбоксилирование , связанное с трансаминированием .
R1 R2 R1 R2
| | | |
 CH – NH2
+ C = O
C = O
+ CH – NH2
CH – NH2
+ C = O
C = O
+ CH – NH2
| | - CO2 | |
COOH COOH H COOH
альдегид новая аминокислота
4.Декарбоксилирование , связанное с конденсацией молекул .
R1 R2 R1
| | |
 CH
– NH2
+ CO – S – KoA
CH – NH2
+ HSKoA
CH
– NH2
+ CO – S – KoA
CH – NH2
+ HSKoA
| - CO2 |
COOH CO – R2
Открыт ещё одна реакция декарбоксилирования , сопряжённая с генерацией энергии АТФ .Этот анаэробный механизм утилизирует глицин в качестве единственного источника углерода , превращая его в ацетат :
 2CH2
– COOH + 2 НАД + АДФ
+ Фн + 2НОН
2CO2
+2NH3
+ CH3COOH
+ АТФ
2CH2
– COOH + 2 НАД + АДФ
+ Фн + 2НОН
2CO2
+2NH3
+ CH3COOH
+ АТФ
глицин
+ НАД*Н2
Р









 еакции
декарбоксилирования в отличии от
других процессов обмена аминокислот
являются необратимыми . Они катализируются
специфическими ферментами –
декарбоксилазами аминокислот , каждая
из которых состоит из белковой части
и простетической группы , представленной
пиридоксальфосфатом . Исключение
составляют гистидиндекарбоксилаза
Micrococcus и Lactobacillus
и S-аденозилметиониндекарбоксилаза
E.coli ,
содержащие вместо пиридоксальфосфата
остаток ПВК . Но эти декарбоксилазы
в животных тканях содержат
пиридоксальфосфат .
еакции
декарбоксилирования в отличии от
других процессов обмена аминокислот
являются необратимыми . Они катализируются
специфическими ферментами –
декарбоксилазами аминокислот , каждая
из которых состоит из белковой части
и простетической группы , представленной
пиридоксальфосфатом . Исключение
составляют гистидиндекарбоксилаза
Micrococcus и Lactobacillus
и S-аденозилметиониндекарбоксилаза
E.coli ,
содержащие вместо пиридоксальфосфата
остаток ПВК . Но эти декарбоксилазы
в животных тканях содержат
пиридоксальфосфат .


 CH2
– CH – COOH CH2
– CH – COOH
CH2
– CH – COOH CH2
– CH – COOH




 |
OH
|
|
OH
|



 NH2
О
NH2
NH2
О
NH2



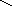 NH
NH
NH











 ТРП
5-окси-ТРП
ТРП
5-окси-ТРП

 СО2
СО2
 CO2
CO2

 CH2
– CH2
– NH2
CH2
– CH2
– NH2





 CH2
– CH2
– NH2
OH
CH2
– CH2
– NH2
OH





NH
NH
триптолин серотонин ( медиатор ЦНС , повышает АД , регули
(оказывает сосудосуживающее действие ) рует температуру тела , почечную фильтрацию , ды
COOH хание , вазорецепторы , участвует в развитии






 | аллергии
,токсикоза беременности , геморраги
| аллергии
,токсикоза беременности , геморраги

 ОН
СН2 – СН
ческих диатезов
.
ОН
СН2 – СН
ческих диатезов
.
|
 NH2
NH2
ОН
ДОФА


СО2








 НО
CH2
– CH2
НО
CH2
– CH2
|
 NH2
NH2
НО
ДОФамин ( предшественник катехоламинов )
В

 животных тканях с высокой скоростью
протекает реакция декарбоксилирования
гистидина , катализируемая специфической
гистидиндекарбоксилазой .
животных тканях с высокой скоростью
протекает реакция декарбоксилирования
гистидина , катализируемая специфической
гистидиндекарбоксилазой .
 N CH2
– CH – COOH CH2
– CH2
– NH2
N CH2
– CH – COOH CH2
– CH2
– NH2








 |
|


 NH2
- CO2
NH2
- CO2
NH NH
Гистидин гистамин
Гистамин – вазомедиатор , образуется воспаления , вызывая расширение сосудов в очаге воспаления, тем самым ускоряя приток лейкоцитов ,участвует в секреции соляной кислоты , имеет прямое отношение к сенсибилизации и десенсибилизации , является медиатором боли . глутаматдекарбоксилаза
 HOOC – CH – CH2
– CH2
– COOH
H2N
– CH2
– CH2
– CH2
– COOH
HOOC – CH – CH2
– CH2
– COOH
H2N
– CH2
– CH2
– CH2
– COOH
| - CO2 АМК ( медиатор торможения деятель
NH2 ГЛУ ности ЦНС , используется для лечения эпи
лепсии )
В животных тканях с высокой скоростью декарбоксилируются цистеиновая и цистеинсульфиновая кислоты .
CH2 – SO2H CH2 – SO3H

 |
|
|
|
C H
– NH2 O
CH – NH2
H
– NH2 O
CH – NH2
| |
COOH COOH
цистеинсульфиновая цистеиновая кислота

 кислота
кислота


СО2 СО2


CH2 – SO2H O CH2 – SO3H
 | |
| |
CH2 – NH2 CH2 – CH2
Гипотаурин таурин ( используется для синтеза парных желчных кислот )
Недавно были открыты два фермента , катализирующих декарбоксилирование аргинина и 5-аденозилметионина .
CH2 – NH2 CH2 – NH2
| |
(CH2)2 орнитиндекарбоксилаза (CH2)2
 | |
| |
CH – NH2 - CO2 CH2 – NH2
|
COOH
C H3
A
CH3
A
H3
A
CH3
A




 |
O
аденозинметионин |
O
|
O
аденозинметионин |
O
+






 S
H2C
+S H2C
S
H2C
+S H2C

 |
карбоксилаза
|
|
карбоксилаза
|
C



 H
– NH2
(CH2)2
H
– NH2
(CH2)2
| OH OH | OH OH
COOH CH2 – NH2
S-аденозилметионин S-метиладенозилалоцистеин
Эти продукты используются для синтеза полиаминов , которые необходимы для регуляции биосинтеза нуклеиновых кислот и белка . Однако накопление биогенных аминов может отрицательно сказаться на функциональном статусе . Поэтому в организме существуют специальные пути их обезвреживания , которые в общем виде сводятся к окислительному дезаминированию с образованием альдегидов и аммиака .
O
+ O2 //
R – CH2
– NH2
+ H2O
моноаминооксидаза
R – C
+ NH3
+ H2O2
– CH2
– NH2
+ H2O
моноаминооксидаза
R – C
+ NH3
+ H2O2
\
H
