
- •Введение
- •Нейромедиаторы центральной нервной системы
- •Синапс торможения
- •Седативно-снотворные средства
- •Нейростимуляторы и конвульсанты
- •Местные и общие анальгетики
- •Местные анальгетики
- •Опиатные анальгетики
- •Галлюциногены
- •Антипсихотические средства
- •Психотические средства
- •Введение ………………………………………………………… 3
-
Опиатные анальгетики
В течение многих лет опиум – высохший млечный сок из повреж-дённых зелёных семенных коробочек мака Papaver somniferum, использо-вался в медицине в качестве снотворного и общего обезболивающего средства. Ещё в ХIХ веке и в начале двадцатого века во всех домашних аптечках были опийные капли, которые принимали при болях в желудке и при кишечных расстройствах, а до середины ХХ века в аптеках можно было свободно получить один из алкалоидов опиума кодеин в таблетках от кашля, однако распространение наркомании привело к строгому ограниче-нию доступа ко всем опиатным алкалоидам. При изучении химического состава опиума из него в 1804 году было выделено в кристаллическом виде основное действующее вещество, получившее название морфин по имени древнегреческого бога сновидений Морфея. Химическое строение морфина было установлено в 1925 году (Р.Робертсон):

Обезболивающее действие морфина сопровождается целым рядом побочных эффектов, среди которых эйфория, эффект привыкания (при длительном приеме доза должна постоянно увеличиваться), запоры и подавление дыхательного рефлекса, поэтому для снятия часто повторяю-щихся или постоянных болей морфин непригоден. Выделение из опиума чистого кристаллического морфина породило иллюзии, что это очищенное соединение окажется гораздо более безопасным, чем исходная смесь алка-лоидов. Однако и чистый морфин оказался наркотиком, опасность выра-ботки болезненного пристрастия к которому долгое время недооценива-лась. В результате частого, но как казалось контролируемого, употребле-ния морфина (других эффективных снотворных препаратов и средств для обезболивания тогда просто не существовало) многие пациенты и врачи (писатель М.А.Булгаков, рассказ «Морфий») стали наркозависимыми.
После установления химического строения морфина были предпри-няты многочисленные опыты по синтезу его структурных аналогов с целью получения средств для обезболивания, которые были бы менее токсичны (у морфина ЛД50 на собаках при внутривенном введении состав-ляет 316 мг/кг) и лишены опасных побочных эффектов, сопровождающих лекарственное использование этого вещества. Алкалоиды мака и их произ-водные представляют собой классический пример для демонстрации био-активности через хеморецепцию. Они взаимодействуют с соответствую-щими рецепторами стереоспецифично, и их оптические изомеры могут очень сильно отличаться по биоактивности. Ещё одним следствием этого является возможность получения агонистов и антагонистов в результате сравнительно небольших изменений в строении молекул. Так, например, замена в молекуле морфина группы NСН3 на группу NСН2СН=СН2 приводит к антагонисту морфина – налорфину, который использовался для спасения наркоманов, принявших слишком высокую дозу наркотика. Сейчас от налорфина отказались из-за его галлюциногенных свойств.
Упрощение структуры морфина с гидрированием двойной связи и удалением циклоалифатической гидроксильной группы (1932 г., США) привело к получению анальгетика дезоморфина; он примерно в 10 раз активнее морфина и в 5 раз токсичнее его:

Легко получаемый в кустарных условиях из кодеина, дезоморфин вышел на второе место после героина по частоте применений в России, однако примитивный способ получения и очистки делает его крайне опасным из‑за непредсказуемости эффекта разных по условиям получения примесей. Одно из названий этого наркотика – «крокодил», поскольку даже непродолжительное использование его приводит к огрублению кожи, она становится похожей на кожу крокодила.
Молекула морфина не имеет подвижных структурных элементов, она жёстко фиксирована в виде буквы Т. При более глубоких упрощениях структуры морфина было установлено, что обезболивающий эффект сохраняется до тех пор, пока в молекуле остаётся фрагмент, в котором ароматическое ядро связано с атомом углерода, у которого нет связей с атомом водорода, а к этому атому углерода мостиком из двух атомов углерода присоединена третичная аминогруппа:
 и
и

Эффективность получаемых с соблюдением этого правила веществ заметно возрастает в тех случаях, когда атом азота включен в пипери-диновый цикл и в фенильном остатке находится гидроксильная группа. В качестве примера можно привести петидин, у которого гидрофильный участок молекулы морфина представлен этоксикарбонильной группой:



Переход от этоксикарбонильной группы к пропионилоксигруппе с введением гидроксильной группы в мета-положение увеличивает актив-ность петидина в тридцать раз, однако более доступным и эффективным средством оказался промедол.
Пространственное расположение структурных элементов молекулы может поддерживаться и за счёт электрофильно-нуклеофильных взаимо-действий входящих в её состав атомов. Так, очевидно, что в молекулах метадона и пропоксифена нуклеофильный атом азота и электрофильный атом углерода карбонильной группы создают условия для стабильного расположения этих функциональных групп в непосредственной близости друг от друга, как в цикле:


Метадон Пропоксифен
Из двух оптических изомеров метадона активен только L-изомер, пре-восходящий по анальгетической активности морфин в два раза. Это соеди-нение предполагается использовать для лечения щадящим способом нарко-зависимых больных путем замены героина метадоном с постепенным снижением вводимой в стационарных условиях дозы. Однако индивиду-альный подбор методики лечения очень проблематичен, и часто при этом героиновый наркоман становится метадоновым наркоманом, а лечение метадоновой зависимости даётся ещё труднее, чем лечение героиновой зависимости.
Хорошая иллюстрация влияния пространственного расположения молекулы на анальгетическую активность представлена структурами лев-орфанола и декстрометорфана. Первое из этих соединений – леворфанол – в четыре раза превосходит по анальгетической активности морфин, тогда как второе может быть использовано только для успокоения кашля:

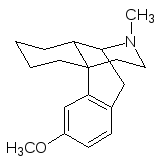
Замена в структуре леворфанола метильной группы у атома азота на аллильную и циклопропилметильную приводит к мощным антагонистам морфина, но они, как и налорфин, являются галлюциногенами.
И всё же опыты по модификации заместителей у атома азота привели к получению эффективных анальгетических препаратов. Одним из них является близкий по свойствам к промедолу просидол. Другое направ-ление поисков привело к получению пентазоцина с диметилаллильным заместителем у атома азота и с гидроксигруппой в фенильном ядре, а также к ещё более эффективному феназоцину.


Просидол Пентазоцин

Феназоцин
Модификация структуры феназоцина с целью получения соединений с остатком пропионовой кислоты, который оказался важным структурным элементом многих опиатных анальгетиков, привела к обнаружению новой группы обезболивающих средств – фентанилов, получивших это название по одному из самых эффективных представителей – фентанилу:

Его эффективная доза (ЕД50) составляет около 0,01 мг/кг при ЛД50 = 3,5 мг/кг. Фентанил отличается очень быстрым наступлением анальгезирующего действия (при внутривенном введении максимальный эффект достигается через 1-3 минуты), при разовом введении обезбо-ливание длится около 30 минут.
При модифицировании структуры фентанила было получено большое количество соединений, отличавшихся от прототипа скоростью наступле-ния анальгетического эффекта, действующей дозой и терапевтической широтой. Все они соответствуют общей формуле

Очень быстрым действием отличается ремифентанил:

Самым безопасным соединением в этой группе считается суфентанил:

У некоторых структурных аналогов фентанила эффективная доза может лежать в пределах от 0,0001 до 0,0007 мг/кг.
Очень сильным опиоидным анальгетиком является соединение, в котором отсутствует пиперидиновый цикл:

Экзоциклическая диметиламинная группа есть в ещё одном обез-боливающем средстве со свойствами опиатных анальгетиков трамадоле (трамале), у которого изомер с экваториальным расположением диметил-аминометильной группы (вторая формула) неактивен:


Трамадол получают из диметиламинометилциклогексанона, образу-ющегося из циклогексанона по реакции Манниха:

Далее на это соединение действуют реактивом Гриньяра, который получают из 3‑броманизола:

В этой реакции образуется, конечно, смесь изомеров, из которой наиболее активное соединение выделяют кристаллизацией.
Несмотря на то, что структура трамадола очень сильно отличается от структуры морфина, она все же соответствует представленным выше минимальным требованиям к опиатным анальгетикам: фенильное ядро соединено с атомом углерода без атомов водорода и третичная амино-группа отделена от этого атома углерода двумя другими атомами углерода. Как обезболивающее средство трамадол слабее морфина, но, тем не менее, его часто используют для купирования послеоперационных болей и для облегчения состояния раковых больных, так как отрицательные побочные эффекты морфина у него выражены гораздо слабее.
Наряду с морфином в опиуме содержатся другие алкалоиды, которые были использованы в качестве исходных продуктов для получения анта-гонистов морфина и опиатных анальгетиков с усложненной по сравнению с морфином структурой. В качестве примера можно привести получение налоксона, используемого для лечения героиновой передозировки. В качестве исходного продукта при этом используют тебаин. Этот алкалоид содержится в опии в количестве около 0,5%, но есть виды мака, в млечном соке которых его гораздо больше. Тебаин токсичен и в отличие от морфии-на не обладает наркотическим действием. Для получения налоксона проводят окисление тебаина пероксидом водорода, полученное кетопро-изводное деметилируют по атому азота действием бромциана, гидроли-зуют образующийся цианамид, алкилируют вторичную аминную группу аллилбромидом и после этого переводят метоксигруппу в гидроксильную группу действием трибромида бора:


Налоксон является «чистым» опиатным антагонистом, т.е. он блокирует эффект морфина по всем видам его активности.
Используя в качестве исходного соединения тебаин, получают также бупренорфин, эффективный в качестве опиатного анальгетика в дозе 0,2 мг (для сравнения: таблетка пентазоцина содержит 50 мг субстанции). При взаимодействии тебаина с трет-бутил-винилметилкарбинолом по реакции Дильса-Альдера получают аддукт, который деметилируют по атому азота по аналогии с предыдущим, алкилируют образовавшийся вторичный амин циклопропилметилбромидом, переводят связанную с ароматическим ядром метоксигруппу в гидроксигруппу и гидрируют двойную связь. Бупренорфин имеет следующее строение:

По интенсивности связывания с выделенным из ткани мозга опиат-ным рецептором бупренорфин превосходит морфин примерно в 20 раз, тогда как по анальгетической активности он лучше его в несколько тысяч раз. Это расхождение легко объясняется повышенной липофильностью бупренорфина по сравнению с морфином, что обеспечивает ему более легкое прохождение гематоэнцефалического барьера. Различие в липо-фильности лежит также в основе более сильного обезболивающего и наркотического эффекта героина, который представляет собой диацетиль-ное производное морфина. В виде диэфира это вещество проходит через гематоэнцефалический барьер и деацетилируется в глиальных клетках, создавая в головном мозге значительно более высокую концентрацию активного аналога морфина – 6‑ацетилморфина.
Пример фентанила показывает насколько далеко различаются иногда строение прототипа и модифицированной в результате многочисленных проб и ошибок структуры с аналогичным механизмом действия. После того, как была показана роль пиперидинового цикла в проявлении анальге-тической активности, были проведены многочисленные опыты по синтезу различных замещённых пиперидинов, увенчавшиеся разработкой несколь-ких препаратов, сохраняющих значение до настоящего времени, и препа-ратов, которые очень скоро пришлось запретить. В этой связи нельзя не назвать препарат фенциклидин (сернил, РСР), который был получен в 1954 году и после непродолжительных клинических испытаний внедрен в фар-макологическую практику в качестве внутривенного анестетика (он будет рассмотрен в разделе, относящемся к психотическим средствам, стр. 90).
При изучении механизма действия алкалоидов мака было установ-лено, что они являются агонистами эндогенных веществ пептидной приро-ды, выполняющих функции нейромедиаторов и нейрогормонов. В работе мозга участвуют около 15 таких олиго- и полипептидов, но они продуци-руются и многими другими клетками организма теплокровных. В част-ности, клетки слизистой оболочки желудка также генерируют значитель-ные количества одного из главных представителей эндогенных веществ этой группы – Мет-энкефалина. Чаще всего структура Мет-энкефалина включена в более крупные пептидные молекулы (динорфины, эндорфины) и в нужное время он выделяется из этих пептидов в результате их гидро-лиза высокоизбирательными ферментами. Роль пептидов с морфиноподоб-ным действием многогранна, и полной картины, отражающей все особен-ности этих регуляторов высшей нервной деятельности, пока не сущест-вует. В то же время можно предполагать, что они предназначены для модуляции болевого сигнала (их действие противоположно эффекту усиливающих болевой сигнал простагландинов), кроме того, они являются нейромедиаторами внутреннего подкрепления, например, ими опосредо-вано чувство удовлетворения от вкусного и сытного обеда, радости от добрых дел, счастья; выброс большого количества этих пептидов вызывает эйфорию (как и приём опиатных наркотиков).
Известны два пентапептидных энкефалина: Тир-Гли-Гли-Фен-Мет (Мет-энкефалин) и менее активный Лей-энкефалин, у которого С-концевая гидрофобная аминокислота представлена лейцином. Большая и гибкая молекула энкефалина очень сильно отличается от молекулы морфина, особенно когда её представляют без учёта пространственного расположения функциональных групп в пептидной молекуле:
 и
и
 или
или

В то же время видно, что у этих двух молекул есть общий структур-ный элемент – гидроксифенильная группа, отделённая от аминогруппы двумя атомами углерода (это характерно для подавляющего большинства нейромедиаторов). С помощью морфина с радиоактивной меткой были выделены рецепторные гликопротеины, с которыми он связывается в проч-ный комплекс, а изучение их естественных лигандов привело к открытию опиоидных пептидов. При связывании с этими лигандами происходит структурная перестройка рецепторов, приводящая к блокировке калиевых каналов (мю‑рецептор), кальциевых каналов (каппа-рецептор) и аденилат-циклазы (дельта‑рецептор). То есть этими веществами может быть одно-временно заблокирована проводимость сигнала на уровне аксона, на уровне высвобождения нейромедиатора возбуждения и на метаболи-ческом уровне.
Как отмечалось выше, опиаты, как лекарственные средства, отмечены целым рядом недостатков. Они не могут быть использованы для снятия хронических болей, так как их поступление в организм в течение продол-жительного времени приводит к болезненному пристрастию и к привы-канию. В основе этого явления лежит обычный отклик живой природы на избыток какого-либо регулятора: появление в организме морфина или его аналогов соответствует появлению избыточного количества естественного лиганда (в данном случае энкефалина). Следствием этого становится прекращение биосинтеза энкефалина, эндорфинов и динорфинов, и тогда для достижения того же эффекта, что и от первых доз, отсутствующий энкефалин должен заменяться дополнительным количеством опиатного анальгетика. Кроме того, в присутствии синтетических аналогов энкефа-лина блокируется участвующий в биоэнергетических процессах фермент аденилатциклаза (дельта‑рецептор) и в клетках прекращается биосинтез циклического аденозинмонофосфата и связанное с этим уменьшение выработки аденозинтрифосфата. Клетки организма отвечают на это биосинтезом новых молекул аденилатциклазы. Увеличенное содержание в клетках аденилатциклазы также нуждается в повышенной дозе её блокатора, и так идёт постепенное наращивание дозы наркотика и содержания фермента в клетках. При отказе от приёма наркотического вещества происходит высвобождение активной аденилатциклазы в количествах, которые значительно превышают её нормальное содержание. В клетках образуется слишком много цАМФ и АТФ (оба эти вещества алгогены), а избыток источника химической энергии АТФ приводит к непроизвольным сокращениям мышц, повышенной двигательной актив-ности, а в серьёзных случаях и к судорогам, которые сопровождаются сильнейшими болями во всем теле (это и есть синдром абстиненции или так называемая «ломка» наркоманов).
Кроме того, обусловленное присутствием наркотика снижение нор-мального уровня эндорфинов вплоть до полного прекращения их босин-теза, а эти вещества, как отмечалось выше, являются нейромедиаторами внутреннего подкрепления, чувства радости от хороших дел, счастья, создает у прекратившего прием наркотика человека постоянное ощущение неудовлетворённости – никакие дела и события не приносят удовольствия, раздражает всё. Очень остро воспринимаются болевые ощущения, даже прикосновения одежды, складки простыни вызывают неприятные ощуще-ния. Такое состояние может длиться годами, поскольку исчезают фермент-ные системы для биосинтеза эндорфинов и разлаживается механизм регуляции уровня этих нейрогормонов. У прекративших приём опиатов наркоманов естественный уровень энкефалина никогда уже не выходит на прежнее значение. Чаще всего человек не выдерживает этого и снова прибегает к наркотикам для того, чтобы почувствовать хотя бы иллюзию радости жизни.
Нельзя не отметить и серьёзные изменения в психике, в нравственных установках наркоманов и даже тех, кто всего лишь несколько раз попро-бовал тяжёлые наркотики. Эти люди теряют способность к сопережива-нию, они становятся несоциальными. По сути дела именно тяжёлые нарко-тики проще всего использовать для того, чтобы выведывать секретные сведения у их носителей, поскольку хранить тайну могут только высоко-нравственные люди. Деградация личности в конце концов приводит к полному отключению от нормального образа жизни и к преждевременной смерти от передозировки или от болезней, полученных от уколов зараженными шприцами.
После обнаружения естественных лигандов опиатных рецепторов казалось, что проблему избирательных анальгетиков, действующих на уровне центральной нервной системы, можно будет легко решить. Стоит только найти их пептидные аналоги, которые устойчивы к действию гид-ролаз, и будут получены совершенные обезболивающие средства. Важно отметить, что такие вещества образуются и в естественных процессах. Так, например, при ферментативном гидролизе содержащегося в коровьем молоке казеина образуются сравнительно устойчивые к действию пептидаз фрагменты этого белка со свойствами опиатных анальгетиков: ‑казомор-фин-5 (Тир-Про-Фен-Про-Гли) и -казоморфин-7 (Тир-Про-Фен-Про-Гли-Про-Иле). Материнское молоко содержит казеин другого аминокислотного состава, из которого образуется активный гептапептид Тир-Про-Фен-Вал-Глу-Про-Иле. Их поступление из кишечника в кровь объясняет мягкий успокаивающий и снотворный эффект молока, который особенно хорошо проявляется у детей. В детском возрасте желудочно-кишечный тракт достаточно легко ассимилирует олигопептиды. Это заложено в природе, поскольку именно через такие пептиды формируется врожденный иммунитет и регулируется высшая нервная деятельность ребенка. Аналогичный энкефалину гептапептид материнского молока на ранней стадии развития детского организма играет важную роль в формировании характера и умственных способностей ребенка. Входящий в состав казоморфинов С‑концевой фрагмент Про-Гли-Про хорошо защи-щает небольшие пептиды от действия пептидаз. Это было использовано, например, при разработке нового лекарственного средства «Семакс». Было известно, что аминокислотная последовательность 4-7 в гипофизарном адренокортикотропном гормоне (АКТГ, 39 аминокислотных фрагментов) оказывает очень хороший стимулирующий эффект на высшую нервную деятельность. Этот тетрапептид с биохимической формулой Мет-Глу-Гис-Фен улучшает восприятие, обучаемость, стимулирует работу головного мозга, но его действие слишком непродолжительно из-за гидролиза протеазами (период полупревращения составляет около 1,5 минут). Аналогичными свойствами обладает и более длинный фрагмент АКТГ, представляющий собой гептапептид 4-10. Исходя из этого, можно было предположить, что дополнение тетрапептида с С-конца фрагментом Про-Гли-Про сохранит его биологическую активность и в то же время сделает его более устойчивым к ферментативному гидролизу. Детальное изучение терапевтического эффекта синтетического гептапептида Мет-Глу-Гис-Фен-Про-Гли-Про, получившего название семакс, подтвердило эти предположения и показало, что он может приниматься здоровыми людьми для улучшения высшей нервной деятельности. Прием этого лекарства (капли в нос, чтобы не травмировать сосуды инъекциями или не подвер-гать пептид действию ферментов пищеварительной системы) значительно улучшает состояние больных с нарушениями функций головного мозга, например, после инсульта или при паркинсонизме. Отмечено также благоприятное влияние семакса на течение некоторых глазных болезней.
Подобный способ модификации молекулы можно было применить и для стабилизации структуры энкефалина, но в этом случае был исполь-зован более распространенный в химии пептидов подход, основанный на замене L-аминокислот с небольшими радикалами их D-изомерами, а также на замене фрагмента фенилаланина его тиенильным аналогом и на введе-нии аминоизомасляной кислоты вместо аланина или других аминокислот. Такое незначительное изменение структурных элементов может оказаться незначимым для соответствующего рецептора, но протеазы, гидролизую-щие только пептидные связи, которые построены из белковых L-амино-кислот, не катализируют гидролиз пептидных связей с небелковыми аминокислотами. В случае энкефалина можно было использовать замену глициновых фрагментов на D-аланиновые. Были, конечно, проведены и другие модификации структуры энкефалина, которые можно представить в следующем виде:

На схеме показаны изменения структуры и их влияние на активность в сравнении с исходной молекулой. Чаще всего биологическая активность измененного пептида снижалась, но в других вариантах были получены соединения, которые сохраняли присущую энкефалину активность и были значительно более устойчивы к биотрансформации. При этом оказалось, что использование таких стабильных пептидов в качестве лекарственных средств не дает никаких преимуществ, поскольку им присущи все недостатки морфина. Это означает, что морфин является настоящим пептидомиметиком, то есть веществом, которое повторяет все свойства соответствующего нейропептида.
Обезболивающее средство было получено при ином подходе к вмешательству в функционирование энкефалина. По аналогии с другими блокаторами пептидаз, в частности, по аналогии с используемыми для лечения гипертонии блокаторами ангиотензинконвертирующего фермента (каптоприл, эналаприл), был получен тиорфан:


Каптоприл Тиорфан
Тиорфан блокирует фермент энкефалиназу, предназначенную для раз-ложения выполнившего медиаторную функцию энкефалина и его избытка. Такие подобные пептидам соединения занимают в каталитическом центре пептидаз место естественного субстрата, прочно связываются за счёт сульфгидрильной группы с участвующим в работе каталитического центра ионом цинка (кофактор) и это приводит к ингибированию фермента:

Здесь представлен возможный вариант соответствия строения ак-тивного центра энкефалиназы структуре энкефалина с участками связыва-ния карбонильной группы второй молекулы глицина с принимающим участие в работе гидролаз ионом цинка, с гидролизуемым участком в пептидной цепочке, с центром узнавания последней пептидной связи и с катионоидным участком для связывания карбоксилатной группы. В моле-куле тиорфана есть бензильная группа, пептидная связь и карбоксилатная группа, но место гидролизующейся пептидной связи -СO-NH- между второй молекулой глицина и остатком фенилаланина занимает группа HS‑CH2-, образующая прочную связь с ином цинка, что и приводит к блокировке фермента.
Тиорфан является эффективным обезболивающим средством, которое повышает концентрацию энкефалина только там, где он образуется для регуляции интенсивности болевого сигнала. Поэтому он не вызывает болезненного пристрастия и его действие не сопровождается состоянием эйфории, блокировкой аденилатциклазы и другими побочными эффек-тами, возникающими при приёме морфина или его структурных аналогов в результате их распределения по всему организму. Это вещество уже посту-пает в продажу под торговыми марками гидрасек и рацекадотрил. В част-ности, его, как и опий, можно использовать для лечения острой диареи.
Ещё один способ обезболивания основан на использовании структур-ных аналогов производных жирных кислот нейролипинов, которые также вовлечены в регуляцию интенсивности болевых сигналов. Эти вещества были обнаружены при изучении биологической активности капсаицина (активного вещества жгучего перца):

Рецепторы на капсаицин, называемые ванилоидными или капсаици-новыми, расположены в спинном мозге вместе с каннабиноидными рецепторами, реагирующими на тетрагидроканнабинол (см. стр. 86), действующее начало гашиша (из растений конопли). Эндогенные произ-водные жирных кислот, участвующие в работе нервной системы, представлены, амидами и эфирами жирных кислот, например:

Олеамид

Виродамин

2-Арахидонилглицерин

Анандамид

Арахидонилдофамин
Среди ацилированных липофильными кислотами нейромедиаторов самым активным веществом, относящимся к нейролипинам, является дофамид ретиноловой кислоты:

Анандамид (от санскритского слова ананда – блаженство) является важным противовоспалительным и противораковым средством, он действует на сердечнососудистую систему, вызывая снижение кровяного давления и сокращение частоты сердечных сокращений. В дополнение к этому он является анаболическим регулятором, повышающим аппетит, стимулирующим образование жировой ткани и снижающим потребление энергии. Он также участвует в регуляции температуры тела, двигательной активности и таких состояний психики, как тревога и беспокойство. Показана также способность анандамида связываться с некоторыми другими рецепторами. Предполагается, что изменение уровня анандамида может быть использовано для лечения воспалительных заболеваний кишечника и рака прямой кишки. Анандамид присутствует в жидких средах мужской и женской репродуктивных систем. Анандамид и его структурный аналог 2-арахидонилглицерин содержатся в бобах какао.
N-Олеилэтаноламин является, очевидно, сигнализатором насыщения. Внутрибрюшинное и даже пероральное введение этого вещества крысам лишает их аппетита.
В спинномозговой жидкости крыс, которых искусственно лишали сна, был обнаружен амид олеиновой кислоты. Олеамид вызывает физиоло-гический сон при введении в мозг крысы. В спинномозговой жидкости присутствуют и другие амиды жирных кислот, но такую активность демонстрирует только олеамид. В дополнение к этому олеамид проявляет и другие виды неврологической активности, в частности, он принимает участие в формировании памяти и в восприятии боли, снижает темпе-ратуру тела и понижает двигательную активность, а также связывается с другими типами рецепторов.
Было также обнаружено, что эндогенная компонента нервной ткани млекопитающих содержит N-арахидонилдофамин, проявляющий опреде-лённые регуляторные свойства. Так, например, N-арахидонилдофамин взаимодействует с ванилоидными рецепторами первого типа по аналогии с близким по строению капсаицином. Он взаимодействует также с каннаби-ноидными рецепторами, т.е. его агонистом является тетрагидроканнаби-нол. Такие же свойства показывает N-олеилдофамин, тогда как N‑пальми-тоилдофамин и N-стеароилдофамин с этими рецепторами не взаимодейст-вуют. Правда, полная картина всех возможных регуляторных механизмов с участием нейролипинов пока не получена.
Исследования по поиску обезболивающих средств в области нейроли-пинов связаны с тем, что болевое ощущение может возникать и от термо-рецепторов, предназначенных для передачи в центральную нервную систему информации о действии на них тепла или холода. Очевидно, что от одного типа терморецепторов организм не может получить полную информацию обо всем диапазоне температур от очень холодной до очень горячей, приводящей к разрушению клеток.
Так, например, есть по крайней мере два рецептора, реагирующих на пониженную температуру. Первый тип рецепторов управляет ионным каналом, который открывается для прохода ионов кальция и натрия в ответ на падение температуры ниже 28С. Он реагирует также на ментол, который создает ощущение прохлады на коже и во рту:

Второй тип рецепторов сигнализирует об охлаждении ниже 18С. Когда количество сигналов от этого рецептора преодолевает определённое пороговое значение, центральная нервная система отвечает на это генерированием болевого ощущения. Более глубокое охлаждение, включая обморожение, приводит к гибели клеток и тогда болевое ощущение возни-кает уже по обычной для таких состояний схеме с выделением эндогенных алгогенов и усилителей болевого сигнала из мембран и внутренних сред разрушенных клеток.
Выявлено четыре типа рецепторов, предназначенных для сигнализа-ции о тепловом воздействии. Первые два реагируют на умеренные темпе-ратуры (25С и 31С). Третий тип рецепторов при температуре более 43С создает ощущение жжения. Кроме термических факторов, срабатыва-ние этих рецепторов могут вызвать и некоторые химические соединения, самыми известными из которых являются капсаицин, камфора и кислоты (протоны). Агонистом третьего типа рецепторов является также получен-ное путём оптимизации структуры капсаицина синтетическое соединение, представляющее собой морфолид пелларгоновой кислоты:

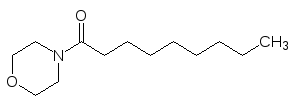
Камфора Морфолид пелларгоновой кислоты
Мофолид пелларгоновой кислоты используют в согревающих мазях. Раздражение реагирующих на тепло рецепторов приводит к расширению сосудов (избыточное тепло надо отводить), но при отсутствии реального источника тепла это создает согревающий эффект.
Четвертый тип рецепторов, реагирующих на термическое воздейст-вие, включается при температуре более 52С, когда уже идет коагуляция белков. Его сигнал воспринимается как боль.
При парентеральном введении капсаицина он вызывает у подопытных животных сильный болевой эффект, после которого наступает длительное обезболивание. Инъекции капсаицина новорожденным мышатам делают их нечувствительными к боли на всю жизнь. Модификация структуры капсаицина с целью лишения его способности вызывать первичный болевой эффект привела к ванилиламиду олеиновой кислоты:

Сообщения об опытах по изучению этого вещества в качестве внутривенного средства для обезболивания появлялись в литературе, но соответствующего лекарственного средства пока нет.
