
- •Глава VI. Атом
- •§ 6.1. Развитие представлений о строении атома
- •§ 6.2. Спектры испускания и поглощения атомов. Формула Бальмера
- •§ 6.3. Модель атома Бора
- •§ 6.4. Волновая модель атома
- •§ 6.5. Многоэлектронные атомы
- •§ 6.6. Лазер
- •Глава VII. Ядро атома
- •§ 7.1. Характеристики ядра атома: состав, размер, стабильность
- •§ 7.2. Энергия связи ядра атома
- •§ 7.3. Радиоактивность. Закон радиоактивного распада
- •§ 7.4. Виды радиоактивного распада
- •§ 7.5. Ядерные реакции
§ 6.4. Волновая модель атома
Д
 вижение
электрона в атоме трехмерное, так что
его волновая функция зависит от трех
координат: =(х,y,z)
и является решением трехмерного уравнение
Шредингера. Энергия кулоновского
взаимодействия электрона с ядром атома
водорода зависит только от расстояния
между ними и выражается следующей
потенциальной функцией:
вижение
электрона в атоме трехмерное, так что
его волновая функция зависит от трех
координат: =(х,y,z)
и является решением трехмерного уравнение
Шредингера. Энергия кулоновского
взаимодействия электрона с ядром атома
водорода зависит только от расстояния
между ними и выражается следующей
потенциальной функцией:
![]() (см. предыдущий параграф). Эта функция
является сферически симметричной, так
что целесообразно решать УШ в сферической
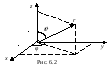
системе координат (рис. 6.2). Формулы
перехода от декартовых координат {x,y,z}
к сферическим координатам {r,,φ}таковы:
(см. предыдущий параграф). Эта функция
является сферически симметричной, так
что целесообразно решать УШ в сферической
системе координат (рис. 6.2). Формулы
перехода от декартовых координат {x,y,z}
к сферическим координатам {r,,φ}таковы:
x= rsincosφ, y= rsinsinφ, z= rcos.
В сферических координатах трехмерная волновая функция превращается в произведение трех одномерных функций, каждая из которых зависит от одной сферической координаты:
(r,,φ)=R(r)()(φ), и трехмерное уравнение Шредингера превращается в три одномерных уравнения. Их решение дает три квантовых числа, каждое из которых определяет собственные функции этих уравнений, т.е. состояние микрочастицы. Рассмотрим названия, численные значения и физический смысл этих чисел.
n
– главное квантовое число,
n=1,2,3,
...
Оно определяет значения собственных
энергий электрона в атоме водорода,
которые совпадают со значениями уровней
энергии в модели Бора (формула 6.4):
![]() .
Таким образом, физический
смысл главного квантового числа –
квантование энергии.
.
Таким образом, физический
смысл главного квантового числа –
квантование энергии.
l
– азимутальное или орбитальное квантовое
число. Оно
связано с главным квантовым числом и
для одного и того же n
может
принимать n
целочисленных значений от 0 до (l-1).
Это квантовое число определяет орбитальный
момент импульса электрона: L=![]() . Таким образом, физический
смысл азимутального квантового числа
– квантование момента импульса.
. Таким образом, физический
смысл азимутального квантового числа
– квантование момента импульса.
m
– магнитное квантовое число.
Оно связано с азимутальным числом и для
одного и того же l
принимает
все целочисленные значения от (-
l)
до (+l),
включая ноль, т.е. всего (2l+1)
значений. Оказывается, что квантуется
не только момент импульса, но его проекция
на ось, направление которой физически
задано, например, направление внешнего
магнитного поля. Обозначим эту ось z,
тогда Lz=![]() .
Таким образом, физический
смысл магнитного квантового числа –
квантование проекции момента импульса
на физически заданное направление.
.
Таким образом, физический
смысл магнитного квантового числа –
квантование проекции момента импульса
на физически заданное направление.
Волновая функция
электрона в атоме водорода, как следует
из уравнения Шредингера, зависит от
трех квантовых чисел: =nlm,
тогда как его энергия зависит только
от n.
Наименьший уровень энергии n=1
называется основным, ему соответствует
только одно состояние. Всем остальным
уровням энергии (они называются
возбужденными) соответствует несколько
разных состояний. Такие уровни называется
вырожденным, а соответствующее им число
разных состояний (т.е. разных волновых
функций) называют кратностью вырождения
уровня. Кратность вырождения равна
![]() .
.
В квантовой механике, учитывающей волновые свойства электрона, понятие электронной орбиты теряет смысл. Электрон при движении в атоме представляет собой электронное облако, плотность которого пропорциональна nlm 2. Квантовые числа n и l определяют размеры и форму электронного облака, квантовое число m определяет его ориентацию в пространстве. Для состояний с l=0 для разных главных квантовых чисел n волновая функция сферически симметричная, и максимальная плотность электронного облака соответствует орбитам электрона в модели атома Бора с теми же номерами n.
Волновая модель атома водорода, как и модель Бора, выводит формулу Бальмера для спектра атома водорода. Это совпадение с опытом является экспериментальным подтверждением квантования энергии, задаваемым главным квантовым числом n. Квантование момента импульса и его проекции также подтверждается опытом. Квантовая теория формулирует определенные правила отбора: разрешены только такие переходы между уровнями энергии, когда изменяется не только n, но и l: Δl=±1. Например, при n=2 и l=1 магнитное квантовое число может иметь три разных значения: m= -1, 0, 1, т.е. в трех разных состояниях электрон имеет одинаковую энергию. Это значит, что разные атомы, каждый из которых находился в одном из рассматриваемых состояний, при переходе в основное состояние испустят одинаковые фотоны, дающие одну спектральную линию. Иная получится картина, если атомы поместить во внешнее магнитное поле. Уровень энергии расщепляется на три близких подуровня для трех разных значений m. О таком говорят, что вырождение уровня снимается. Рассмотрим механизм снятия вырождения уровня энергии. Магнитное квантовое число связано с моментом импульса электрона. Вспомним его классическое определение: L=mυr – электрон движется по окружности, и это движение заряженной частицы можно рассматривать как круговой ток, характеризуемый вектором магнитного момента. Контур с током ведет себя в магнитном поле как магнитная стрелка: при ориентации магнитной стрелки по полю ее энергия минимальна (положение устойчивого равновесия), при ориентации против магнитного поля ее энергия максимальна, всем прочим промежуточным положениям соответствуют промежуточные значения энергии. С орбитальным механическим моментом электрона жестко связан его орбитальный магнитный момент, причем, их векторы направлены противоположно. Квантование Lz физически означает, что проекции орбитального механического и магнитного моментов электрона на направление внешнего магнитного поля могут иметь три разных значения, и трем разным волновым функциям с n=2 и l=1 соответствуют три разных значения энергии. Такие три атома будут испускать при переходе в основное состояние три разных кванта энергии, и в спектре излучения вместо трех одинаковых спектральных линий появятся три разных пространственно разделенных линии. Расщепление в магнитном поле соответствующей спектральной линии на (2l+1) близких линий экспериментально было обнаружено еще в конце XIX в. и называется эффектом Зеемана. Такой эффект есть проявление орбитального l и магнитного m квантовых чисел.
Таким образом, волновая модель атома водорода подтверждается опытом, и состояние электрона в атоме водорода однозначно определяют три квантовых числа: n, l и m.
Позднее эксперименты
обнаружили, что даже без внешнего
магнитного поля некоторые спектральные
линии являются двойными (дублетами),
что свидетельствует об еще одном
квантовом числе, которое может принимать
два значения. Его существование было
также подтверждено в опытах Штерна и
Герлаха, где пучок атомов серебра
(одновалентного металла) направлялся
на фотопластинку через область
неоднородного магнитного поля, и на
пластинке следы электронов давали две
четко разделенные полосы. Они
свидетельствовали о том, что кроме
орбитального магнитного момента у
электрона имеется еще какой-то магнитный
момент. Его назвали спиновым магнитным
моментом, а связанный с ним собственный
механический момент назвали спином
Ls.
Соответствующее
ему квантовое число получило название
спинового квантового числа s.
Оно может принимать два значения: s=±![]() .
.
Смена времен года вызвана вращением Земли вокруг Солнца, с этим движением связан орбитальный механический момент; с вращением Земли вокруг собственной оси связан ее собственный механический момент. Классическая модель электрона, имеющего вид шарика, в микромире не имеет смысла. Спин – сугубо квантовая характеристика микрочастицы, не имеющая аналога в классической физике. Спин электрона – это некоторая его индивидуальная характеристика, как, например, заряд.
Представление о спине и спиновом квантовом числе, возникшее из экспериментов, позднее было получено теоретически из квантового релятивистского уравнения движения, носящего имя Дирака.
Таким образом, полное описание состояния электрона в атоме дают четыре квантовых числа: n, l, m и s. Каждое из них связано с квантующейся физической величиной: энергией, орбитальным и собственным моментом импульса электрона, и их квантование подтверждает опыт.
