
- •Глава VI. Атом
- •§ 6.1. Развитие представлений о строении атома
- •§ 6.2. Спектры испускания и поглощения атомов. Формула Бальмера
- •§ 6.3. Модель атома Бора
- •§ 6.4. Волновая модель атома
- •§ 6.5. Многоэлектронные атомы
- •§ 6.6. Лазер
- •Глава VII. Ядро атома
- •§ 7.1. Характеристики ядра атома: состав, размер, стабильность
- •§ 7.2. Энергия связи ядра атома
- •§ 7.3. Радиоактивность. Закон радиоактивного распада
- •§ 7.4. Виды радиоактивного распада
- •§ 7.5. Ядерные реакции
Глава VII. Ядро атома
§ 7.1. Характеристики ядра атома: состав, размер, стабильность
Согласно современным
представлениям, ядра
разных атомов являются системой квантовых
частиц - нуклонов.
Нуклоны бывают в двух состояниях, т.е.
ядро состоит из частиц двух видов:
протонов-p
и нейтронов-n.
Протон имеет
положительный заряд, равный заряду
электрона, нейтрон – электрически
нейтральная частица. Массы этих частиц
очень мало отличаются друг от друга.
Масса нуклона превышает массу электрона
почти в 1840 раз, так что вся масса атома
практически сосредоточена в его ядре.
В ядерной физике массу измеряют в атомных
единицах массы (а.е.м.), энергию в
мегаэлектронвольтах (МэВ). 1 а.е.м.≈1,66.10-27
кг, она составляет 1/12 часть массы изотопа
углерода
![]() ,
1 МэВ=1,6.10-13
Дж. Согласно
уравнению Эйнштейна E=mc2
масса
и энергия эквивалентны друг другу,
поэтому нередко в ядерной физике массу
указывают в единицах энергии.
Коэффициент
пропорциональности между массой и
энергией - квадрат скорости света в
вакууме c2=9.1016
Дж/кг=931
МэВ/а.е.м. Масса покоя протона mр=1,0076
а.е.м., масса покоя нейтрона mп=1,008665 а.е.м
, масса покоя электрона me=0,00055
а.е.м.
или mр=938,28 МэВ,
mп=939,57
Мэв,
me=0,
51 МэВ.
Протоны и нейтроны, так же как и электроны,
имеют полуцелый спин: s=±
,
1 МэВ=1,6.10-13
Дж. Согласно
уравнению Эйнштейна E=mc2
масса
и энергия эквивалентны друг другу,
поэтому нередко в ядерной физике массу
указывают в единицах энергии.
Коэффициент
пропорциональности между массой и
энергией - квадрат скорости света в
вакууме c2=9.1016
Дж/кг=931
МэВ/а.е.м. Масса покоя протона mр=1,0076
а.е.м., масса покоя нейтрона mп=1,008665 а.е.м
, масса покоя электрона me=0,00055
а.е.м.
или mр=938,28 МэВ,
mп=939,57
Мэв,
me=0,
51 МэВ.
Протоны и нейтроны, так же как и электроны,
имеют полуцелый спин: s=±![]() .
.
О
Рис.7.1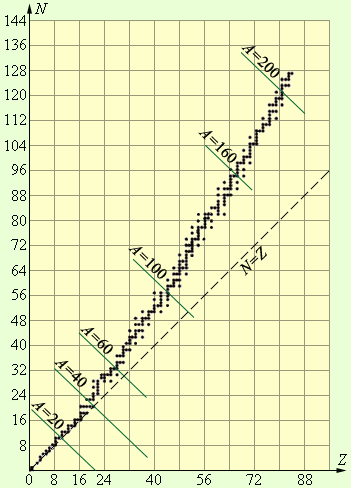
![]() .
Число протонов равно Z,
число нейтронов равно N=A-Z,
и общее число нуклонов равно A.
Атомы одного и того же элемента имеют
одинаковые Z,
т.е. одинаковое число протонов в ядре,
а вот A
у них может быть различным.
Такие атомы называют изотопами
и иногда им даже присваивают разные
обозначения и разные названия. Примером
являются три изотопа водорода,
встречающиеся в природе:
.
Число протонов равно Z,
число нейтронов равно N=A-Z,
и общее число нуклонов равно A.
Атомы одного и того же элемента имеют
одинаковые Z,
т.е. одинаковое число протонов в ядре,
а вот A
у них может быть различным.
Такие атомы называют изотопами
и иногда им даже присваивают разные
обозначения и разные названия. Примером
являются три изотопа водорода,
встречающиеся в природе:
![]() -
протий,
-
протий,
![]() -
дейтерий,
-
дейтерий,
![]() - тритий. У разных изотопов различное
число нейтронов в ядре атома. Некоторые
элементы имеют множество изотопов. Это
приводит к тому, что у некоторых элементов
в таблице Менделеева массовые числа
заметно отличаются от целых: они указывают
массу атома, усредненную по его природному
изотопному составу. Разные комбинации
A
и N
соответствуют более 1500
известным ядрам, тогда как химических
элементов немного более сотни. Стабильными
являются только элементы с порядковыми
номерами Z<83,
остальные нестабильны, а некоторые из
них могут быть получены только
искусственно. Из известных ядер
устойчивыми являются около 20 %, остальные
распадаются вследствие радиоактивности.
На рис. 7.1 приведена так называемая
дорожка стабильности,
где маленькими квадратиками, некоторые
из которых сливаются друг с другом,
указаны стабильные и долгоживущие ядра.
В не слишком тяжелых ядрах, для которых
A<40,
число протонов равно числу нейтронов.
У более тяжелых ядер
число нейтронов превышает число протонов
тем заметнее, чем массивнее ядро.
Гравитационное притяжение нуклонов в
ядре пренебрежимо мало по сравнению с
кулоновским отталкиванием протонов.
Стабильность ядра обеспечивают мощные
ядерные силы, радиус действия которых
порядка 10-15
м. Ядерные силы действуют только между
ближайшими друг к другу нуклонами.
Поэтому по мере увеличения числа протонов
все больше нейтронов необходимо для
«склеивания» нуклонов, но вследствие
малого радиуса действия ядерных сил
тяжелые ядра становятся нестабильными,
а их максимальная масса ограничена.
- тритий. У разных изотопов различное
число нейтронов в ядре атома. Некоторые
элементы имеют множество изотопов. Это
приводит к тому, что у некоторых элементов
в таблице Менделеева массовые числа
заметно отличаются от целых: они указывают
массу атома, усредненную по его природному
изотопному составу. Разные комбинации
A
и N
соответствуют более 1500
известным ядрам, тогда как химических
элементов немного более сотни. Стабильными
являются только элементы с порядковыми
номерами Z<83,
остальные нестабильны, а некоторые из
них могут быть получены только
искусственно. Из известных ядер
устойчивыми являются около 20 %, остальные
распадаются вследствие радиоактивности.
На рис. 7.1 приведена так называемая
дорожка стабильности,
где маленькими квадратиками, некоторые
из которых сливаются друг с другом,
указаны стабильные и долгоживущие ядра.
В не слишком тяжелых ядрах, для которых
A<40,
число протонов равно числу нейтронов.
У более тяжелых ядер
число нейтронов превышает число протонов
тем заметнее, чем массивнее ядро.
Гравитационное притяжение нуклонов в
ядре пренебрежимо мало по сравнению с
кулоновским отталкиванием протонов.
Стабильность ядра обеспечивают мощные
ядерные силы, радиус действия которых
порядка 10-15
м. Ядерные силы действуют только между
ближайшими друг к другу нуклонами.
Поэтому по мере увеличения числа протонов
все больше нейтронов необходимо для
«склеивания» нуклонов, но вследствие
малого радиуса действия ядерных сил
тяжелые ядра становятся нестабильными,
а их максимальная масса ограничена.
Ядро, как и всякая
квантовая частица, не имеет строго
определенных размеров. Объем ядра
пропорционален числу нуклонов А,
а его размер (радиус 2)
rя≈10-15
![]() м.
Плотность равна отношению массы к
объему, а так как обе эти величины
пропорциональны числу нуклонов в ядре,
то плотность различных ядер одинакова
и равна примерно 1017
кг/м3.
м.
Плотность равна отношению массы к
объему, а так как обе эти величины
пропорциональны числу нуклонов в ядре,
то плотность различных ядер одинакова
и равна примерно 1017
кг/м3.
