
- •ПРЕДИСЛОВИЕ
- •ВВЕДЕНИЕ
- •РАЗДЕЛ I. ФИЗИКО-ХИМИЧЕСКИЕ ОСНОВЫ ГОРЕНИЯ
- •ГЛАВА 1. ГОРЕНИЕ – ОСНОВНОЙ ПРОЦЕСС НА ПОЖАРЕ
- •1.1. Определение горения
- •1.2. Характеристика участников процесса горения
- •1.4. Опасные факторы пожара
- •ГЛАВА 2. МАТЕРИАЛЬНЫЙ БАЛАНС ПРОЦЕССОВ ГОРЕНИЯ
- •2.1. Расчет объема воздуха, необходимого для горения
- •2.1.1. Горючее – индивидуальное химическое соединение
- •2.1.2. Горючее – смесь газов и паров
- •2.2.1. Горючее – индивидуальное химическое соединение
- •2.2.2. Горючее – смесь газов и паров
- •2.2.3. Горючее – сложное вещество с известным элементным составом
- •2.3. Продукты сгорания. Дым и его характеристики
- •ГЛАВА 3. ТЕПЛОВОЙ БАЛАНС ПРОЦЕССОВ ГОРЕНИЯ
- •3.1. Уравнение теплового баланса процесса горения
- •3.3. Расчет температуры горения
- •РАЗДЕЛ II. ТЕОРИИ ГОРЕНИЯ
- •4.1. Тепловая теория горения
- •4.1.1. Механизм химических реакций при горении
- •4.1.2. Факторы, влияющие на скорость реакций горения
- •4.2. Цепная теория горения
- •4.3. Диффузионная теория горения
- •ГЛАВА 5. ПЛАМЯ И ЕГО РАСПРОСТРАНЕНИЕ В ПРОСТРАНСТВЕ
- •5.1. Виды пламени
- •5.2. Структура пламени
- •5.3. Процессы, протекающие в пламени
- •5.4. Скорость распространения пламени
- •5.5. Характер свечения пламени
- •IV.I. ВОЗНИКНОВЕНИЕ ГОРЕНИЯ
- •ГЛАВА 6. САМОВОСПЛАМЕНЕНИЕ
- •ГЛАВА 7. САМОВОЗГОРАНИЕ
- •7.1. Механизм процесса самовозгорания веществ
- •7.2. Самовозгорание жиров и масел
- •7.3. Самовозгорание химических веществ
- •ГЛАВА 8. ВЫНУЖДЕННОЕ ВОСПЛАМЕНЕНИЕ (ЗАЖИГАНИЕ)
- •8.2. Закономерности перехода самовоспламенения к зажиганию
- •8.3. Зажигание нагретым телом
- •8.4. Элементы тепловой теории зажигания
- •8.6. Элементы тепловой теории зажигания электрической искрой
- •8.8. Зажигание твердых и жидких горючих веществ
- •8.9. Зажигание лучистым тепловым потоком
- •8.10. Основные виды и характеристики источников зажигания
- •IV.II. РАЗВИТИЕ ПРОЦЕССОВ ГОРЕНИЯ
- •ГЛАВА 9. ГОРЕНИЕ ГАЗОПАРОВОЗДУШНЫХ СМЕСЕЙ
- •9.1. Концентрационные пределы распространения пламени
- •9.2. Факторы, влияющие на КПР
- •9.2.1. Зависимость КПР от химической природы горючего вещества
- •9.2.2. Влияние начальной температуры смеси на КПР
- •9.2.3. Влияние давления горючей смеси на КПР
- •9.2.4. Влияние флегматизаторов и ингибиторов на КПР
- •ГЛАВА 10. ГОРЕНИЕ ЖИДКОСТЕЙ
- •10.1. Условия для возникновения горения жидкостей
- •9.2. Температурные пределы распространения пламени
- •10.3. Скорость испарения жидкости
- •10.4. Температура вспышки. Температура воспламенения жидкости
- •10.5. Механизм теплового распространения горения жидкостей
- •10.7. Распределение температуры в горящей жидкости
- •10.8. Вскипание и выброс при горении резервуара с ГЖ
- •ГЛАВА 11. ГОРЕНИЕ ТВЕРДЫХ ВЕЩЕСТВ И МАТЕРИАЛОВ
- •11.2. Основные закономерности процессов горения органических твердых горючих материалов
- •11.4. Гетерогенное горение
- •11.5. Горение металлов
- •11.6. Особенности горения пылевидных веществ
- •РАЗДЕЛ V. ВЗРЫВЫ.
- •ГЛАВА 12. ВЗРЫВЫ. УДАРНЫЕ ВОЛНЫ И ДЕТОНАЦИЯ
- •12.1. Основные определения. Типы взрывов
- •12.4. Основные свойства и параметры ударной волны
- •12.6. Взрывчатые вещества
- •12.6.1. Краткие сведения об основных взрывчатых веществах
- •Приложение 1
- •Приложение 2
- •Приложение 3
- •Приложение 4
- •Приложение 5

|
187 |
|
Пример 10.3. В герметичной емкости объемом 30 м3, за- |
Вычисление объемной доли |
|
и объема пара в |
полненной на 1/3, давление паров ацетона при температуре |
паровоздушной смеси |
300С составляет 190 мм рт.ст. Определить концентрацию |
паров ацетона в % и объем его паров в м3 в свободном про- |
|
|
странстве емкости. |
Решение: |
|
1. Объемная концентрация паров в замкнутом объеме рассчитывается через давление насыщенного пара по формуле:
ϕОБ = PPs 100 , % ,
АТМ
(смотри предыдущую задачу).
В условии данной задачи величина атмосферного давления не указана, поэтому принимаем его равным нормальному атмосферному давлению.
Определим объемную концентрацию паров ацетона:
ϕОБ = 190760 100 = 25 %
2.По условию задачи в емкости жидкий ацетон занимает 1/3 всего объема. Следо-
вательно, газообразная фаза, в которую входят пары ацетона и воздух, составляет 2/3 объема емкости или
30 (2/3) = 20 м3.
25 % этого объема составляют пары ацетона. Определим объем паров ацетона в м3: 20 0,25 = 5 м3
9.2. Температурные пределы распространения пламени
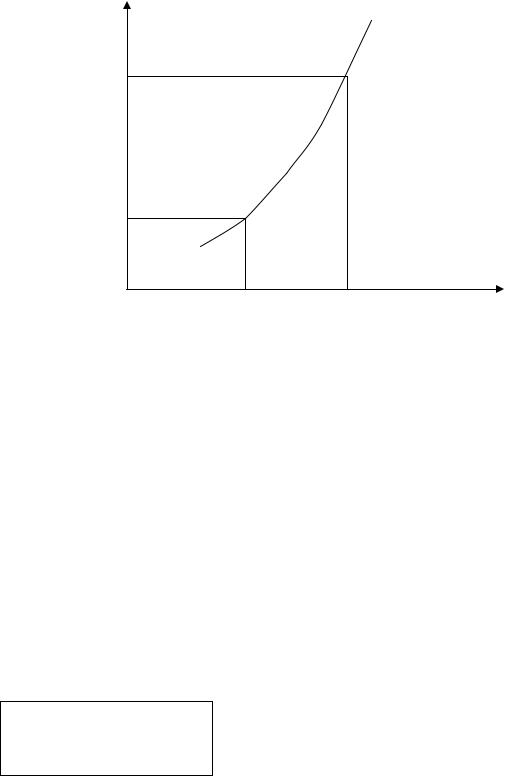
Выражения (10.1) и (10.2) показывают, что парциальное давление насыщенного пара пропорционально температуре жидкости. Графически эта зависимость в общем, виде представлена на рис.10.4 (здесь численные значения Рs пересчитаны на концентрацию пара). На приведенном графике видно, что НКПР и ВКПР пара достигаются при знач ениях температур: Тн и Тв. Эти температуры называются температурными пределами распространения пламени жидкости, обозначаются ТПР.
Нижним (НТПР) или верхним (ВТПР) температурным пределом распространения пламени называется температура жидкости, при которой концентрация паров над ее поверхностью равна соответствующему концентрационному пределу.
Температурные пределы распространения пламени могут быть определены как экспериментальным, так и расчетным путем.
188
φнас,%
φв
φн
Тн |
Тв |
Т |
Рис.10.4. Зависимость концентрации паров от температуры жидкости
Температурные пределы Тн и Тв связаны с КПР пламени зависимостью:
tпр = |
B |
|
− Ca , |
(10.4) |
|
A − lg(0,01 |
ϕпр p0) |
||||
|
|
|
где ϕпр - нижний или верхний КПР, %; Р0 - атмосферное давление, кПа;
А, В, Са - константы уравнения Антуана для давления насыщенных паров.
Расчет ТПР по данным Пример 10.4. Вычислить температурные пределы рас-
уравнения Антуана пространения пламени 2-метилнонана, если известны следующие данные: НКПР 0,71 %; ВКПР 5,4 %; уравнение Ан-
туана lg р = 6,12003 – 1521,3/(202,75 + t); Р0 = 101,3 кПа.
Решение:
Расчет НТПР:

|
|
|
|
|
|
|
|
189 |
|
tн = |
|
1521,3 |
|
|
|
|
|
−202,75 = 40,10С |
|
|
|
|
|
101,3 |
|
||||
6,12003 |
−lg(0,71 |
) |
|
||||||
100 |
|
||||||||
|
|
|
|
|
|
|
|
||
Расчет ВТПР: |
|
|
|
|
|
|
|||
tв = |
|
1521,3 |
|
|
|
−202,75= 79,90С. |
|||
|
−lg(5,4 |
|
101,3 |
) |
|||||
6,12003 |
100 |
|
|
||||||
|
|
|
|
|
|
|
|
||
По справочным данным НТПР 2-метилнонана составляет 430С.
Если неизвестна зависимость давления насыщенного пара от температуры, то для веществ, состоящих из атомов С, Н, О, N значение нижнего или верхнего температурного предела (tп) вычисляют по формуле
|
n |
|
tп = а0 + а1tкип + |
∑a jlj |
(10.5.) |
|
j=2 |
|
где а0 — размерный коэффициент, равный минус 62,46°С для нижнего и минус 41,43°С для верхнего пределов;
а1 — безразмерный коэффициент, равный 0,655 для нижнего и 0,723 для верхнего пределов;
aj — эмпирические коэффициенты, характеризующие вклад j-х структурных групп, приведены в табл. 10.1.
|
|
|
|
|
Таблица 10.1. |
|
Вид |
aj, °C |
Вид |
aj, °C |
|
||
струк- |
tн |
tв |
струк- |
tн |
tв |
|
турной |
|
|
турной |
|
|
|
группы |
|
|
группы |
|
|
|
С—С |
—0,909 |
—1,158 |
C—N |
—2,14 |
0,096 |
|
С=С |
—2,66 |
—4,64 |
N—H |
6,53 |
6,152 |
|
С—Н |
—0,009 |
0,570 |
О—Н |
19,75 |
17,80 |
|
С—О |
0,110 |
1,267 |
|
—4,40 |
—4,60 |
|
|
|
|
|
|
|
|
С=O |
5,57 |
5,86 |
|
|
|
|
Среднее квадратичное отклонение расчета составляет 9 °С.
|
|
|
190 |
|
|
|
|
Пример 10.5. Рассчитать температурные пределы рас- |
|||
Расчет ТПР по |
|
||||
структурной формуле |
пространения пламени этиламина С2Н5NH2. |
||||
вещества |
|
|
|
|
|
|
|
|
|
|
|
Решение: |
|
|
|
|
|
Н |
Н |
Н |
|
Данные для расчета: |
|
|
tкип = |
16,60C |
|||
|
|
|
|
||
Н С |
С |
N Н |
Число связей: |
||
|
|
|
|
||
Н |
Н |
|
|
С – С |
1 |
|
|
|
|
||
|
|
|
|
С – Н |
5 |
|
|
|
|
С – N |
1 |
|
|
|
|
N – Н |
2 |
Для расчета воспользуемся формулой 10.5 и данными таблицы 10.1.
Расчет НТПР:
tн = − 62,46 + 0,655 16,6 + 1 (−0,909) + 5 (– 0,009) +1 (– 2,14) + 2 (6,53) = – 41,60С.
Расчет ВТПР:
tв = − 41,43 + 0,723 16,6 + 1 (−1,158) + 5 (0,570) +1 (0,0967) + 2 (6,152) = – 15,30С.
По справочным данным НТПР этиламина составляет – 390С, ВТПР этиламина составляет – 220С.
Температурные пределы распространения пламени применяются при расчете пожаровзрывобезопасных температурных режимов работы технологического оборудования, при оценке аварийных ситуаций, связанных с разливом жидкостей и для расчетов КПР пламени.
10.3. Скорость испарения жидкости
Интенсивность испарения WИСП жидкости с открытой поверхности может быть определена расчетным путем по следующей формуле
WИСП = 10-6 η |
|
PS , кг/м2 с, |
(10.6.) |
М |
где
M - молярная масса, кг/кмоль;

191
PS - давление насыщенного пара жидкости при рабочей температуре tРАБ, определяемое по номограмме или расчетным способом по уравнению Антуана [3], кПа;
Приведенную формулу допускается использовать для не нагретых выше температуры окружающей среды ЛВЖ при отсутствии справочных и экспериментальных данных.
η - коэффициент, принимаемый по таблице 10.2, приведенной ниже, в зависимости от скорости и температуры воздушного потока над поверхностью испарения
Таблица 10.2.
Скорость воздушного потока Значение коэффициента η при температуре t, ° С, воздуха в помещении
в помещении, м с-1
|
10 |
15 |
20 |
30 |
35 |
|
|
|
|
|
|
0 |
1,0 |
1,0 |
1,0 |
1,0 |
1,0 |
|
|
|
|
|
|
0,1 |
3,0 |
2,6 |
2,4 |
1,8 |
1,6 |
|
|
|
|
|
|
0,2 |
4,6 |
3,8 |
3,5 |
2,4 |
2,3 |
|
|
|
|
|
|
0,5 |
6,6 |
5,7 |
5,4 |
3,6 |
3,2 |
|
|
|
|
|
|
1,0 |
10,0 |
8,7 |
7,7 |
5,6 |
4,6 |
Масса испарившейся жидкости рассчитывается по следующей форму-
ле:
mИСПАР. ЖИДК. = SИСП WИСП τИСП, |
(10.7) |
где
SИСП - площадь испарения жидкости, м2; τИСП - время испарения, с;
WИСП - интенсивность испарения, кг/м2 с.
Площадь испарения жидкости SИСП определяется исходя из следующего расчета:
1 литр смесей и растворов, содержащих 70 % и менее
(по массе) растворителей разливается на площади 0,5 м2., соответственно 1 м3 разливается на площади 500 м2.
1 литр остальных жидкостей разливается на площади 1,0 м2, соответственно 1 м3 разливается на площади 1000 м2.
