
Пособие Гравиметрия решение задач Зарембо, Аладжаловa 2013
.pdf
KS0 = [M ]p [A]q .
Для Ag2CrO4 p = 2, q = 1, тогда: |
|
|
|||||||||
K 0 |
(Ag |
|
CrO ) = [Ag+]2 [CrO−2 |
] |
|
||||||
S |
|
2 |
|
4 |
|
|
|
4 |
|
|
|
[CrO |
−2 |
] = |
K 0 |
(Ag |
CrO ) |
, |
|
|
|||
|
S |
2 |
|
4 |
|
|
|||||
|
4 |
|
|
|
|
[Ag+]2 |
|
|
|
|
|
где [Ag+], моль/л – равновесная молярная концентрация ионов серебра |
|||||||||||
в растворе. |
|
|
|
|
|
|
|||||
[Ag+] |
можно |
рассчитать |
через |
заданную массовую концентрацию |
|||||||
ρ(Ag+) = 20мг/л = 2,0 10−2 г/л по формуле (16):
[Ag+] = ρ(Ag+) = 2,0 10−2 г/л =1,9 10−4 моль/л. M (Ag) 107,8г/моль
Тогда: |
|
|
|
|
|
|
|
|
|
[CrO |
−2 |
] = |
K 0 |
(Ag CrO ) |
= |
1,1 10−12 |
=3,1 10 |
−5 |
моль/л |
|
S |
2 4 |
|
|
|||||
|
(1,9 10−4 )2 |
|
|||||||
4 |
|
|
|
[Ag+]2 |
|
|
|
|
2)Для PbCrO4 р =1, q = 1, тогда:
K 0 |
(PbCrO ) = [Pb+2 ] [CrO−2 |
] |
|
|||||
S |
|
|
|
4 |
|
4 |
|
|
[CrO |
−2 |
] = |
K 0 |
(PbCrO ) |
, |
|
|
|
|
S |
4 |
|
|
||||
|
|
[Pb+2 ] |
|
|
||||
|
4 |
|
|
|
|
|
|
|
где [Pb+2 ], моль/л – равновесная молярная концентрация ионов свинца |
||||||||
в растворе. |
|
|
|
|
||||
[Pb+2 ] |
можно |
рассчитать через |
заданную массовую концентрацию |
|||||
ρ(Pb+2 ) = 20мг/л = 2,0 10−2 г/л по формуле (16):
51

[Pb |
+2 |
] = |
ρ(Pb+2 ) |
= |
2,0 10−2 г/л |
=9,7 |
10 |
−5 |
моль/л. |
|||||||
|
M (Pb) |
207,19г/моль |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Тогда: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[CrO |
|
−2 |
] = |
K 0 (PbCrO ) |
= |
1,8 10−14 |
=1,9 10 |
−10 |
моль/л |
|||||||
|
|
S |
|
4 |
9,7 10−5 |
|
||||||||||
|
4 |
|
|
|
[Pb+2 ] |
|
|
|
|
|
|
|||||
Расчет показывает, что для образования осадка PbCrO4 нужна гораздо меньшая концентрация [СrO4−2 ] (1,9 10−10 моль/л << 3,1 10−5 моль/л), поэтому он выпадет первым.
Пример 21. Рассчитать, при какой концентрации гидроксид-ионов начнется осаждение гидроксида магния из 0,010М раствора хлорида магния.
KS 0 (Mg(OH )2 ) =6,0 10−10 . Влияние ионной силы не учитывать.
Решение:
Реакция осаждения:
Mg2+ +2 OH − = Mg(OH )2 ↓
Осадок начнет образовываться при условии выполнения зависимости (33):
[Mg2+] [OH −]2 > KS 0 (Mg(OH )2 ) ,
где [Mg2+] =с(MgCl2 ) =0,010моль/л.
Отсюда:
[OH |
− |
] = |
K |
0 (Mg(OH ) |
) |
, |
|
S |
2 |
|
|||
|
|
[Mg2+] |
|
|||
|
|
|
|
|
|
52

[OH −] = |
6,0 10−10 |
= 2,45 10−4 моль/л. |
|
0,010 |
|
Ответ: осаждение Mg(OH )2 начнется при концентрации OH − ионов равной
2,45 10−4 моль/л.
Врасчетах условий образования осадка зависимостью (33) можно пользоваться только при малой ионной силе раствора (I ≤ 0,001) или при проведении приближенных расчетов.
Вреальных условиях влиянием ионной силы раствора часто пренебречь нельзя. В этом случае для точных расчетов используют зависимость (31).
Пример 22. Рассчитать, при какой концентрации гидроксид-ионов начнется осаждение гидроксида магния из 0,01М раствора хлорида магния. Расчет выполнить с учетом влияния ионной силы раствора.
KS 0 (Mg(OH )2 ) =6,0 10−10 .
Решение:
Реакция осаждения:
Mg2+ +2 OH − = Mg(OH )2 ↓
При условии влияния ионной силы раствора, осадок начнет образовываться при выполнении неравенства (31):
[Mg2+] [OH −]2 > Ks (Mg(OH )2 )
Отсюда:
53

[OH −] = |
KS (Mg(OH )2 ) |
|
[Mg2+] |
Для расчета концентрационной константы растворимости KS (Mg(OH )2 )
необходимо вычислить ионную силу раствора, создаваемую ионами магния и хлорид-ионами. В соответствии с уравнением (4):
I = 12 ∑(ci zi2 ) =
=12 (c(Mg2+) z2 (Mg2+) +c(Cl−) z2 (Cl−)) =
=12 (0,01 22 +2 0,01 12 ) =0,03.
По таблице справочника [5] для I = 0,03 можно найти коэффициенты активности ионов, образующих осадок:
γ(Mg2+) = 0,54;
γ(OH–) =0,85,
Величину |
|
|
концентрационной |
константы растворимости осадка |
||||||||||||||||
( KS (Mg(OH )2 ) можно рассчитать используя формулу (3): |
||||||||||||||||||||
K |
|
= |
K 0 |
, |
|
|
|
|
|
|
|
|
|
|
|
|||||
S |
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
γ p |
|
γq |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
M |
|
A |
|
|
|
|
|
|
|
|
|
|
|
|
||
K |
S |
(Mg(OH ) |
) = |
KS0 (Mg(OH )2 ) |
= |
|
6,0 10−10 |
|
=1,54 10−9 |
|||||||||||
γ(Mg2+) γ2 (OH −) |
0,54 (0,85)2 |
|||||||||||||||||||
|
|
|
|
|
|
|
2 |
|
|
|
||||||||||
Тогда: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
[OH |
− |
] = |
K |
S |
(Mg(OH ) |
) |
= |
1,54 10−9 |
=3,9 10 |
−4 |
(моль/л) |
|||||||||
|
|
|
|
2 |
|
0,01 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
[Mg2+] |
|
|
|
|
|
|
|
||||
Ответ: |
|
|
|
[OH −] =3,9 10−4 моль/л. |
|
|
|
|
|
|
||||||||||
54
Результаты расчетов в примерах 21 и 22, показывают, что при учете влияния ионной силы концентрация осадителя (OH − ионов), необходимая для образования осадка, больше. Это объясняется тем, что солевой эффект увеличивает растворимость осадка.
3.3.5 Расчет условий полного осаждения
Значение растворимости можно использовать также при оценке полноты осаждения определяемого иона.
Осаждение считается практически полным (количественным), если выполняются условия:
•масса потери осадка не превышает абсолютной погрешности взвешивания на аналитических весах (±10–4г);
•допустимое значение растворимости осадка (Sдоп.) не превышает 10–6моль/л.
При объеме раствора V ≈ 0,5л и молярной массе осадка Mос. ≈ 200г/моль
Sдоп. = |
nпотери |
= |
|
mпотери |
= |
10−4 |
=10 |
−6 |
моль/л |
|
V |
V Mос. |
0,5 |
200 |
|
||||||
|
|
|
|
|
|
|||||
Выполнение неравенств |
|
|
|
|
|
|
||||
mпотери ≤ 10–4 г, |
|
|
|
|
|
(34) |
||||
Sдоп. ≤ 10–6 моль/л |
|
|
|
|
|
(35) |
||||
принимается как количественный критерий полного осаждения.
Пример 23. Можно ли практически полностью осадить Са2+ в виде CaF2? Рассчитать избыточную молярную концентрацию NH4F, необходимую для обеспечения полного осаждения кальция. KS0 (CaF2 ) = 4,0 10−11 .
55

Решение:
Условие полного осаждения ионов Са2+: S = [Ca2+] ≤ 10–6моль/л.
Для расчета равновесной концентрации ионов Са2+ в насыщенном растворе надо записать равновесие между осадком CaF2 и раствором:
CaF2 R |
Са2+ + 2F – |
осадок |
раствор |
Исходя из стехиометрии равновесия растворимости, равновесные концентрации ионов Са2+ и F– составят:
[Ca2+] = S;
[F −] = 2S.
Выражение для константы растворимости будет иметь вид:
K |
S |
(CaF ) =[Ca2+] [F −]2 = S (2S)2 = 4S3 , |
|
|||||
|
|
2 |
|
|
|
|
|
|
отсюда: |
|
|
|
|
|
|
|
|
[Ca2+] ≡ S = |
3 KS (CaF2 ) . |
|
||||||
|
|
|
|
|
4 |
|
|
|
Полагая, |
что |
K |
S |
(CaF ) = K 0 |
(CaF ) = 4,0 10−11 |
(не учитывая ионную силу |
||
|
|
|
|
2 |
S |
2 |
|
|
раствора), получим: |
|
|
|
|||||
[Ca2+] ≡ S = |
3 4,0 10−11 |
= 2,2 10−4 моль/л |
|
|||||
|
|
|
|
|
4 |
|
|
|
Расчет показывает, что равновесная концентрация ионов кальция (растворимость осадка CaF2) ≈ в 200 раз больше допустимой (Sдоп. ≤ 10–6моль/л). Следовательно, полностью осадить кальций можно только в том случае, если использовать избыток осадителя NH4F (одноименного иона).
56

Избыточную молярную концентрацию NH4F можно рассчитать из уравнения
(27):
KoS =(pS)p·CAq |
. |
Для осадка CaF2 : р =1; q = 2,
тогда: K 0 |
(CaF ) = S (C |
NH4F |
)2 |
=[Ca+2 ] (C |
NH4F |
)2 |
|
|
||||||||
|
S |
|
2 |
|
|
|
|
|
|
|
|
|
|
|||
С |
|
|
= |
K |
S |
(CaF ) |
= |
4,0 10−11 |
=6,32 10 |
−3 |
моль/л. |
|||||
NH4F |
|
|
2 |
10−6 |
|
|||||||||||
|
|
[Ca2+] |
|
|
|
|
|
|
|
|
||||||
Ответ: Полностью осадить кальций нельзя. Для полного осаждения необходима избыточная концентрация осадителя: СNH4F =6,32 10−3 моль/л.
Пример 24. Ионы серебра осадили стехиометрическим количеством хлорид-ионов из раствора общим объемом 100мл. Рассчитать массу серебра, оставшегося в растворе. Будет ли полным осаждение ионов серебра?
KS0 (AgCl) =1,78 10−10 .
Решение:
Ag+ +Cl− = AgCl ↓
Не учитывая влияние ионной силы раствора, растворимость осадка AgCl можно рассчитать, используя уравнение (22) для бинарного соединения:
S =С |
Ag |
+ = |
K |
0 |
(AgCl) = 1,78 10−10 |
=1,33 10−5 моль/л |
|
|
|
S |
|
|
Зная растворимость, можно рассчитать массу серебра, оставшегося в растворе по (29):
57
m(Ag) = S V M (Ag) =
=1,33 10−5 моль/л 0,1л 108г/моль =1,44 10−4 г.
Поскольку условие полного осаждения не выполняется: m(Ag) > 10–4г (больше погрешности взвешивания на аналитических весах), осаждение ионов серебра из раствора будет неполным.
Ответ: m(Ag) =1,4 10−4 г. Осаждение неполное.
Пример 25. К 150мл 0,05М раствора Н2SO4 добавили 100мл раствора, содержащего 0,42г BaCl2. Вычислить массу бария в растворе над осадком.
Будет ли осаждение бария полным? KS0 (BaSO4 ) =1,1 10−10 .
Решение:
H2SO4 + ВаСl2 = ВаSO4 ↓+2НСl
По уравнению реакции осаждения вещества взаимодействуют в равных количествах. Уравнение материального баланса имеет вид:
n(H2SO4 ) = n(ВаСl2 ).
По условию задачи можно рассчитать количество вещества Н2SO4 и BaCl2 в исходных растворах:
n(H2SO4 ) =c(H2SO4 ) V (H2SO4 ) =0,05ммоль/мл 150мл =7,5ммоль,
n(BaCl2 ) = |
m(BaCl2 ) |
= |
420,0мг |
2,0 ммоль. |
|
M (BaCl2 ) |
208,3мг/ммоль |
||||
|
|
|
Следовательно, взят избыток Н2SO4:
n(H2SO4 )изб. =7,5 −2,0 =5,5 (ммоль).
58
Избыточная концентрация Н2SO4 составит:
c(H SO ) |
изб. |
= |
n(H2SO4 )изб. |
= |
|
5,5 |
= 2,2 10−2 ммоль/мл = |
|
|
||||||
2 4 |
|
Vобщ. |
150 +100 |
|
|||
|
|
|
|
||||
= 2,2·10–2 моль/л.
Растворимость осадка ВаSO4 в присутствии избытка осадителя можно рассчитать по формуле (28):
S =[Ba |
2+ |
] = |
K 0 |
(BaSO ) |
= |
1,1 10−10 |
=5 10 |
−9 |
моль/л. |
|
|
S |
|
4 |
2,2 10−2 |
|
|||||
|
c(Н SO ) |
изб. |
|
|||||||
|
|
|
|
|
|
|
||||
|
|
|
|
2 4 |
|
|
|
|
|
|
Зная растворимость осадка (молярную равновесную концентрацию иона бария) по формуле (29) можно рассчитать массу бария в растворе над осадком:
m(Ba) = S V M (Ba) =5 10−9 моль/л 0,250л 137г/моль = 2 10−7 г.
Условие полного осаждения выполняется: m(Ba) 10−4 г, |
следовательно, |
осаждение бария полное. |
|
Ответ: m(Ba) = 2 10−7 г. Осаждение полное. |
|
3.3.6 Влияние «солевого эффекта» на растворимость осадка
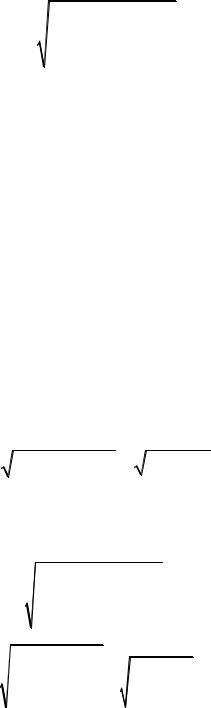
При введении в гетерогенную систему осадок – раствор электролита, не имеющего одноименного иона с осадком, увеличивается ионная сила раствора и, соответственно, уменьшаются коэффициенты активности ионов осадка. Расчет растворимости осадка M p Aq в этом случае проводят по
формуле (21):
59
|
|
|
|
K0 |
|
|
|
|
||
S = p+q |
|
|
|
|
S |
|
|
|
|
. |
p |
p |
q |
q |
γ |
|
p |
γ |
q |
||
|
|
|
M |
A |
|
|||||
|
|
|
|
|
|
|
|
|||
Анализ формулы показывает, что уменьшение коэффициентов активности приводит к увеличению растворимости осадка. Это явление называется «солевым эффектом».
Пример 26. Рассчитать растворимость осадка оксалата кальция в воде и в 0,01М растворе нитрата калия. KS0 (CaC2O4 ) = 2,3·10–9. Сделать выводы.
Решение: |
|
CaC2O4 бинарное соединение: |
p = 1; q = 1. |
Растворимость в воде можно рассчитать по формуле (22):
S = K |
0 (СаС О ) = 2,3 10−9 |
= 4,8 10−5 моль/л. |
S |
2 4 |
|
Растворимость в 0,01М растворе КNO3 можно рассчитать по формуле (21):
|
|
|
K0 |
|
|
|
|
||
S = p+q |
|
S |
|
|
|
|
|
||
|
p p qq γ |
p |
γq |
||||||
|
|
|
|
|
M |
A |
|
||
S = |
0 |
(СаС2О4 ) = |
2,3 10−9 . |
|
|||||
KS |
|
||||||||
|
γM γA |
|
|
γM γA |
|
|
|||
Ионная сила 0,01М раствора КNO3 равна 0,01.
По справочной таблице [5] можно найти коэффициенты активности ионов осадка:
γ(Са2+) = 0,66;
γ(C2O4−2 ) =0,66,
60
