
- •Глава 1. Основні положення титриметричного аналізу
- •Вимоги до реакцій у титриметричному аналізі
- •Класифікація методів титриметрії в залежності від типу реакції
- •Класифікація методів титриметрії за способом титрування
- •Способи приготування стандартних розчинів
- •1. Приготування первинних стандартних розчинів
- •2. Приготування вторинних стандартних розчинів
- •3. Приготування стандартних розчинів із фіксаналів
- •Глава 2. Розрахунки в титриметричному аналізі
- •2.1. Способи виразу концентрації речовин у розчинах у титриметрії
- •Глава 3. Метод кислотно–основного титрування Теоретичні основи
- •Індикатори методу кислотно-основного титрування
- •Показник індикаторів рК, показник титрування рН
- •Класифікація індикаторів
- •Криві титрування
- •1. Титрування сильних кислот сильними основами (Рис 1.)
- •2.Титрування слабких основ сильними кислотами. (Рис 2.)
- •3. Титрування слабких кислот сильними основами.(Рис 3.)
- •4. Титрування слабких кислот слабкими основами. (Рис. 4)
- •5. Титрування багатоосновних кислот (Рис 5.)
- •Кислотно-основне титрування в неводних середовищах
- •Робочі розчини у методах неводного титрування
- •Практичне використання методів кислотно-основного титрування в аналізі фармацевтичних препаратів
- •Практична робота способи виразу вмісту речовин у розчинах
- •Приклади розв’язання задач
- •Практична робота розрахунок результатів аналізу в титриметрії
- •Приклади розв'язання задач
- •Використаний аналітичний прийом – метод піпетування.
- •Розв’язання задачі
- •Використаний прийом – метод окремих наважок.
- •Розв’язання задачі
- •Лабораторна робота приготування та стандартизація титранту натрій гідроксиду
- •Хімізм процесу
- •План експерименту
- •Висновок
Криві титрування
Для того, щоб мати можливість вибрати індикатор для титрування, крім якісних показників, застосовують методи, які дають кількісну характеристику цього процесу. До таких методів відносять метод побудови «кривих титрування».
Криві кислотно-основного титрування графічного відбивають залежність зміни рН розчину, що титрують, від об'єму доданого титранту: рН = f(V). Для побудови кривих розраховують значення рН розчину, що титрується, в різних точках титрування для вихідного розчину: до точки еквівалентності, в точці еквівалентності, після точки еквівалентності. При побудові графіку на осі ординат відкладають величину рН, а на осі абсцис – кількість розчину титранту (у см3). При цьому утворюється крива, яка буде характеризувати зміну рН в залежності від об’єму прилитого титранта.
Не наводячи розрахунків, наведемо загальний вигляд кривих титрування основних типів реакцій кислотно-основної взаємодії.
1. Титрування сильних кислот сильними основами (Рис 1.)
При титруванні в точці еквівалентності утворюється розчин солі сильної основи і сильної кислоти, який має нейтральну реакцію (рН = 7).
Найкращим індикатором у цьому випадку буде індикатор, для якого рТ = 7. Крім того, враховуючи те, що інтервал рН стрибка титрування від 4 до 10, можна брати індикатори, що мають інтервал переходу в межах інтервалу стрибка титрування.
2.Титрування слабких основ сильними кислотами. (Рис 2.)
Внаслідок титрування слабкої основи сильною кислотою утворюється сіль слабкої основи і сильної кислоти. Такі солі у водних розчинах зазнають гідролізу, і реакція розчину буде слабокислою (рН < 7). Таким чином, при титруванні слабких основ сильними кислотами треба використовувати індикатори, що мають рТ < 7. Щоб вибрати індикатор з потрібною величиною рТ, обчислюють рН розчину у точці еквівалентності, беруть той індикатор, для якого рТ максимально наближається до значення рН у точці еквівалентності.
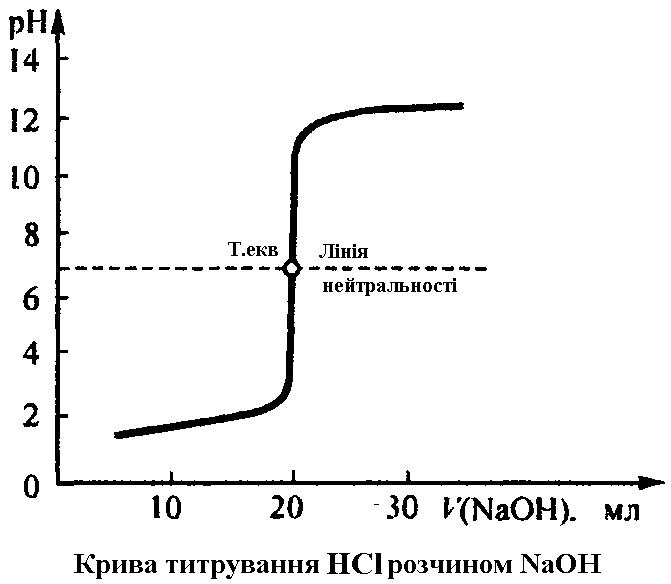
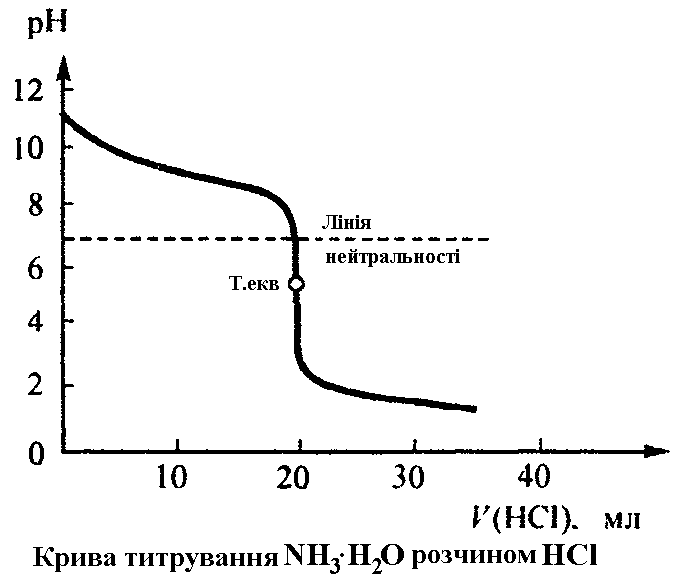
Рис 1. Рис 2.
3. Титрування слабких кислот сильними основами.(Рис 3.)
При взаємодії слабкої кислоти і сильної основи утворюється сіль сильної основи і слабкої кислоти. Внаслідок гідролізу такої солі реакція розчину буде слабколужною рН > 7. При титруванні в цьому випадку треба використовувати індикатори, що мають рТ > 7. Обчислюють рН розчину в точці еквівалентності і оберають той індикатор, для якого рТ максимально наближається до значення рН у точці еквівалентності.
4. Титрування слабких кислот слабкими основами. (Рис. 4)
У процесі взаємодії слабкої кислоти із слабкою основою утворюється буферна суміш. До точки еквівалентності буферна суміш складається із слабкої кислоти і її солі, а після точки еквівалентності – із слабкої основи та її солі.
При взаємодії слабкої кислоти зі слабкою основою стрибка титрування практично немає. Таким чином, відтитрувати слабку кислоту слабкою основою практично неможливо.
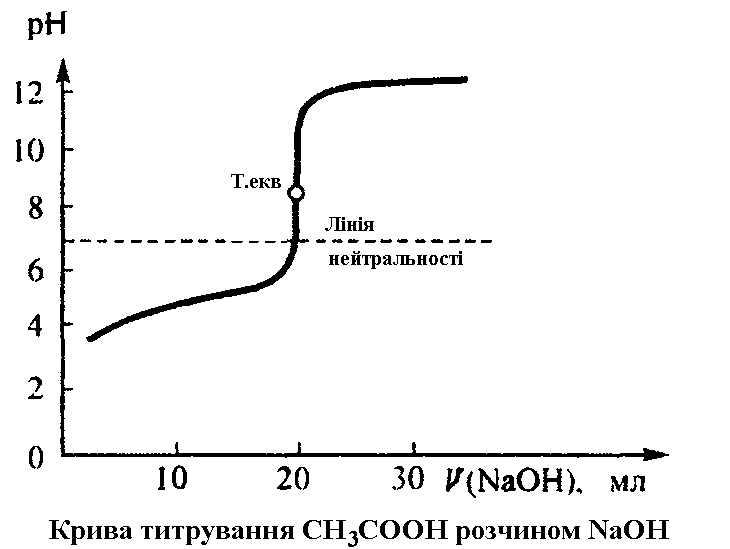
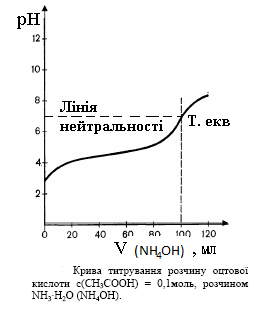
Рис 3. Рис 4.
