
- •Глава 1. Основні положення титриметричного аналізу
- •Вимоги до реакцій у титриметричному аналізі
- •Класифікація методів титриметрії в залежності від типу реакції
- •Класифікація методів титриметрії за способом титрування
- •Способи приготування стандартних розчинів
- •1. Приготування первинних стандартних розчинів
- •2. Приготування вторинних стандартних розчинів
- •3. Приготування стандартних розчинів із фіксаналів
- •Глава 2. Розрахунки в титриметричному аналізі
- •2.1. Способи виразу концентрації речовин у розчинах у титриметрії
- •Глава 3. Метод кислотно–основного титрування Теоретичні основи
- •Індикатори методу кислотно-основного титрування
- •Показник індикаторів рК, показник титрування рН
- •Класифікація індикаторів
- •Криві титрування
- •1. Титрування сильних кислот сильними основами (Рис 1.)
- •2.Титрування слабких основ сильними кислотами. (Рис 2.)
- •3. Титрування слабких кислот сильними основами.(Рис 3.)
- •4. Титрування слабких кислот слабкими основами. (Рис. 4)
- •5. Титрування багатоосновних кислот (Рис 5.)
- •Кислотно-основне титрування в неводних середовищах
- •Робочі розчини у методах неводного титрування
- •Практичне використання методів кислотно-основного титрування в аналізі фармацевтичних препаратів
- •Практична робота способи виразу вмісту речовин у розчинах
- •Приклади розв’язання задач
- •Практична робота розрахунок результатів аналізу в титриметрії
- •Приклади розв'язання задач
- •Використаний аналітичний прийом – метод піпетування.
- •Розв’язання задачі
- •Використаний прийом – метод окремих наважок.
- •Розв’язання задачі
- •Лабораторна робота приготування та стандартизація титранту натрій гідроксиду
- •Хімізм процесу
- •План експерименту
- •Висновок
Практична робота розрахунок результатів аналізу в титриметрії
Мета: навчитися проводити розрахунки за результатами кількісного титриметричного аналізу.
Приклади розв'язання задач
Приклад 1. На титрування янтарної кислоти масою 0,1560 г витрачено 26,00 см3 розчину КОН. Визначити молярну концентрацію еквіваленту і титр розчину КОН.
Дано: |
Рішення: |
m(H2C4H4O4) = 0,1560 г V(KOH)= 26,00 см3 |
Хімізм: H2C4H4O4 +2KOH = K2C4H4O4 + 2H2O З рівняння реакції вибігає, що:
1. Розраховуємо молярну концентрацію еквіваленту розчину КОН:
2. Розраховуємо титр розчину КОН:
|
с(KOH) – ? TKOH– ? |
|
|
Відповідь: с(КОН) = 0,1016 моль/дм3, ТКОН = 0,005701 г/см3. |
Приклад 2. На нейтралізацію 25,00 см3 розчину H2SO4 з с(1/2H2SO4) = 0,1125 моль/дм3 витрачено 28,50 см3 розчину NaOH. Обчислити молярну концентрацію еквівалента NaOH.
Дано: |
Рішення: |
V(H2SO4)= 25,00 см3 с(1/2H2SO4) = 0,1125 моль/дм3
|
Хімізм: H2SO4 +2NaOH = Na2SO4 + 2H2O
За законом еквівалентів розраховуємо молярну концентрацію еквіваленту розчину NaOH:
|
с(NaOH) – ?
|
|
|
Відповідь: с(NaOH) = 0,09868 моль/дм3. |
Приклад 3. Наважка технічної оксалатної кислоти масою 1,7020 г розчинена у мірній колбі місткістю 250,00 см3. На титрування 20,00 см3 одержаного розчину було використано 19,50 см3 стандартного розчину лугу (К=1,006; с(NaOH) = 0,1 моль/дм3). Визначити масову частку кристалогідрату оксалатної кислоти в технічному продукті.
Використаний аналітичний прийом – метод піпетування.
Алгоритм розв’язання задачі в загальному вигляді:
Визначити концентрацію основного компоненту, використовуючи основне рівняння титриметрії:
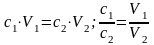
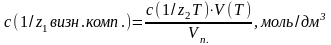 (1)
(1)
де: с(1/z2T) – молярна концентрація еквіваленту титранту, моль/дм3;
V(T) – об’єм титранту, витрачений на титрування, см3;
Vп. – об’єм піпетки (аліквоти, дослідного розчину), см3.
Визначити масу основного компоненту в мірній колбі Vм.к.:
 (2)
(2)
де: с(1/z1 визн.комп.) – молярна концентрація еквіваленту визначаємого компоненту в розчині, моль/дм3;
М(1/z1 визн.комп.) – молярна маса еквіваленту визначає мого компоненту, г/моль.
Визначити масову частку (ω) основного компоненту в досліджуваній речовині, тобто у вихідній наважці mнав.:
-
mнав.
-
100 %
m(визн.комп.)
-
ω
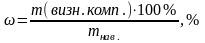 (3)
(3)
Для виведення загальної формули послідовно підставити в формулу (3) необхідні значення з формул (1) та (2).
Загальна формула розрахунку результатів аналізу за методом піпетування:
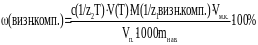

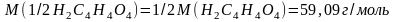
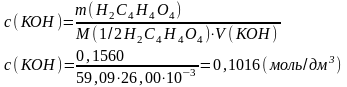
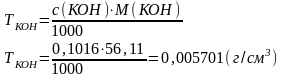
 V(NaOH)
= 28,50 см3
V(NaOH)
= 28,50 см3