
- •Безопасность жизнедеятельности
- •1. Контроль состава воздуха.
- •2. Метеорологические условия на производстве и их влияние на организм человека.
- •3.Защитное заземление.
- •З ануление.
- •4. Условия поражения человека током в сетях напряжением до 1 кВ.
- •5. Защита атмосферного воздуха от загрязнения промышленными выбросами.
- •6. Оказание первой помощи пострадавшему.
- •7. Правила котлонадзора.
- •8. Приборы безопасности.
- •9. Предохранительные устройства топки и газоходов.
- •Предохранительные клапаны.
- •Энергосбережение в теплоэнергетике и теплотехнологиях Теоретические основы теплотехники
- •1. Первый закон термодинамики и его математическое обоснование.
- •2. Второй закон термодинамики и его математические выражения. Круговые процессы. Цикл Карно (прямой и обратный) и его анализ. Понятие о обобщённом цикле Карно.
- •4. Эксергия, её свойства и физический смысл. Эксергия теплоты, потока и квазистатической системы.
- •5. Уравнения состояния идеальных и реальных газов и паров.
- •7. Циклы пту. Общая характеристика. Цикл Ренкина и его анализ. Методы повышения эффективности циклов пту.
- •8. Циклы теплофикационных пту.
- •Нетрадиционные и возобновляемые источники энергии
- •1. Виды возобновляемых источников энергии и возможности их использования.
- •Способы использования энергии солнца.
- •3. Использование энергии ветра.
- •4. Использование энергии воды.
- •5. Использование энергии биомассы.
- •Энергетические системы обеспечения жизнедеятельности
- •1. Теплотехнический расчет наружного ограждения.
- •2. Определение теплопотерь отапливаемого помещения.
- •3. Схемы систем водяного отопления
- •4. Преимущества и недостатки парового отопления по сравнению с водяным.
- •5. Системы воздушного отопления.
- •6. Системы кондиционирования воздуха.
- •7. Схемы внутреннего водопровода.
- •8. Элементарные процессы обработки воздуха в I – d диаграмме.
- •Источники и системы теплоснабжения промышленных предприятий
- •1. Устройство и работа тэс.
- •2. Выбор начальных параметров пара на кэс и в котельной.
- •3. Регенеративный подогрев питательной воды на тэс.
- •4. Термическая деаэрация питательной воды.
- •5. Способы выработки производственного пара на тэц.
- •6. Схема выработки горячей воды на тэц.
- •7. Экономия топлива при комбинированной выработке энергии на тэц.
- •8. Устройство и работа водогрейной котельной.
- •9. Устройство и работа паровой котельной.
- •10. Присоединение систем отопления к тепловой сети.
- •Зависимые схемы присоединения систем отопления.
- •Схемы с насосом и элеватором
- •11. Схемы присоединения систем горячего водоснабжения. Закрытые тепловые сети.
- •Двухступенчатая смешанная схема горячего водоснабжения.
- •Двухступенчатая последовательная схема.
- •Двухступенчатая смешанная схема с ограничением максимального расхода воды на ввод.
- •Открытые тепловые сети.
- •12. Пьезометрический график
- •Отопительно-бытовой график центрального качественного регулирования
- •Регулирование разнородной нагрузки при отопительном графике.
- •Центральное качественное регулирование по совмещенной нагрузке.
- •15. Тепловой расчет трубопроводов.
- •16. Устройство и конструктивные особенности тепловых сетей.
- •17. Испытания тепловых сетей.
- •1. Гидравлические испытания на прочность и плотность
- •2. Испытания на максимальную температуру теплоносителя.
- •3. Испытания на тепловые потери.
- •4. Испытания на гидравлические потери
- •5.Испытания на потенциалы блуждающих токов.
- •18. Защита теплосети от коррозии
- •Контроль за использованием блуждающих токов
- •Котельные установки и парогенераторы
- •1. Общая характеристика топлив и классификация топлив.
- •Классификация топлив.
- •2. Термические характеристики топлив.
- •3. Подготовка к сжиганию твердого топлива.
- •4. Закономерности измельчения топлива.
- •6. Тепловой баланс котельного агрегата.
- •Кпд котельного агрегата и расход топлива.
- •7. Принципиальная технологическая схема котельной установки и ее оборудование
- •Тепломассообменное оборудование промышленных предприятий
- •Основные виды расчетов тепломассообменных аппаратов
- •Классификация тепломассообменных аппаратов
- •Методика теплового расчета рекуперативных тепломассообменных аппаратов
- •Деаэраторы
- •Выпарные установки
- •Гидравлический расчет рекуперативных тепломассообменных аппаратов
- •Сушильные установки и рациональное использование тепловой энергии
- •Тепловые двигатели и нагнетатели
- •Принцип действия основных типов нагнетателей (центробежный, осевой, вихревой, поршневой, ротационный, струйный, эрлифт).
- •Производительность, напор, давление, мощность и кпд нагнетателя.
- •Характеристики центробежного нагнетателя (напор, мощность, кпд).
- •Способы регулирования центробежных нагнетателей.
- •Параллельное и последовательное соединение центробежных нагнетателей.
- •7.Принцип действия, работа, мощность и кпд поршневого компрессора.
- •10. Характеристики и методы регулирования производительности осевых нагнетателей.
- •11. Классификация и обозначение паровых турбин.
- •12. Мощности и кпд паротурбинных установок.
- •13. Преобразование энергии парового потока в турбинной ступени. Активная ступень.
- •Реактивная ступень.
- •14. Виды внутренних и внешних потерь в паровой турбине. Внутренние потери
- •Внешние потери.
- •15. Способы парораспределения в паровых турбинах.
- •16. Турбины с промежуточными регулируемыми отборами пара.
- •Турбина с одним отбором.
- •Т урбины с 2-мя промежуточными регулируемыми отборами пара.
- •Технологические энергоносители предприятий
- •1. Виды нагрузок на воздушную компрессорную станцию и выбор воздушного компрессора.
- •2. Вспомогательное оборудование воздушных компрессорных станций.
- •5. Классификация холодильных машин.
- •6. Работа одноступенчатой парокомпрессионной холодильной машины. Схема парокомпрессионной холодильной установки.
- •7. Схема простейшей абсорбционной холодильной машины.
- •8. Подготовка воздуха к промышленному разделению.
- •9. Схемы производственных систем водоснабжения.
- •Теплоэнергетические системы промышленных предприятий
- •1. Способы теплоснабжения жилых поселков. Их характеристика и эффективность.
- •2. Расчет тепловых нагрузок коммунальных потребителей и промышленных предприятий по удельным тепловым потокам. Расчет отопительной нагрузки.
- •Расчет вентиляционной нагрузки.
- •Расчет нагрузки гвс.
- •3. Выбор теплоносителя, его параметров и расхода.
- •4. Выбор паровых турбин и энергетических паровых котлов тэц.
- •5. Выбор оборудования теплофикационной установки тэц. Ремонт и эксплуатация теплоэнергетического оборудования
- •1. Эксплуатация топливного хозяйства.
- •2.Основы эксплуатации котельных установок. Пуск, останов, случаи аварийного останова.
- •Останов котла.
- •Аварийные случаи останова котла
- •3.Эксплуатация центробежных машин. Вентиляторы. Насосы. Дымососы.
- •5.Методы очистки поверхностей нагрева. Очистка поверхностей нагрева от золы.
- •6.Методы повышения надежности сложных систем
- •7. Ремонт энергооборудования.
- •9.Приемка оборудования из ремонта.
- •Охрана окружающей среды в энергетике
- •1. Нормирование выбросов в атмосферу
- •2. Сравнительные хар-ки сухих инерционных з/ул-ей
- •3. Аппараты мокрой очистки газов
- •5. Снижение выбросов оксидов серы и азота.
- •7. Упрощенные малозатр-е техн-гии сероочистки
- •8. Очистка дымовых газов от оксидов азота.
- •9. Режимно-конструктивные мероприятия по снижению nOx.
- •10. Выбор высоты дымовой трубы по условиям рассеивания
Энергосбережение в теплоэнергетике и теплотехнологиях Теоретические основы теплотехники
1. Первый закон термодинамики и его математическое обоснование.
Количество теплоты, переданное системе, идёт на изменение внутренней энергии системы и работу системы против внешних сил.
Составим энергетический баланс открытой термодинамической системы

Внешним называют устройство потому, что с помощью него можно подводить работу из вне или отводить.
Рассмотрим случай подвода энергии в форме работы и теплоты.
Для произвольного расхода рабочего тела уравнения сохранение энергии
Е2-Е1=Q+(-Lтехнич); E1 и Е2 полная энергия потока во I и II сечении.
Для mсек=1 е2-е1=q-lтехнич; е1 и е2 удельная энергия потока во I и II сечении.
ΔU=U2-U1 – изменение внутренней энергии.
![]() ;
;
![]() -
изменение удельной потенциальной
энергии.
-
изменение удельной потенциальной
энергии.
![]() ;
;
![]() -
изменение удельной кинетической энергии.
-
изменение удельной кинетической энергии.
За 1 секунду перемещение составит х1 – х2
![]()
Уравнение неразрывности или сплошности потока
![]() mсек1=mсек2
mсек1=mсек2
![]() - работа по
перемещению (статический напор)
- работа по
перемещению (статический напор)
![]() -
работа по перемещению рабочего тела
между сечениями I-I
и II-II.
-
работа по перемещению рабочего тела
между сечениями I-I
и II-II.
![]() математическое
выражение 1го закона термодинамики
математическое
выражение 1го закона термодинамики
![]()
![]() ,
где
,
где
![]() удельная
энтальпия.
удельная
энтальпия.
Удельная энтальпия – это функция термических параметров состояния или функция состояния. Она относится к калорическим параметрам состояния и характеризует энергию
термодинамической системы.
![]()
![]()
Рассмотрим процесс в координатах PV

![]()

![]() - удельная
располагаемая работа (внешняя полезная
работа)
- удельная
располагаемая работа (внешняя полезная
работа)
![]()
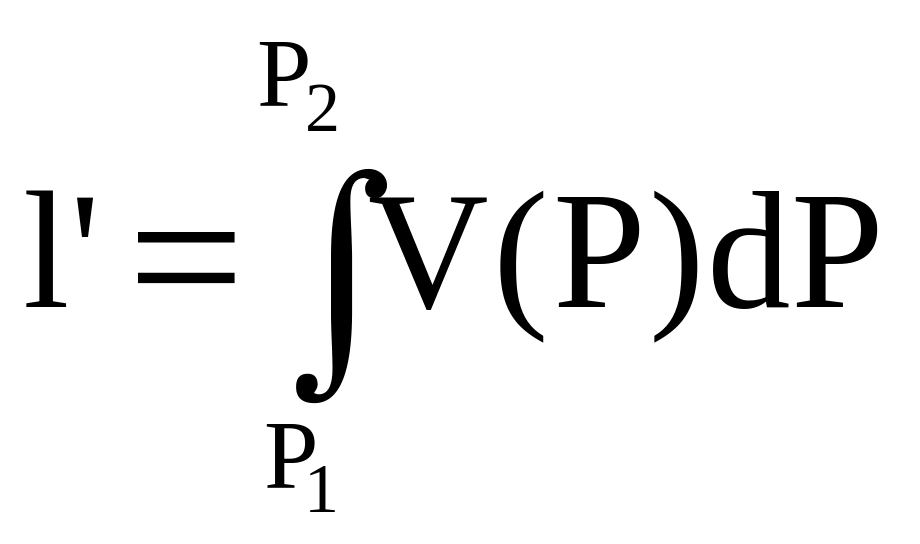 ;
;
![]() ;
;
![]()

d q=dU+dl=dU+p·dV
q=dU+dl=dU+p·dV
 Данная форма записи
– математическое выражение 1го закона
термодинамики называется канонической
Данная форма записи
– математическое выражение 1го закона
термодинамики называется канонической
Пусть 1кг рабочего тела совершает некоторый процесс на участке a-b которого подводится бесконечно малое количество теплоты dQ, при этом P, T, V тела увеличивается соответственно на dP, dT, dV.
При росте Т растёт внутренняя энергия.
dU – сумма изменений внутренней кинетической и потенциальной энергии.
dl – работа системы при изменении объёма на dV.
По закону сохранения энергии запишем dQ=dU+dl
Q=U2-U1+l
Q=ΔU+l
2. Второй закон термодинамики и его математические выражения. Круговые процессы. Цикл Карно (прямой и обратный) и его анализ. Понятие о обобщённом цикле Карно.
1ый закон термодинамики даёт всё необходимое для составления энергобаланса сколь угодно сложной термодинамической системы, однако он не может характеризовать качества энергосистемы.
Например, он не показывает разницы между теплотой и работой. Из опыта известно, что всю работу можно превратить в работу и наоборот тепло нельзя полностью превратить в работу. Ограничение накладывается именно 2м законом термодинамики, который формулируется: все естественные самопроизвольные процессы, протекающие в природе, являются необратимыми. Такими процессами являются процессы теплообмена, процессы смешения газов и жидкостей, движение жидкости под действием перепада высот. Процессы обратные вышеперечисленным возможны, но требуют энергокомпенсации.
К тепловым машинам относят двигатели внутреннего и внешнего сгорания, паровые и газовые турбины, реактивные ракетные двигатели, МТД – генераторы, холодильные машины и тепловые насосы.
Под циклом тепловых машин понимают замкнутый круговой процесс, состоящий из нескольких элементарных процессов в результате осуществления которых рабочее тело возвращается в исходное состояние, а с помощью тепловой машины создаётся полезный энергетический эффект.
Циклы могут быть обратимыми и необратимыми. К необратимым относят цикл, если в нём хотя - бы 1 из процессов является необратимым. Различают циклы прямые и обратные. В прямых циклах направление процесса по часовой стрелке, в обратных – против. По прямым циклам работают тепловые двигатели, по обратным – тепловые насосы.
Рассмотрим произвольный прямой цикл.


1-а-2 – расширение рабочего тела;
2-b-1 – сжатие рабочего тела;
b-1-2 – подвод теплоты в цикле;
a-2-b – отвод тепла.
dq=dU+PdV
![]()
qц – полезная теплота цикла;
lц – полезная работа цикла.

lц=пл.(1-a-2-b-1)
![]()
q1 – удельная подводимая теплота;
q2 – удельная отводимая теплота.
qц=пл.(b-1-a-2-b) lц=qц
Термодинамическое совершенство прямых циклов характеризуется термическим КПД.
![]() ,
т.к.
,
т.к.
![]()
В соответствии со 2м законом термодинамики для реализации цикла тепловой машины необходимо иметь как минимум 2 источника с различными средними температурами. Источник с меньшей средней температурой называют теплоприёмником, с большей - теплоотдатчиком.
Для циклов холодильных машин вводится другой коэффициент.
![]() - характеризует
выработку искусственного холода на
единицу затраченной энергии, на привод
холодильной машины. Чем больше εхол,
темэффективнее работает установка.
εхол
может быть <1 при пуске.
- характеризует
выработку искусственного холода на
единицу затраченной энергии, на привод
холодильной машины. Чем больше εхол,
темэффективнее работает установка.
εхол
может быть <1 при пуске.
Для тепловых насосов (термотрансформаторы)
![]() (2…4)
(2…4)
Цикл Карно и его анализ.
Теоретический цикл Карно.

![]() ηоцк<1,
т.к.
ηоцк<1,
т.к.
![]()
Любой цикл реализуется между 2мя источниками теплоты: горячим и холодным.
ГИТ→Тгит Т1=Тгит-ΔТ1
ХИТ→Тхит Т2=Тхит+ΔТ2
В обратном цикле Карно
ΔТ1→dT1
![]() ΔT2→dT2
ΔT2→dT2
![]()
Для необратимого цикла Карно
![]()
![]()
Термический КПД цикла Карно не зависит от свойств рабочего тела, а определяется лишь температурой горячего и холодного источника теплоты.
Т.к. шкала Кельвина не зависит от свойств термометрической жидкости и в целом от свойств веществ, следовательно, род вещества не определяет КПД.
Обобщённый цикл Карно.
Это цикл, состоящий из 2х изотермических и 2х эквидистантных процессов.
S 2-S1=S3-S4=const
2-S1=S3-S4=const
qрег=пл.(2-3-S3-S2-2)=пл.(1-4-S4-S1-1)
В обобщённом цикле Карно осуществляется внутреннее регенеративное перераспределение энергии в форме теплоты с помощью устройства регенератора. Теплота отводимая в процессе 2-3 в специальном теплообменнике передаётся рабочему телу в процессе 4-1. Теплота регенерации является внутренней теплотой цикла и поэтому не участвует в расчёте термического КПД.
![]()
Этот
цикл называют циклом с предельной
регенерацией теплоты. В реальных
установках, например ГТУ, степень
регенерации![]()
Математическое выражение 2го закона термодинамики.
![]()
Перемещая левую часть в правую, и записав q2 с учётом знака получаем
![]()
Рассмотрим произвольный обратимый цикл.
Р азобьём
площадь адиабатами. При большом числе
разбиений рассматриваемый процесс
можно рассматривать как множество
элементарных циклов Карно.
азобьём
площадь адиабатами. При большом числе
разбиений рассматриваемый процесс
можно рассматривать как множество
элементарных циклов Карно.
![]() Суммируя
по всем элементарным циклам, в пределе
получим:
Суммируя
по всем элементарным циклам, в пределе
получим:
![]()
![]() Первый интеграл
Клаузиуса или математическое выражение
2го закона термодинамики для обратимых
круговых процессов (циклов).
Первый интеграл
Клаузиуса или математическое выражение
2го закона термодинамики для обратимых
круговых процессов (циклов).
Для необратимого цикла Карно можно записать, что термический КПД будет
![]()
Рассматривая произвольный необратимый цикл, путём рассуждений, аналогичных выше рассмотренных для обратимого цикла можно показать, что
![]() или
или
![]() - 2й интеграл Клаузиуса или математическое
выражение 2го закона термодинамики для
необратимого кругового процесса.
- 2й интеграл Клаузиуса или математическое
выражение 2го закона термодинамики для
необратимого кругового процесса.
![]() - объединённое
математическое выражение 2го закона
для цикла.
- объединённое
математическое выражение 2го закона
для цикла.
Получим математическое выражение 2го закона не для круговых процессов.
В озвратим
систему в исходное состояние другим
обратимым процессом (2-b-1).
озвратим
систему в исходное состояние другим
обратимым процессом (2-b-1).

![]() переходя
к бесконечно малым получим:
переходя
к бесконечно малым получим:
![]() - математическое
выражение 2го закона термодинамики для
необратимых процессов. Объединяя это
выражение с аналогичным для обратимого
процесса получим
- математическое
выражение 2го закона термодинамики для
необратимых процессов. Объединяя это
выражение с аналогичным для обратимого
процесса получим
![]() - объединённое математическое выражение
2го закона термодинамики для некруговых
процессов.
- объединённое математическое выражение
2го закона термодинамики для некруговых
процессов.
