
- •1. Предмет химическая технология, ее содержание. Технологические и технико-экономические показатели химического производства.
- •2. Виды и классификация сырья. Подготовка сырья к переработке. Методы обогащения сырья. Безотходная технология.
- •3. Виды и источники энергии, применяемой в химических производствах. Экономия и пути рационального использования энергии и теплоты реакции. Топливно-энергетическая проблема и пути ее решения.
- •4. Использование воды в химической промышленности. Характеристика природной воды. Технология подготовки питьевой воды.
- •5. Технология подготовки промышленной воды. Методы умягчения и обессолевания воды. Очистка сточных вод.
- •12. Катализ. Типы важнейших каталитических процессов. Свойства твердых катализаторов. Промышленные контактные массы и аппараты.
- •13. Сырье сернокислотной промышленности и его комплексное использование. Типы печей для обжига колчедана. Оптимальные условия.
- •14. Контактный способ получения серной кислоты. Технологическая схема. Теоретические основы производства серной кислоты.
- •15. Сорта, свойства и применение серной кислоты. Перспективы развития производства серной кислоты.
- •16. Теоретические основы синтеза аммиака. Устройство колонны синтеза. Схема.
- •17. Синтез аммиака при среднем давлении. Технологическая схема. Пути совершенствования производства аммиака.
- •18. Теоретические основы синтеза азотной кислоты.
- •19. Производство азотной кислоты комбинированным способом. Технологическая схема.
- •20. Прямой синтез концентрированной азотной кислоты. Свойства и применение азотной кислоты.
- •21. Химизация сельского хозяйства. Роль химической промышленности в реализации продовольственной программы.
- •22. Классификация минеральных удобрений. Калийные удобрения. Получение хлорида калия из сильвинита.
- •23. Фосфорные удобрения, их классификация. Производство простого суперфосфата. Схема.
- •24. Концентрированные и сложные фосфорные удобрения. Производство двойного суперфосфата.
- •25. Производство азотных удобрений. Схема синтеза аммиачной селитры.
- •26. Производство карбомида. Техноогическая схема. Свойства и применение карбомида.
- •27. Фосфорная кислота, способы получения, их сравнение.
- •28. Производство кормовых продуктов для животных, микро-бактериальные удобрения.
- •29. Средства защиты растений (ядохимикаты) и стимуляторы роста.
- •31. Черные металлы. Сплавы на основе железа, их классификация и свойства.
- •32. Производства чугуна. Сырье, химические реакции, устройство доменной печи. Пути интенсификации доменного процесса. Технологическая схема производства.
- •33. Производство стали. Мартеновский процесс, кислородно-конверторный процесс и выплавка стали в электропечах. Схема процессов.
- •34. Производство алюминия. Получение глинозема из бокситов, электролиз глинозема. Свойства алюминия и его сплавов. Схема.
- •35. Производство силикатных материалов. Классификация, свойства и назначение, сырье. Типовые процессы технологии силикатов, типы реакторов. Схема. Производство керамики.
- •36. Стекла. Классификация, сырье. Стадии производства, способы фомования.
- •37. Производство портландцемента. Схема.
- •38. Коксование каменных углей. Сырье, устройство коксовой батареии, химизм процесса. Переработка твердого топлива.
- •39. Коксовый газ, его разделение и использование. Переработка прямого коксового газа, сырого бензола, каменноугольной смолы.
24. Концентрированные и сложные фосфорные удобрения. Производство двойного суперфосфата.
Наличие в суперфосфате большого количества гипса и сравнительно небольшого количества Р2О5 делают его невыгодным при дальних перевозках. Более эффективны концентрированные фосфорные удобрения, содержащие 30% и более РзОб. Для их производства необходима фосфорная кислота. Ее получают экстракционным (сернокислотным разложением природных фосфатов) или термическим способом (восстановлением фосфатов до фосфора с последующим его сжиганием и растворением оксида фосфора (V) в воде).
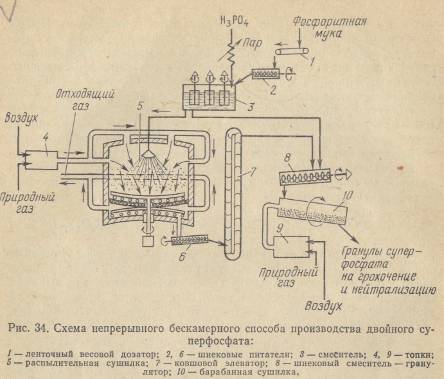
Двойной суперфосфат (название указывает на двукратную обработку фосфата) получают взаимодействием мелкоразмолотoгo фосфата с 62—70-процентной фосфорной кислотой согласно уравнению (2) в рассмотренной ранее камере. Вследствие отсутствия в нем гипса и воды он содержит (после нейтрализации фосфорной кислоты и гранулирования) 42—55% ?2Об. Более экономичен бескамерный способ, при котором можно применять и 40-процентную фосфорную кислоту, а также фосфоритную муку вместо апатита (рис. 34). Из весового дозатора ) (см. стр. 84) мука поступает вместе с кислотой в смеситель 3, а из него часть пульпы стекает в распылительную сушилку 5, обогреваемую продуктами горения из топки 4 с температурой до 700 °С. Здесь быстро протекает реакция (2) и сухой продукт поднимается ковшовым элеватором 7 и вводится вместе с остальной частью пульпы в смеситель-гранулятор 8. Гранулы направляются в барабанную сушилку 10, где реакция заканчивается и происходит высушивание гранул. Производительность установки до 500 т/сут. а/
Частичной нейтрализацией газообразным аммиаком фосфорной кислоты получают аммофос NH4H2PO4 с примесью (NH4)2HPO4 Пульпу направляют в распылительную сушилку, а затем гранулируют и высушивают как двойной суперфосфат. Производительность до 750 т/сут. Аммофос — сложное удобрение и содержит 47—53% Р2О5 и 11 —12% N. Из кислоты можно получить удобрение с общим содержанием питательных элементов 70—80%.
Из термической фосфорной кислоты частичной ее нейтрализацией известковым молоком или мелкоразмолотым известняком осаждают гидрофосфат кальция в виде дигидрата:
Н3РО4 + Са (ОН)2 = СаНРО4 • 2Н2О, Н3РО4 + СаСОз + Н2О = СаНРО4 • 2Н2О + СО2
Пульпу смешивают с готовым продуктом и высушивают. Полученный кормовой преципитат содержит 50—55% РаО5 и применяется в качестве подкормки скоту и птице.
Обесфторенный фосфат образуется при нагревании апатитового концентрата (смоченного водой и с добавлением 2% песка) во вращающейся печи топочными газами до 1450—1550 °С. При этом фторапатит взаимодействует с водяным паром и превращается в гидроксилапатит:
ЗСа3 (РО4)2 -CaF2 + 2Н2О = ЗСа3 (РО4)2 • Са (ОН), + 2HF,
который вступает в реакцию с оксидом кремния и образует силикофосфат:
m [3Ca3 (РО4)2 • СаО] • nSiO2
Он дешев, содержит 26—41% Р2О5 и применяется в первую очередь как кормовой продукт, а также как удобрение, пригодное для всех почв.
Разложение фосфатов азотной кислотой вместо серной имеет большие преимущества, так как вместо сульфата кальция одновременно получается азотное удобрение в виде селитры. Для разложения фосфат смешивают со слабой азотной кислотой, после чего пульпа при 40—50 °С протекает через несколько аппаратов. При этом происходит реакция:
ЗСа3 (РО4)2 • CaF2 + 20HNO3 = 10 Са (NO3)2 + 6H3PO4 + 2HF
(с целью увеличения соотношения между фосфорной кислотой и нитратом кальция азотную кислоту частично заменяют серной или вводят дополнительно фосфорную кислоту). Для образования дигидрофосфата аммония раствор насыщают аммиаком и добавляют в него хлорид калия:
(NH4)2 НРО4 + Са (NO3)2 = СаНРО4 + 2NH4NO3,
КС1 + NH4N03 = KN03 + NH4C1,
после этого пульпу высушивают и одновременно гранулируют в барабане. Таким путем получают полное удобрение — нитрополифосфорной фоску (название получается от соединения слогов в словах: нитрогениум, фосфор и калий), состоящую в основном из дигидрофосфата аммония, нитрата аммония, хлорида аммония, гидрофосфата кальция, нитрата калия и содержащую по 12—16% N, P2О5 и К2O. Вырабатывается также нитрофос без добавления хлорида калия.
Другое сложно-смешанное полное удобрение — нитроаммофоску (по 17% N, Р2О5 и К2О) получают проще — нейтрализацией аммиаком смеси фосфорной и слабой азотной кислоты и выпариванием раствора, как в производстве аммиачной селитры; после добавления хлорида калия плав гранулируют в башне или в барабанном грануляторе. В составе этого удобрения в отличие от нитрофоски отсутствует гидрофосфат кальция.
