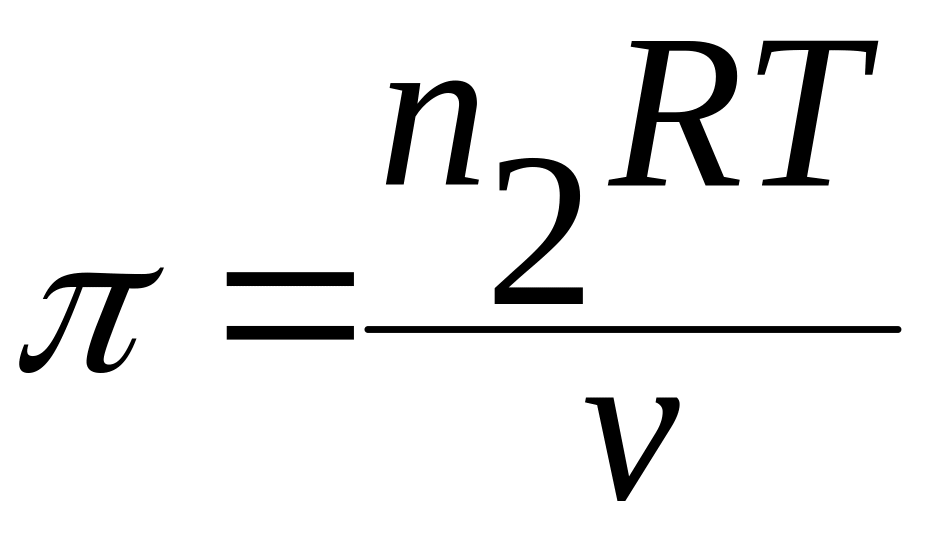- •65. Осмос. Определение осмотического давления и уравнения его вычисления.
- •66. Термодинамический вывод уравнения Вант-Гоффа осмотического давления.
- •67. Связь осмотического давления с понижением давления для разбавленных растворов.
- •68. Термодинамический вывод уравнения, связывающего понижение температуры замерзания с моляльностью.
- •69. Термодинамический вывод уравнения, связывающего повышение температуры кипения раствора с его моляльностью.
- •70. Свойства разбавленных растворов электролитов и методы их вычисления. Изотонический коэффициент.
- •71. Определение молекулярной массы растворенного вещества по понижению температуры замерзания раствора, по повышению температуры кипения раствора и по осмотическому давлению.
65. Осмос. Определение осмотического давления и уравнения его вычисления.
Осмос – это самопроизвольный переход растворителя в раствор через полупроницаемую перегородку. Избыточное давление, которое необходимо приложить к раствору на высоте h = 0, чтобы воспрепятствовать проникновению растворителя в раствор, называют осмотическим давлением. Величина этого давления равна весу столба жидкости в трубке высотою h.
Осмотическое давление может быть рассчитано по выражению
![]()
где ρ- плотность раствора,
g – сила земного притяжения,
h – вес столба жидкости.
Величина осмотического давления зависит от концентрации раствора. Вант-Гофф установил, что осмотическое давление растворов прямолинейно меняется с изменением их концентрации, а произведение их осмотического давления на объём раствора, содержащего 1 моль растворенного вещества, есть величина постоянная и равна
π∙ν = 22,9 Дж/моль
Осмотическое давление равно такому давлению, которое развивало бы растворенное вещество в заданном объёме раствора, если бы оно находилось в идеальном газообразном состоянии и занимало бы объём указанного раствора.
Растворы, обладающие одинаковыми осмотическими давлениями, называют изоосмотическими. Для растворов одинакового объёма осмотическое давление прямо пропорционально температуре:
π/T = const
для разбавленных растворов неэлектролитов: π∙ν/T = R
учитывая, что ν = 1/C, получаем уравнение Вант-Гоффа:
π = cRT
66. Термодинамический вывод уравнения Вант-Гоффа осмотического давления.
Пусть в заданном сосуде давление, развиваемое 1 молем пара от Ро до Р, производит работу за счёт изменения величины потенциальной энергии, которую можно определить по выражению 1-го закона термодинамики при Т=const в таком виде:
dW = - vdp
знак минус определяет затраченную системой работу. Для идеального газа v = RT/p, откуда получим
dW = -RT dp/p
интегрируем в пределах от Ро до Р:
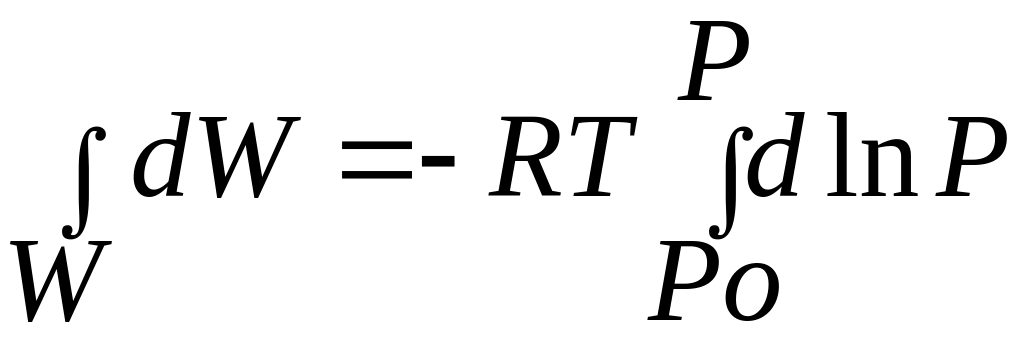 W
= RT
ln
Po
/P
W
= RT
ln
Po
/P
1 моль вещества можно механически перенести на высоту h, затрачивая работу
W = Mgh, где М – молекулярная масса растворителя.
Тогда Mgh = RT ln Po /P
Откуда
h
=

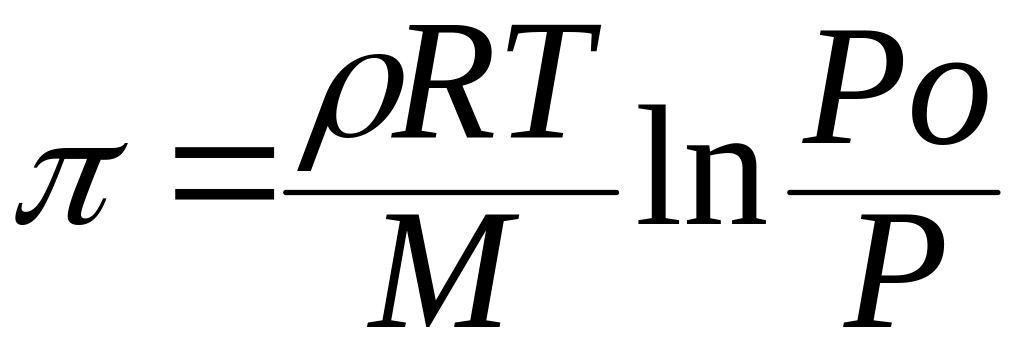
Для разбавленного раствора давление насыщенного пара над чистой жидкостью po = p + ∆p
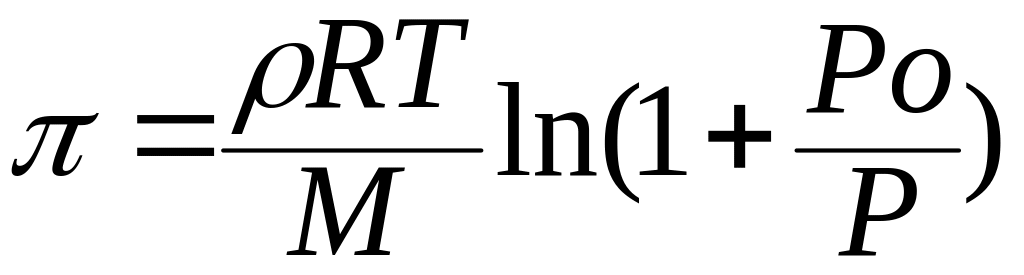
Для разбавленных растворов ∆p/р<<1, тогда
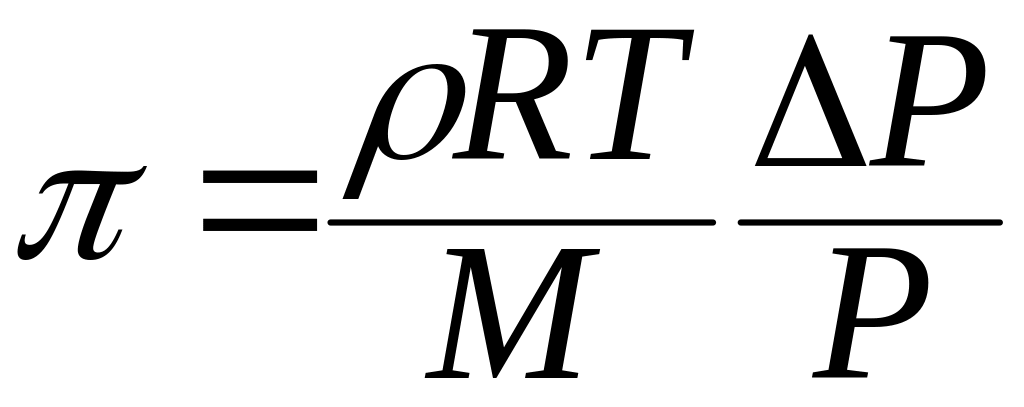
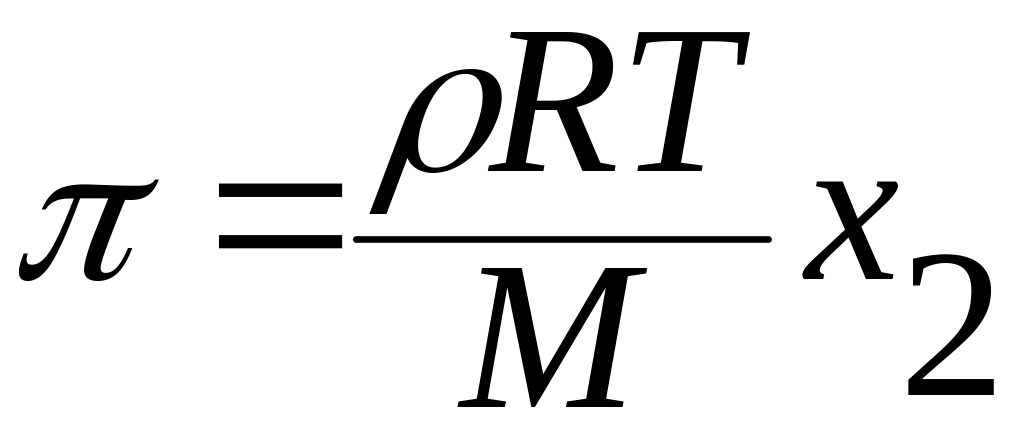
допуская ρ = n1/v и М=М1, получим
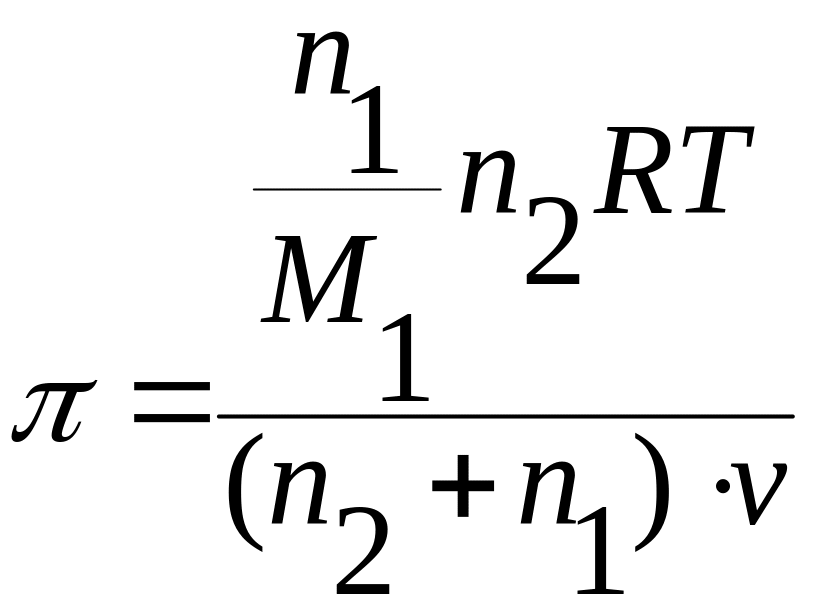 при
n2<<n1
находим
при
n2<<n1
находим