
- •Должность, ученая степень, ученое звание, воинское звание, инициал имени, фамилия автора (авторов)
- •(Номер по тематическому плану изучения дисциплины) по дисциплине: «Биохимия»
- •(Наименование учебной дисциплины)
- •1. Общие принципы регуляции путей метаболизма
- •1.1. Равновесные и неравновесные реакции
- •1.2 Определяющая скорость реакция метаболического пути
- •2. Регуляция метаболизма углеводов
- •Гликолитическая оксидоредукция
- •Обращение гликолиза
- •3. Регуляция глюконеогенеза (обращение гликолиза).
- •4. Регуляция окислительного декарбоксилирования
- •5. Регуляция цикла трикарбоновых кислот
- •6.Пентозофосфатный цикл (гексозомонофосфатный путь метаболизма глюкозы).
- •7. Регуляция процессов синтеза и распада гликогена
- •8. Регуляция концентрации сахара в крови
- •1. Углеводы, содержащиеся в пищевом рационе.
- •3. Гликоген печени
- •9.Механизмы развития гипергликемии и гипогликемии
- •10. Сахарный диабет
2. Регуляция метаболизма углеводов
Главным моносахаридом, подвергающимся окислительным превращениям в клетках, является глюкоза, поскольку именно она в наибольших количествах поступает из кишечника во внутреннюю среду организма, именно она синтезируется при глюконеогенезе или образуется в свободном виде или же в виде фосфорных эфиров при расщеплении гликогена. Роль других моносахаридов менее значительна, так как их количество, поступающее в клетки в количественном отношении сильно варьирует в зависимости от состава пищи [1,6].
Известно несколько метаболических путей окисления глюкозы, главными из которых являются:
а) аэробное расщепление до углекислого газа и воды;
б) анаэробное окисление до лактата;
в) пентозный путь окисления;
г) окисление с образованием глюкуроновой кислоты.
Глубина окислительного расщепления молекулы глюкозы может быть различной: от окисления одной из концевых группировок молекул до карбоксильной группы, что происходит при образовании глюкуроновой кислоты, до полной деградации молекулы глюкозы при ее аэробном распаде [1].
АЭРОБНОЕ ОКИСЛЕНИЕ ГЛЮКОЗЫ
В клетках аэробных организмов основным, по крайней мере в отношении общего количества расщепляющейся глюкозы, является ее
аэробный распад до углекислого газа и воды. При расщеплении 1 М
глюкозы ( 180 г ) в аэробных условиях выделяется 686 ккал свобод-
ной энергии [2]. Сам процесс аэробного окисления глюкозы можно разде-
лить на 3 этапа:
1.Расщепление глюкозы до пирувата.
2.Окислительное декарбоксилирование пирувата до ацетил-КоА.
3.Окисление ацетила в цикле Кребса (ЦТК), сопряженное с работой цепи дыхательных ферментов.
Регуляция работы первого этапа аэробного расщепления глюкозы (гликолиза).
Осуществляется с помощью термодинамических механизмов и с помощью механизмов аллостерической модуляции регуляторных ферментов, принимающих участие в работе этого метаболического пути. С помощью термодинамических механизмов осуществляется контроль направления потока метаболитов по данному метаболическому пути. В описанную систему реакций включены три реакции, в ходе которых теряется большое количество энергии: гексокиназная( G 50 0= - 5,0 ккал/моль ),фосфофруктокиназная ( G 50 0= -3,4 ккал/моль ) ипируваткиназная( G 50 0= - 7,5 ккал/моль )[2]. Эти реакции в клетке практически не обратимы, в особенности пируваткиназная реакция, и за счет их необратимости процесс становится необратимым в целом.
Интенсивность потока метаболитов по рассматриваемому метаболическому пути контролируется в клетке за счет изменения активности включенных в систему аллостерических ферментов: гексокиназы, фосфофруктокиназы и пируваткиназы. Таким образом, пункты термодинамического контроля метаболического пути одновременно являются и участками, на которых осуществляется регуляция интенсивности потока метаболитов. Главным регуляторным звеном системы является фосфофруктокиназа-1.
Фосфофруктокиназа-1
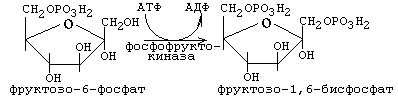
Фосфофруктокиназа (фосфофруктокиназа-1) является еще одним ферментом, регуляция которого осуществляется по принципу обратной связи. Этот фермент играет ключевую роль в регуляции гликолиза.
AMФ.
АМР функционирует как своего рода индикатор энергетического состояния клетки. Благодаря присутствию аденилаткиназы в клетках печени и многих других тканей быстро достигается равновесие в реакции
АТФ+AMФ ↔ 2AДФ
Таким образом, при расходовании АТФ в потребляющих энергию реакциях и образовании AДФ возрастает концентрация AMФ. Поскольку в исходном равновесии концентрация АТФ может в 50 раз превышать концентрацию AMФ, то при сравнительно небольшом уменьшении концентрации АТФ может многократно увеличиться концентрация AMФ. Таким образом, большое увеличение концентрации AMФ действует как своего рода метаболический усилитель при незначительном изменении концентрации ATФ. Данный механизм делает фосфофруктокиназу-1 высокочувствительной к небольшим изменениям энергетического состояния клетки и позволяет регулировать количество углеводов, подвергающихся гликолизу, до их вступления в цикл лимонной кислоты. Увеличение концентрации AMФ позволяет также объяснить, почему процесс гликолиза усиливается при недостатке кислорода, когда концентрация АТФ снижается. Одновременно AMФ активирует фосфорилазу и тем самым усиливает гликогенолиз [2,6,8].
Цитрат
Ингибирование фосфофруктокиназы-1 цитратом и АТФ является еще одним путем, который объясняет тормозящее действие окисления жирных кислот на окисление глюкозы; это ингибирование объясняет также эффект Пастера, заключающийся в том, что аэробное окисление субстратов в цикле лимонной кислоты ингибирует анаэробное расщепление глюкозы. Следствием ингибирования фосфофруктокиназы-1 является также накопление глюкозо-6-фосфата, который снижает поступление глюкозы во внепеченочные ткани путем аллостерического ингибирования гексокиназы [6].
Фруктозо-2,6-бисфосфат
Аллостерический активатор фосфофруктокиназы-1.
Роль фруктозо-2,6-бисфосфата.
В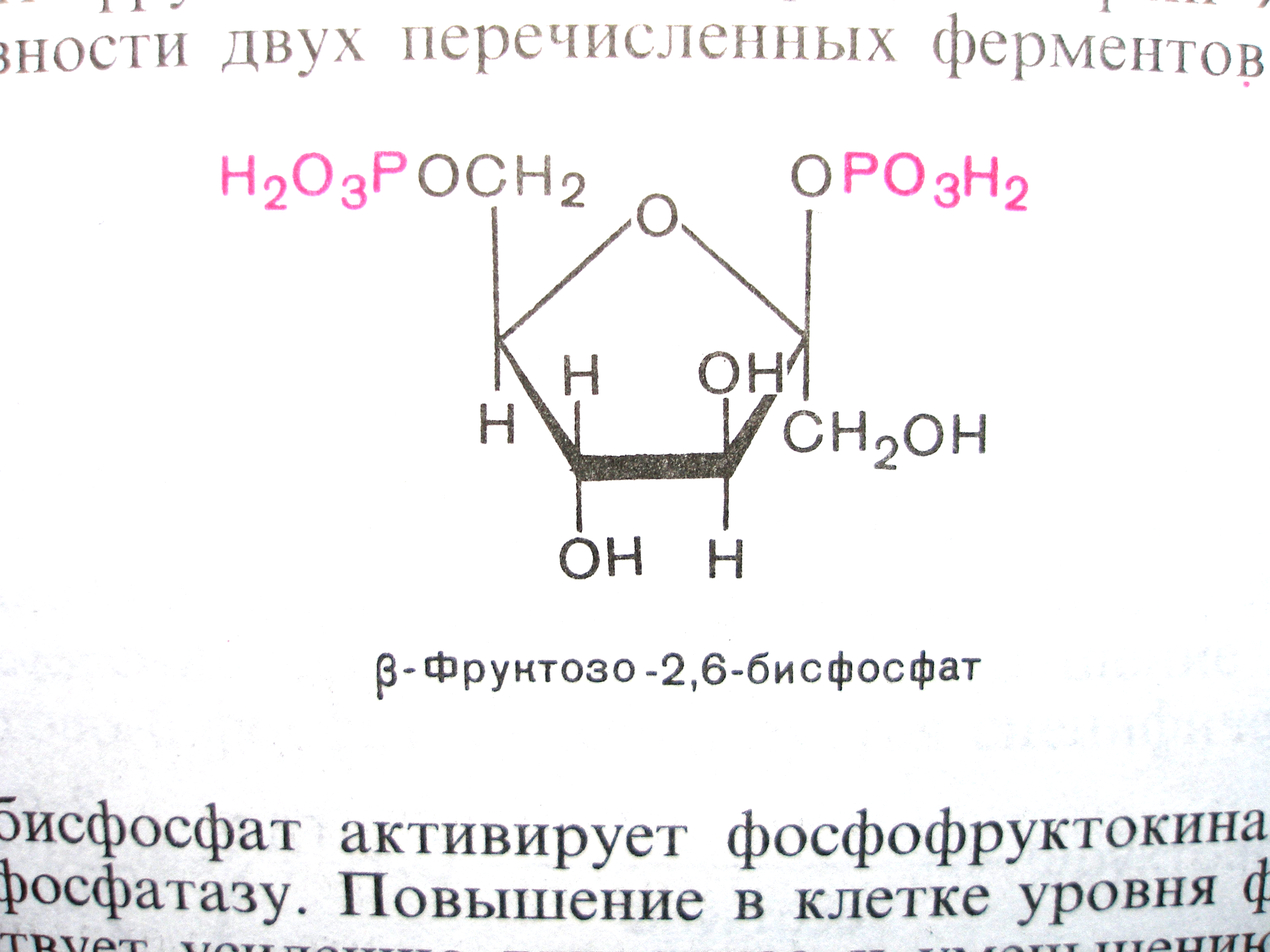 1980 году группой бельгийских исследователей
(Г. Херс и др.) в ткани печени был открыт
фруктозо-2,6-бисфосфат, который являетсянаиболее
мощным аллостерическим
активатором фосфофруктокиназы-1 и
ингибитором фруктозо-1,6-бисфосфатазы
печени является фруктозо-2,6-бисфосфат
[1]. Он
снижает ингибирующее действие АТФ на
фосфофруктокиназу-1 и увеличивает
сродство этого фермента к фруктозо-6-фосфату.
При ингибировании фруктозо-1,6-бисфосфатазы
фруктозо-2,6-бисфосфатом происходит
увеличение Км
для фруктозо-1,6-бисфосфата. Концентрация
фруктозо-2,6-бисфосфата регулируется
концентрацией фруктозо-6-фосфата и
гормонами. Фруктозо-2,6-бисфосфат
образуется при фосфорилировании
фруктозо-6-фосфата, катализируемом
фосфофруктокиназой-2. Этот фермент
является бифункциональным (он
обладает также фруктозо-2,6-бисфосфатазной
активностью) и находится под аллостерическим
контролем фруктозо-6-фосфата (при
повышении концентрации фруктозо-6-фосфата,
наблюдаемой в случае избытка глюкозы,
происходит стимулирование киназной
и ингибирование фосфатазной активности).
Киназная активность проявляется, когда
бифункциональный фермент находится
в дефосфорилированной форме (БИФ-ОН)
[8]. С другой стороны, при
снижении концентрации глюкозы
глюкагон стимулирует образование
цАМФ; последний активирует цАМФ-зависимую
протеинкиназу, которая в свою очередь
ингибирует фосфофруктокиназу-2 и
активирует фруктозо-2,6-бисфосфатазу
путем фосфорилирования. Превращение
фруктозо-2,6-бисфосфата в фруктозо-6-фосфат
не является обратимым процессом.
Образование фруктозо-2,6-бисфосфата
требует затрат АТФ, а при образовании
фруктозо-6-фосфата из
фруктозо-2,6-бисфосфатвысвобождается
неорганический фосфат.
Киназная и фосфатазная
реакции катализируются разными
активными центрами БИФ, но в каждом из
двух состояний фермента -
фосфорилированном и
дефосфорилированном - один из активных
центров ингибирован. Таким
образом, при избытке глюкозы увеличивается
концентрация фруктозо-2,6-бисфосфата,
который активирует фосфофруктокнназу-1
и ингибирует
фруктозо-1,6-6исфосфатазу; в результате
происходит стимулирование гликолиза.
При недостатке глюкозы глюкагон
уменьшает концентрацию фруктозо-2,6-бисфосфата;
это приводит к снижению активности
фосфофруктокиназы-1 и повышению
активности фруктозо-1,6-бисфосфатазы, в
результате чего стимулируется
глюконеогенез.
1980 году группой бельгийских исследователей
(Г. Херс и др.) в ткани печени был открыт
фруктозо-2,6-бисфосфат, который являетсянаиболее
мощным аллостерическим
активатором фосфофруктокиназы-1 и
ингибитором фруктозо-1,6-бисфосфатазы
печени является фруктозо-2,6-бисфосфат
[1]. Он
снижает ингибирующее действие АТФ на
фосфофруктокиназу-1 и увеличивает
сродство этого фермента к фруктозо-6-фосфату.
При ингибировании фруктозо-1,6-бисфосфатазы
фруктозо-2,6-бисфосфатом происходит
увеличение Км
для фруктозо-1,6-бисфосфата. Концентрация
фруктозо-2,6-бисфосфата регулируется
концентрацией фруктозо-6-фосфата и
гормонами. Фруктозо-2,6-бисфосфат
образуется при фосфорилировании
фруктозо-6-фосфата, катализируемом
фосфофруктокиназой-2. Этот фермент
является бифункциональным (он
обладает также фруктозо-2,6-бисфосфатазной
активностью) и находится под аллостерическим
контролем фруктозо-6-фосфата (при
повышении концентрации фруктозо-6-фосфата,
наблюдаемой в случае избытка глюкозы,
происходит стимулирование киназной
и ингибирование фосфатазной активности).
Киназная активность проявляется, когда
бифункциональный фермент находится
в дефосфорилированной форме (БИФ-ОН)
[8]. С другой стороны, при
снижении концентрации глюкозы
глюкагон стимулирует образование
цАМФ; последний активирует цАМФ-зависимую
протеинкиназу, которая в свою очередь
ингибирует фосфофруктокиназу-2 и
активирует фруктозо-2,6-бисфосфатазу
путем фосфорилирования. Превращение
фруктозо-2,6-бисфосфата в фруктозо-6-фосфат
не является обратимым процессом.
Образование фруктозо-2,6-бисфосфата
требует затрат АТФ, а при образовании
фруктозо-6-фосфата из
фруктозо-2,6-бисфосфатвысвобождается
неорганический фосфат.
Киназная и фосфатазная
реакции катализируются разными
активными центрами БИФ, но в каждом из
двух состояний фермента -
фосфорилированном и
дефосфорилированном - один из активных
центров ингибирован. Таким
образом, при избытке глюкозы увеличивается
концентрация фруктозо-2,6-бисфосфата,
который активирует фосфофруктокнназу-1
и ингибирует
фруктозо-1,6-6исфосфатазу; в результате
происходит стимулирование гликолиза.
При недостатке глюкозы глюкагон
уменьшает концентрацию фруктозо-2,6-бисфосфата;
это приводит к снижению активности
фосфофруктокиназы-1 и повышению
активности фруктозо-1,6-бисфосфатазы, в
результате чего стимулируется
глюконеогенез.
Рассмотренный механизм регуляции позволяет понять, каким образом при стимулировании гликогенолиза глюкагоном происходит высвобождение глюкозы и тормозится ее превращение по гликолитическому пути [1].
А ктивность
бифункционального фермента регулируется
также некоторыми метаболитами, среди
которых наибольшее значение имеетглицерол-3-фосфат [1].
Действие глицерол-3-фосфата на фермент
по своей направленности аналогично
эффекту, вызываемому цАМФ-зависимой
протеинкиназой, т.е.
глицерол-3-фосфат
активирует центр фосфатазной активности
бифункционального фермента и ингибирует
центр киназной активности.
ктивность
бифункционального фермента регулируется
также некоторыми метаболитами, среди
которых наибольшее значение имеетглицерол-3-фосфат [1].
Действие глицерол-3-фосфата на фермент
по своей направленности аналогично
эффекту, вызываемому цАМФ-зависимой
протеинкиназой, т.е.
глицерол-3-фосфат
активирует центр фосфатазной активности
бифункционального фермента и ингибирует
центр киназной активности.
В настоящее время фруктозо-2,6-бисфосфат, помимо печени, обнаружен и в других органах и тканях животных, а также у растений и микроорганизмов.В тканях животных бифункциональный фермент представлен четырьмя основными изоферментами: изофермент L-типа (печеночный), Н-типа (сердечный), М-типа (мышечный) и Т-типа (тестикулярный)[2].
Изофермент М-типа не фосфорилируется ни протеинкиназой А, ни протеинкиназой С (ПК С), в то время как Н- и Т-изоферменты фосфорилируются протеинкиназой С. Бифункциональный фермент Н-типа модифицируется также и при участии ПК А, при этом активность фосфофруктокиназы-2 возрастает при фосфорилировании как ПК А, так и ПК С [10]. Исследования последних лет показали, что Н-изофермент может активироваться и при фосфорилировании протеинкиназами, участвующими в передаче сигнала от рецептора инсулина, в частности, протеинкиназой В новой серин/треониновой киназой, которая активируется фосфоинозитол-3-киназой.
Гексокиназа
Э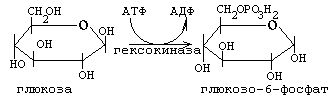 та
реакция катализируется ферментом
гексокиназой . В качестве фосфорилирующего
агента в клетке используется АТФ. Реакция
сопровождается потерей свободной
энергии порядка 5,0 ккал/моль и в условиях
клетки является необратимой. В печени
реакция катализируется глюкокиназой[1].
та
реакция катализируется ферментом
гексокиназой . В качестве фосфорилирующего
агента в клетке используется АТФ. Реакция
сопровождается потерей свободной
энергии порядка 5,0 ккал/моль и в условиях
клетки является необратимой. В печени
реакция катализируется глюкокиназой[1].
Регуляция:
Глюкозо-6-фосфат и АТР
Гексокиназа ингибируется по аллостерическому механизму высокими концентрациями глюкозо-6-фосфата. В этом случае мы имеем делом с работой сопряженного регуляторного механизма. В клетке после угнетения активности фосфофруктокиназы высокими концентрациями АТФ накапливается фруктозо-6-фосфат, а значит накапливается и глюкозо-6-фосфат, поскольку реакция, катализируемая фосфогексоизомеразой, легко обратима. В таком случаеповышение концентрации АТФв клетке ингибирует активность не только фосфофруктокиназы, но и гексокиназы[6].
Инсулин
Инсулин осуществляет медленную гуморальную регуляцию путем индукции транскрипции генов. Увеличивается синтез гексокиназы и происходит ускорение фосфорилирования глюкозы[1,6,10].
Пируваткиназа
Субстратное фосфорилирование. Фосфат переносится на АДФ с образованием АТФ. ФЕП переходит в ПВК (пировиноградную кислоту).

Пируваткиназа , фермент осуществляющий перенос фосфата с фосфоенолпирувата на АДФ, фосфорилированная форма которой неактивна, а дефосфорилированная активна.
Регулирующее влияние на пируваткиназу оказывают:
Инсулин(повышение инсулин/глюкагонового индекса),быстрая гормональная регуляция.
В период пищеварения инсулин активирует протеинфосфатазу, которая дефосфорилирует пируваткиназу, переводя ее в активное состояние. Кроме того, инсулин в печени влияет на количество ферментов, индуцируя синтез пируваткиназы и репрессируя синтез ФЕП-карбоксикиназы. Следовательно, гликолитическая реакция фосфоенолпируват > пируват ускоряется при пищеварении и замедляется в постабсорбтивном состоянии [6,8].
Фруктозо-1,6-бисфосфат
Регулирующее влияние на пируваткиназу оказывает фруктозо-1,6-бисфосфат (гликолитическое направление), который является аллостерическим активатором пируваткиназы. В период пищеварения вследствие ускорения начальных стадий гликолиза концентрация фруктозо-1,6-бисфосфата повышается, что приводит к дополнительной активации пируваткиназы.
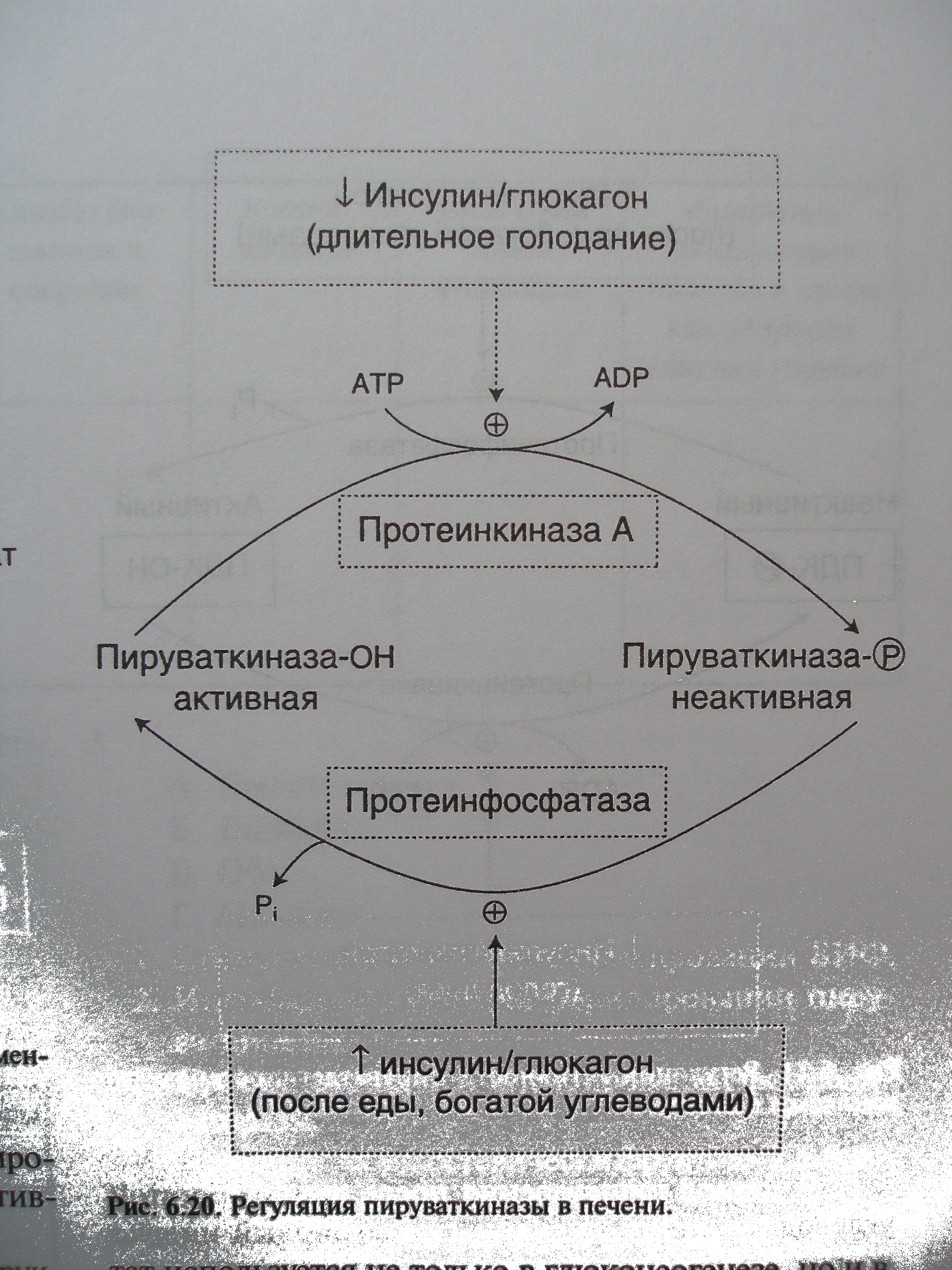
Рис.2Быстрая гормональная регуляция пируваткиназы в печени [8].
Инсулин(повышение инсулин/глюкагонового индекса), медленная гормональная регуляция.
В период пищеварения после приема богатой углеводами пищи инсулин/глюкагоновый индекс возрастает, индуцируется транскрипция генов и увеличивается количество пируваткиназы , а также других гликолитических ферментов: глюкокиназы, фосфофруктокиназы, что стимулирует гликолитический путь [8].
АТФ
АТФ и АМФ являются аллостерическими эффекторами некоторых гликолитических ферментов, в частности АТФ ингибирует пируваткиназу [1].
Активность фермента также стимулируется глюкозо-6-фосфатом и
глицеральдегид-3-фосфатом по аллостерическому механизму - так называя активация предшественником[6].
Высокие внутриклеточные концентрации НАДН2, цитрата, сукцинил-КоА и
жирных кислот угнетают активность
фермента по аллостерическому механизму.
В целом, расщепление глюкозы до пирувата тормозится на уровне 3 указанных киназ при высокой концентрации АТФ в клетке, т.е. в условиях хорошей обеспеченности клетки энергией. При недостатке энергии в клетке активация расщепления глюкозы достигается, во первых, за счет снятия аллостерического ингибирования киназ высокими концентрациями АТФ и аллостерической активации фосфофруктокиназы АМФ и, во-вторых, за счет аллостерической активации пируваткиназы предшественниками: Гл-6-Ф, Фр-1,6-бф и ФГА.
Каков смысл ингибирования цитратом фосфофруктокиназы и цитратом и сукцинил-КоА – пируваткиназы ? Дело в том, что из одной молекулы глюкозы образуется две молекулы ацетил-КоА, который затем окисляется в цикле Кребса. Если в клетке накапливаются цитрат и сукцинил-КоА, значит цикл Кребса не справляется с окислением уже наработанного ацетил-КоА и есть смысл притормозить его дополнительное образование, что и достигается ингибированием фосфофруктокиназы и пируваткиназы. Наконец, угнетение окисления глюкозы на уровне пируваткиназы при повышении концентрации жирных кислот направлено на сбережение глюкозы в клетке в условиях, когда клетка обеспечена другим, более эффективным видом энергетического топлива.
Кроме того, контроль гликолиза осуществляется также ЛДГ и ее изоферментами.
В тканях с аэробным метаболизмом (ткани сердца, почек и др.) преобладают изоферменты ЛДГ1 и ЛДГ2 . Эти изоферменты ингибируются даже небольшими концентрациями пирувата, что препятствует образованию молочной кислоты и способствует более полному окислению пирувата (точнее, ацетил-КоА) в цикле трикарбоновых кислот.
В тканях человека, в значительной степени использующих энергию гликолиза (например, скелетные мышцы), главными изоферментами являются ЛДГ5 и ЛДГ4. Активность ЛДГ5 максимальна при тех концентрациях пирувата, которые ингибируют ЛДГ1. Преобладание изоферментов ЛДГ4 и ЛДГ5 обусловливает интенсивный анаэробный гликолиз с быстрым превращением пирувата в молочную кислоту(гликолитическая оксидоредукция) [1].
