
6.Биосинтез холестерина.
Ещё в 60-х годах нынешнего столетия Блох и сотр. В опытах с использованием ацетата, меченного 14С по метильной и карбоксильной группе, показали, что оба атома углерода уксусной кислоты включаются в холестерин приблизительно в одинаковых количествах. Кроме того, было доказано, что все атомы углерода холестерина происходят из ацетата.
В дальнейшем, благодаря работам Линера, Редней, Поляка, Корнфорта, А.Н.Климова и других исследователей были выяснены основные детали ферментативного синтеза холестерина, насчитывающего более 35 энзиматических реакций. В синтезе холестерина можно выделить три основные стадии: 1-я стадия – превращение активного ацетата в мевалоновую кислоту; 2-я стадия – образование сквалена из мевалоновой кислоты; 3-я стадия – циклизация сквалена в холестерин.
Вначале рассмотрим стадию превращения активного ацетата в мевалоновую кислоту (слайд 9). Начальным этапам синтеза мевалоновой кислоты из ацетил-КоА является образование ацетоацетил-КоА посредством обратимой тиолазной реакции:
CH3-CO-S-KoA + CH3-CO-S-KoA ----→ CH3-CO-CH2-CO-S-KoA + НS-KoA
Ацетил-КоА Ацетил-КоА Ацетоацетил-КоА
Затем последующая конденсация ацетоацетил-КоА с третьей молекулой ацетил-КоА при участии β-гидрокси-β-метилглутарил-КоА-синтетазы (ГМГ-КоА-синтетазы) даёт образование β-гидрокси-β-метилглутарил-КоА:
ГМГ-КоА-синтетазы
CH3-CO-CH2-CO-S-KoA + CH3-CO-S-KoA ---------------------------→
Ацетоацетил-КоА Ацетил-КоА
ОН
|
НООС-СН2-С-СН2-СО- S-KoA
|
СН3
β-гидрокси-β-метилглутарил-КоА
Заметим, что эти первые этапы синтеза мевалоновой кислоты нами уже рассматривались, когда речь шла об образовании кетоновых тел (см. стр.)
Далее β-гидрокси-β-метилглутарил-КоА под влиянием НАДФ-зависимой β-гидрокси-β-метилглутарил-КоА-редуктазы (ГМГ-КоА-редуктазы) в результате восстановления одной из карбоксильных групп и отщепления НS-KoA превращается в мевалоновую кислоту:
ОН
| ГМГ-КоА-редуктаза
НООС-СН2-С-СН2-СО- S-KoA + 2НАДФН2 ---------------------------→
|
СН3
β-гидрокси-β-метилглутарил-КоА
ОН
|
---→ НООС-СН2-С-СН2-СН2ОН + 2НАДФ + НS-KoA
|
СН3
Мевалоновая кислота
ГМГ-КоА-редуктазная реакция – первая практически необратимая реакция в цепи биосинтеза холестерина, и протекает она со значительной потерей свободной энергии (около 8200 ккал). Установлено, что данная реакция является реакцией, лимитирующей скорость биосинтеза холестерина.
Во второй стадии синтеза холестерина мевалоновая кислота превращается в сквален (слайд 10). Реакции второй стадии начинаются с фосфорилирования мевалоновой кислоты с помощью АТФ. В результате образуется 5′-монофосфорный эфир, а затем 5′-пирофосфорный эфир мевалоновой кислоты:
-11-
СООН СООН СООН
| | |
СН2 СН2 СН2
| АТФ АДФ | АТФ АДФ |
Н3С-С-ОН -------------→ Н3С-С-ОН -------------→ Н3С-С-ОН
| | |
СН2 СН2 СН2
| | |
СН2 СН2 СН2
| | |
ОН О О О О
Мевалоновая | || | ||
кислота О-Р-ОН О-Р-ОН
| |
ОН ОН
5′-фосфомевалоновая 5′-пирофосфомевалоновая
кислота кислота
5′-пирофосфомевалоновая кислота в результате последующего фосфорилирования третичной гидроксильной группы образует нестабильный промежуточный продукт - 3′-фосфо-5′-пирофосфомевалоновую кислоту, которая, декарбоксилируясь и теряя фосфорную кислоту, превращается в изопентонилпирофосфат. Последний изомеризуется в диметилаллилпирофосфат:
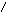

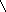 СООН СООН
СН2
СН3
СООН СООН
СН2
СН3
| |
СН2 СН2 С
| АТФ АДФ | Н3РО4 | ←-------------
Н3С-С-ОН -------------→ Н3С-С-ОН -------------→ СН2 -------------→
| | -СО2 |
СН2 СН2 О О О
| | | || ||
СН2 СН2 О-Р-О-Р-ОН
| | | |
О О О О О О ОН ОН
| || || | || || Изопентенил-
О-Р-О-Р-ОН О-Р-О-Р-ОН пирофосфат
| | | |
ОН ОН ОН ОН
5′-пирофосфомевалоновая 3′-фосфо-5′-пирофосфо-
кислота мевалоновая
кислота
СН3 СН3
\ /
СН
|
←-- СН2
 --→
О О
--→
О О
|| ||
О-Р-О-Р-ОН
| |
ОН ОН
Диметилаллилпирофосфат
Затем эти два изомерных изопентенилпирофосфата (диметилаллилпирофосфат и изопентенилпирофосфат) конденсируются с высвобождением пирофосфата и образованием геранилпирофосфата. К геранилпирофосфату вновь присоединяется изопентенилпирофосфат, давая в результате этой реакции фарнезилпирофосфат:
-12-
СН3 О О
Н3С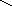 |
|| ||
|
|| ||
С=СН-СН2-СН2-С=СН-СН2-О-Р-О-Р-ОН
Н3С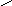 | |
| |
ОН ОН
Геранилпирофосфат
СН3 СН3 О О
Н3С |
| || ||
|
| || ||
С=СН-СН2-СН2-С=СН-СН2-СН2-С=СН-СН2-О-Р-О-Р-ОН
Н3С |
|
|
|
ОН ОН
Фарнезилпирофосфат
В заключительной реакции данной стадии в результате восстановительной конденсации фарнезилпирофосфата с его диметилаллильным изомером образуется сквален:
СН3 СН3 СН3 СН3
| | | |
Н3С-С=СН-СН2-(СН2-С=СН-СН2)2-(СН2-С=СН-СН2)2-СН2-С=С-СН3
Сквален (С30)
На третьей стадии биосинтеза холестерина сквален под влиянием скваленоксидоциклазы циклизирутся с образованием ланостерина. Дальнейший процесс превращения ланостерина в холестерин включает ряд реакций, сопровождающийся удалением трёх метильных групп (слайд 11):































 С Д
С Д































 А В 3СН3
А В 3СН3

 НО НО
НО НО
Ланостерин (С30) Холестерин (С27)
свободный
На четвёртой стадии холестерин вступает во взаимодействие с фосфатидилхолином (или фосфатидилэтаноламином) с помощью фермента ЛХАТ (лецетинхолестеринацетилтрансферазы) (слайд 12). Образуется эфир холестерина и лизофосфолипиды. Чаще всего в эфирную связь с холестерином вступает линолевая кислота (С17Н31СОООН) или линоленовая кислота (С17Н29СООН).
Важно добавить, что образующийся из ацетил-КоА изопентонилпирофосфат представляет собой активированный предшественник, используемый для построения многих биологически важных молекул, содержащих изопреновые единицы. К ним относятся витамины А, Е, К, каротиноиды, боковые цепи хлорофилла и т. д.
-13-
С тероидные
Соли желчных кислот
Витамин Д3
тероидные
Соли желчных кислот
Витамин Д3
 гормоны
гормоны
 Биологические
Биологические
 Холестерин
мембраны
Холестерин
мембраны
Липопротеиды крови
 СН2
СН3
СН2
СН3
Витамин А Каучук
 С
С
|
СН2
В
 итамин
Е |
Фитол
итамин
Е |
Фитол
СН2
|
В
 итамин
К О
итамин
К О
|
К аратиноиды
Р
аратиноиды
Р
|
О Полипренолы
|
Р
Изопентенилпирофосфат
