
- •Лекция № 23 Галогенопроизводные со связью с(sp3)-галоген.
- •Лекция № 24 Галогенопроизводные со связью с(sp3)-галоген.
- •Реакции элиминирования (отщепления)
- •Е2 Элиминирование
- •Е2 Элиминирование
- •Некоторые общие закономерности реакций нуклеофильного замещения и элиминирования:
- •Галогенопроизводные со связью с(sp2)-галоген. Галогеналкены
- •Лекция № 25
- •Галогенопроизводные со связью с(sp2)-галоген. Галогенарены (ароматические галогенопроизводные)
- •Реакции нуклеофильного замещения галогена в ароматическом ряду
- •Механизм присоединения-отщепления
- •Ариновый механизм нуклеофильного замещения
- •Лекция № 26 Металлорганические соединения.
- •Гидроксилсодержащие производные углеводородов и простые эфиры
- •Металлорганические соединения
- •Гидроксилсодержащие производные углеводородов Гидроксилпроизводные со связью с(sp3)-oh (спирты).
- •Лекция № 27 Гидроксилсодержащие производные углеводородов и простые эфиры
- •Гидроксилсодержащие производные углеводородов Гидроксилпроизводные со связью с(sp3)-oh (спирты). Химические свойства
- •Дегидратация спиртов (получение алкенов)
- •Нулеофильное замещение он-группы (получение галогеноалканов)
- •Получение сложных эфиров
- •Получение простых эфиров
- •Окисление
- •Многоатомные спирты
- •Лекция № 28 Гидроксилсодержащие производные углеводородов и простые эфиры
- •Гидроксилсодержащие производные углеводородов Гидроксилпроизводные со связью с(sp2)-oh
- •Получение
- •Химические свойства
- •Образование простых эфиров фенолов
- •Образование сложных эфиров
- •Гидрирование и окисление фенолов
- •Реакции ароматического электрофильного замещения
- •Алкилирование и ацилирование по Фриделю-Крафтсу
- •Карбоксилирование (реакция Кольбе-Шмитта)
- •Формилирование (реакция Раймера-Тимана)
- •Лекция № 29 Простые эфиры.
- •Простые эфиры
- •Получение
- •Химические свойства
- •Тиолы и сульфиды
- •Получение
- •Химические свойства
- •Реакции с электрофилами
- •Окисление и восстановление
- •Лекция № 30 Карбонильные соединения
- •Получение карбонильных соединений
- •Химические свойства альдегидов и кетонов
- •Лекция № 31 Карбонильные соединения
- •Альдегиды и кетоны Химические свойства альдегидов и кетонов Присоединение воды
- •Присоединение спиртов
- •Присоединение тиолов
- •Присоединение синильной кислоты
- •Бисульфитная реакция
- •Реакции присоединения-отщепления
- •Реакции присоединения и отщепления с первичными аминами
- •Конденсация Кневенагеля
- •Полимеризация альдегидов
- •Лекция № 32 Карбонильные соединения
- •Альдегиды и кетоны Химические свойства альдегидов и кетонов Хлорирование
- •Окисление
- •Восстановление
- •Реакция Канниццаро (диспропорционирование)
- •Галогенирование
- •Галоформная реакция
- •Альдольная конденсация (реакция а.П. Бородина)
- •Кротоновая конденсация
- •Конденсация кетонов
- •Перекрестная альдольная и кротоновая конденсации
- •Конденсация Перкина
- •Конденсация Кляйзена-Тищенко
- •Лекция № 33 Карбонильные соединения
Восстановление
Восстановление карбонильных соединений до спиртов было рассмотрено ранее.
Альдегиды и кетоны могут быть восстановлены до углеводородов.

Восстановление может быть выполнено амальгамой цинка в соляной кислоте (по Клеменсену).
К аналогичному результату приводит восстановление гидразином в сильнощелочной среде при высокой температуре (по Кижнеру-Вольфу).
Реакция Канниццаро (диспропорционирование)
Альдегиды, у которых отсутствуют водороды в -положении к карбонильной группе, при действии концентрированной щелочи превращаются в эквимолярную смесь спирта и карбоновой кислоты.
Гидроксид-анион, атакует углерод карбонильной группы с образованием годроксигидроксидного аниона. Последний теряет гидрид-ион (Н-) и превращается в карбоновую кислоту.
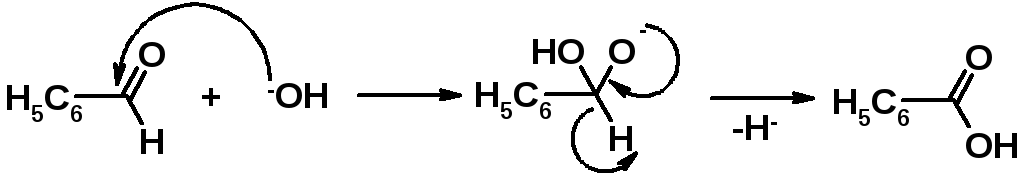
Образовавшийся гидрид-ион атакует другую молекулу альдегида. В результате образуется алкоксид-анион.

Поскольку алкоксидные анионы более сильные основания, чем щелочи, образовавшийся анион отрывает протон от кислоты, образуя в результате первичный спирт. Кислоту, образующуюся в это реакции, выделяют в виде соли.

Реакции анионов карбонильных соединений
Наличие в -положении к карбонильной группе атома водорода создает предпосылки для кето-енольной таутомерии (см. раздел «Алкины»).

Если с карбонильной группой связаны углеводородные радикалы, равновесие всегда сильно сдвинуто в сторону кето-формы. Наличие акцепторных заместителей способно сдвинуть таутомерное равновесие в сторону енольной формы.
Водороды в -положении к карбонильной группе альдегидов и кетонов обладают подвижностью, а соответствующие карбонильные соединения относят к СН-кислотам. Подвижность водорода связанного сsp3-углеродным атомом объясняется двумя факторами:
находящаяся рядом акцепторная карбонильная группа сдвигает к себе электронную плотность связи С-Н, в результате позитивированный водород может быть отдан основанию;

образующийся анион – енолят-анион - стабилизирован за счет сопряжения. Отрицательный заряд распределен по трем атомам (два углерода и кислород).

Енолы и енолят-анионы играют определяющую роль во многих интересных превращениях.
Галогенирование
Водород в в -положении к карбонильной группе может быть легко замещен на атом галогена. Чаще всего используют не хлорирование, а более селективное бромирование. Реакция может быть катализирована как кислотами, так и основаниями и имеет интересную особенность: скорость реакции не зависит от природы галогена. Следовательно: стадия, определяющая скорость реакции (лимитирующая) не включает образование связи углерод-галоген.
Катализ основаниями:

Катализ кислотами:

Ключевая стадия реакции отщепление протона от оксониевого катиона с образованием енола, которая облегчается протонированием карбонильного соединения.
Галоформная реакция
Качественная реакция на метилкетоны и ацетальдегид – обработка карбонильного соединения избытком йода в присутствии щелочи. Выпадение желтого осадка указывает на наличие в исходном соединении метильной группы, связанной с карбонилом. Аналогичные реакции идут с хлором и бромом, но только реакция с йодом с йодом приводит к нерастворимому йодоформу.

