- •Лекция № 23 Галогенопроизводные со связью с(sp3)-галоген.
- •Лекция № 24 Галогенопроизводные со связью с(sp3)-галоген.
- •Реакции элиминирования (отщепления)
- •Е2 Элиминирование
- •Е2 Элиминирование
- •Некоторые общие закономерности реакций нуклеофильного замещения и элиминирования:
- •Галогенопроизводные со связью с(sp2)-галоген. Галогеналкены
- •Лекция № 25
- •Галогенопроизводные со связью с(sp2)-галоген. Галогенарены (ароматические галогенопроизводные)
- •Реакции нуклеофильного замещения галогена в ароматическом ряду
- •Механизм присоединения-отщепления
- •Ариновый механизм нуклеофильного замещения
- •Лекция № 26 Металлорганические соединения.
- •Гидроксилсодержащие производные углеводородов и простые эфиры
- •Металлорганические соединения
- •Гидроксилсодержащие производные углеводородов Гидроксилпроизводные со связью с(sp3)-oh (спирты).
- •Лекция № 27 Гидроксилсодержащие производные углеводородов и простые эфиры
- •Гидроксилсодержащие производные углеводородов Гидроксилпроизводные со связью с(sp3)-oh (спирты). Химические свойства
- •Дегидратация спиртов (получение алкенов)
- •Нулеофильное замещение он-группы (получение галогеноалканов)
- •Получение сложных эфиров
- •Получение простых эфиров
- •Окисление
- •Многоатомные спирты
- •Лекция № 28 Гидроксилсодержащие производные углеводородов и простые эфиры
- •Гидроксилсодержащие производные углеводородов Гидроксилпроизводные со связью с(sp2)-oh
- •Получение
- •Химические свойства
- •Образование простых эфиров фенолов
- •Образование сложных эфиров
- •Гидрирование и окисление фенолов
- •Реакции ароматического электрофильного замещения
- •Алкилирование и ацилирование по Фриделю-Крафтсу
- •Карбоксилирование (реакция Кольбе-Шмитта)
- •Формилирование (реакция Раймера-Тимана)
- •Лекция № 29 Простые эфиры.
- •Простые эфиры
- •Получение
- •Химические свойства
- •Тиолы и сульфиды
- •Получение
- •Химические свойства
- •Реакции с электрофилами
- •Окисление и восстановление
- •Лекция № 30 Карбонильные соединения
- •Получение карбонильных соединений
- •Химические свойства альдегидов и кетонов
- •Лекция № 31 Карбонильные соединения
- •Альдегиды и кетоны Химические свойства альдегидов и кетонов Присоединение воды
- •Присоединение спиртов
- •Присоединение тиолов
- •Присоединение синильной кислоты
- •Бисульфитная реакция
- •Реакции присоединения-отщепления
- •Реакции присоединения и отщепления с первичными аминами
- •Конденсация Кневенагеля
- •Полимеризация альдегидов
- •Лекция № 32 Карбонильные соединения
- •Альдегиды и кетоны Химические свойства альдегидов и кетонов Хлорирование
- •Окисление
- •Восстановление
- •Реакция Канниццаро (диспропорционирование)
- •Галогенирование
- •Галоформная реакция
- •Альдольная конденсация (реакция а.П. Бородина)
- •Кротоновая конденсация
- •Конденсация кетонов
- •Перекрестная альдольная и кротоновая конденсации
- •Конденсация Перкина
- •Конденсация Кляйзена-Тищенко
- •Лекция № 33 Карбонильные соединения
Конденсация Кляйзена-Тищенко

Лекция № 33 Карбонильные соединения
Непредельные карбонильные соединения. Классификация, изомерия, номенклатура. Физические свойства и молекулярная структура кумулированных и сопряженных енонов (строение, сопряжение, распределение электронной плотности), спектральные свойства.
,-Непредельные альдегиды и кетоны. Методы получения: окисление олефинов по аллильному положению и спиртов с гидроксильной группой в аллильном положении, кротоновая конденсация, дегидратация глицерина как метод получения акролеина.
Химические свойства: каталитическое гидрирование, восстановление комплексными гидридами металлов, восстановление металлами в присутствии источников протонов, методы селективного восстановления С=С и С=О связей. Понятие о защитных группах и принципы их синтетического использования. Присоединение воды, спиртов, галогеноводородов, бисульфита натрия, аммиака и аминов, НСN, реактивов Гриньяра. Реакции конденсации с СН-активными соединениями (реакция Михаэля).
Хиноны: методы получения, реакции восстановления и присоединения.
,-Непредельные альдегиды и кетоны
К этой группе относят соединения, в которых двойные связи углерод-кислород и углерод-углерод разделены одной простой С-С связью, т.е. содержат систему сопряженных двойных связей.

Ранее описаны два общих метода получения -непредельных карбонильных соединений:
кротоновая конденсация;
получение -галогенопроизводных с последующем дегидрогалогенированием.
Химические свойства непредельных и карбонильных соединений уже были рассмотрены (см. разделы «Алкены» и «Альдегиды и кетоны»). Следует помнить, что во многих случая для селективного проведения реакции по одной из функциональных групп, вторую необходимо защитить (см. выше).
В этом разделе рассматриваются реакции, характерные именно для ,-непредельных карбонильных соединений.
Электронное строение сопряженного фрагмента:

Четыре -электрона делокализованы на четырех атомах углерода. Ацепторные свойства карбонильной группы приводят к появлению избытка электронной плотности на атоме кислорода и недостатка на-углеродном атоме. Можно предсказать, что такое распределение электронной плотности приведет к дезактивации двойной связи в реакцияхAEи активации в реакцияхAN.
Электрофильное присоединение
Хотя реакции электрофильного присоединения идут формально против «правила Марковникова», ничего необычного в этих превращения нет. Они протекают через наиболее стабильный интермедиат (карбокатион).

Нуклеофильное присоединение
К двойной связи -непредельных карбонильных соединений легко присоединяютсяHCN,NH3и другие нуклеофилы. Реакция идет через наиболее устойчивый промежуточный продукт – енолят-анион. Следует помнить, что присоединение нуклеофила к С-С двойной связи может осложняться реакцией по карбонильной группе.

Реакция -непредельных карбонильных соединений с карбанионами играет важную роль в синтезе полифункциональных веществ и называется реакцией Михаэля. Превращение протекает в присутствии основания и начинается с образования карбаниона (нуклеофила), после чего проходит обычная реакция нуклеофильного присоединения (см. предыдущую схему).

Хиноны
Циклические дикетоны с двумя двойными углерод-углеродными связями и двумя карбонильными группами называются хинонами. Их получают окислением незамещеных или дизамещенных ароматических производных.

Наличие в хинонах сопряженной системы определяет наличие окраски. Так, п-бензохинон окращен в желтый цвет. Соединения этой группы играют заметную роль в процессах жизнедеятельности.
Химические свойства
Хиноны – сильные окислители. Сами хиноны легко восстанавливаются в гидрохиноны.

Типичные реакции – 1,4-присоединение, сопровождаемое ароматизацией.

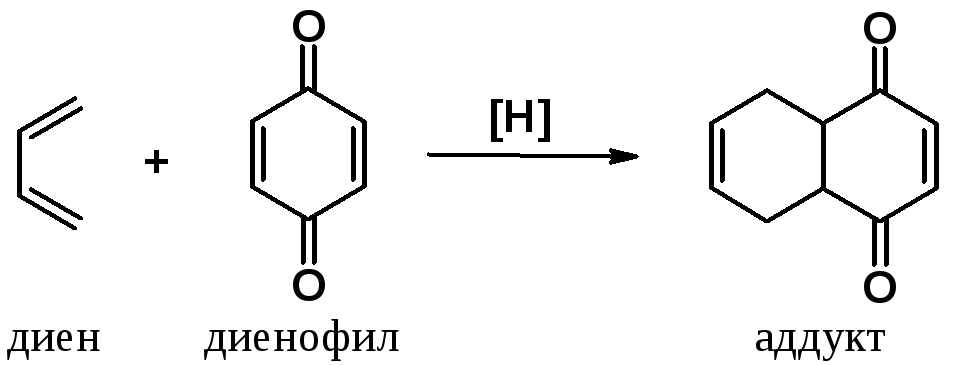
Хиноны – прекрасные диенофилы в реакциях Дильса-Альдера. Эти реакций часто являются первым шагом в синтезе сложных конденсированных полициклических веществ.