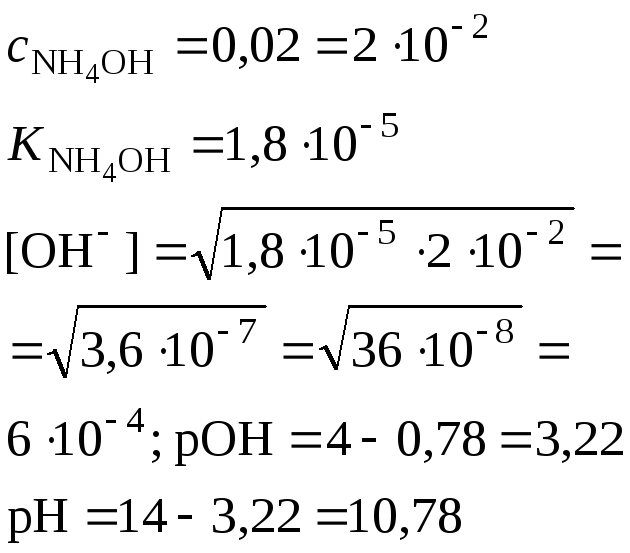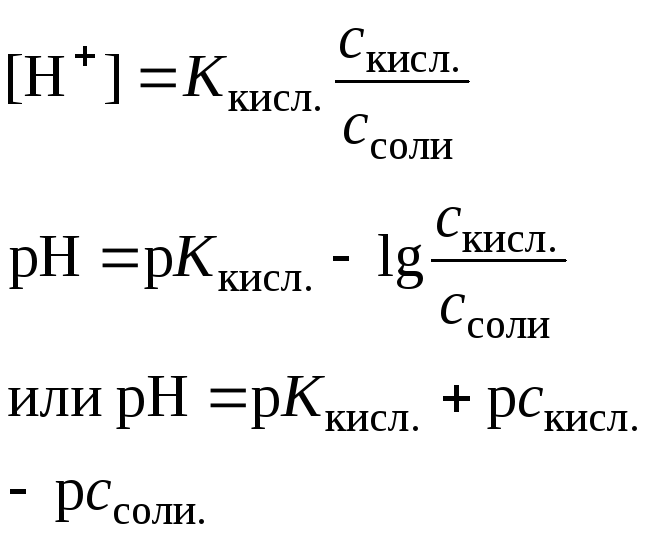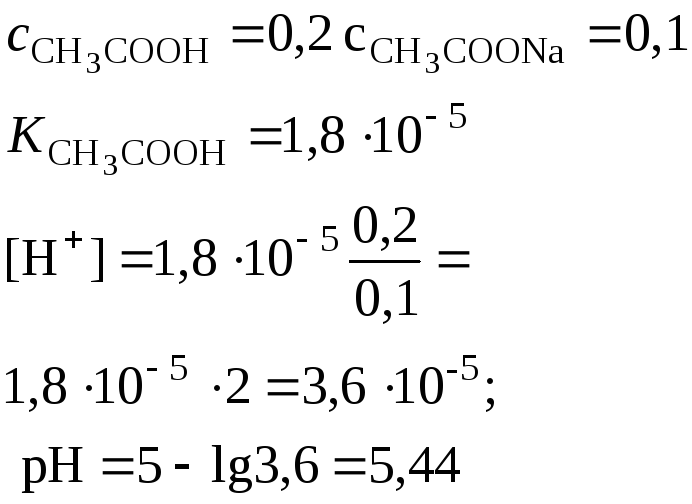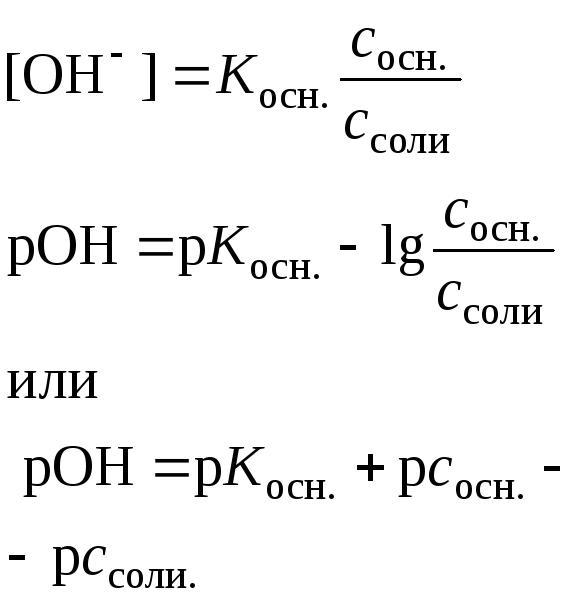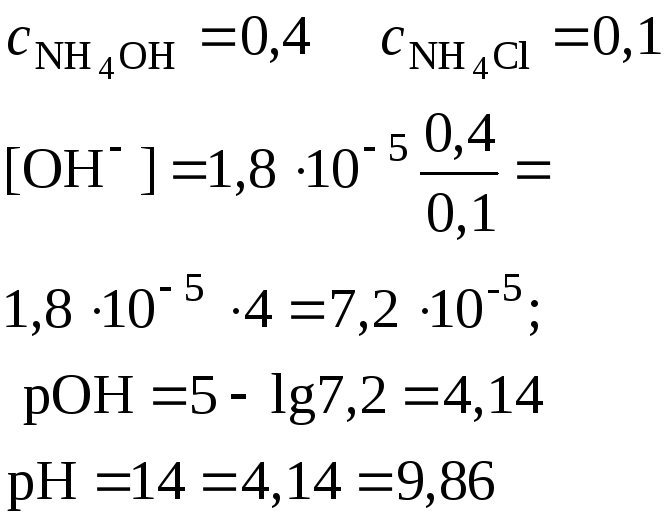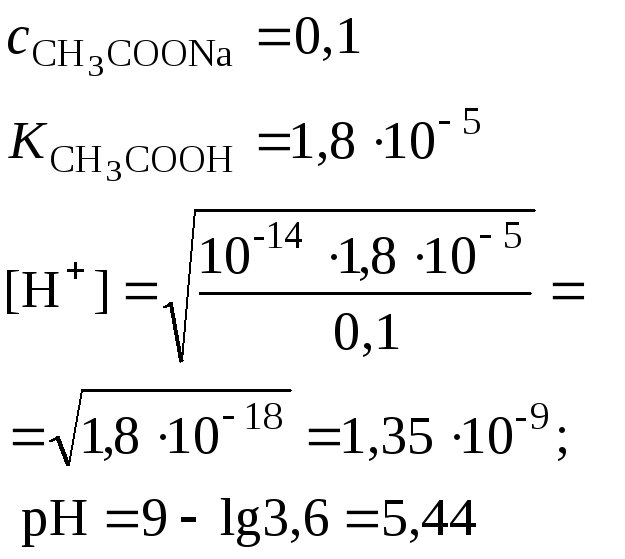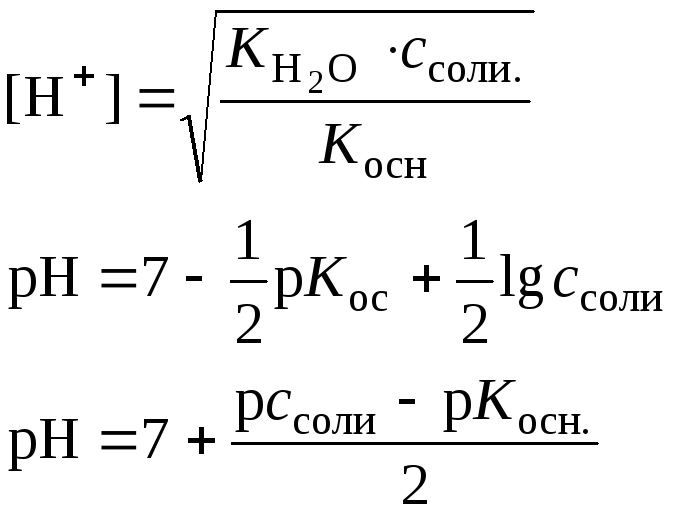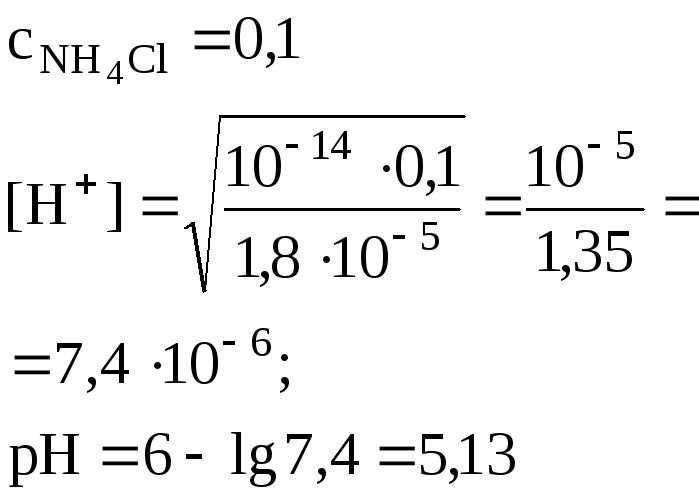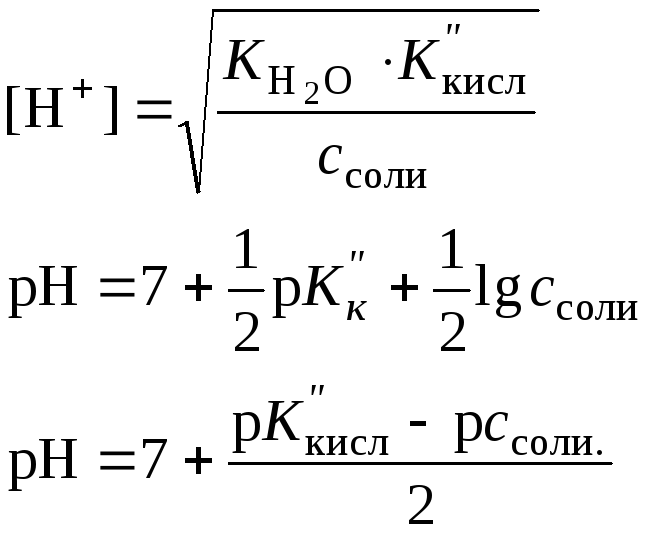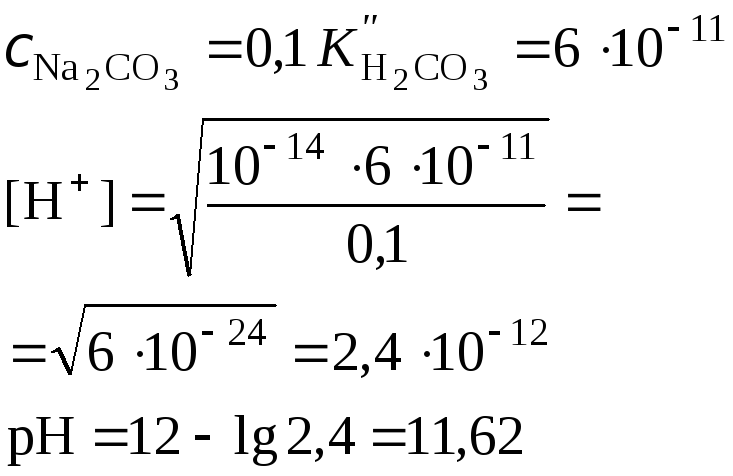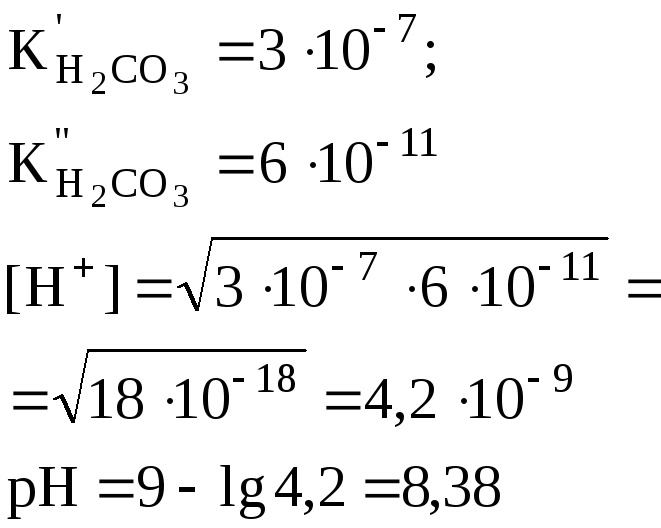- •Министерство образования Российской Федерации
- •Титриметрический (объемный) анализ. Основные понятия
- •Лабораторная работа № 1 Определение содержания Na2co3 и NaHco3 при их совместном присутствии
- •Лабораторная работа № 2 Определение содержания NaОн и Na2co3 при их совместном присутствии
- •Лабораторная работа № 3 Перманганатометрия
- •Определение содержание железа (II)
- •Лабораторная работа № 4 Дихроматометрия
- •Определение содержания железа (II)
- •Лабораторная работа № 5 Иодометрия
- •Определение содержания меди (II)
- •Лабораторная работа № 6 Иодиметрия
- •Определение содержания формальдегида
- •Лабораторная работа № 7 Бромометрия
- •Лабораторная работа № 8 Комплексонометрическое титрование
- •Определение содержания кальция и магния при их совместном присутствии
- •Лабораторная работа № 9 Гравиметрический метод
- •Метод осаждения
- •Определение содержания сульфат-иона
- •Вопросы к коллоквиуму № 1
- •Вопросы к коллоквиуму № 2
- •1. Комплексонометрическое титрование
- •2. Гравиметрический анализ
- •Формулы для вычисления концентрации ионов водорода и значения рН водных растворов кислот, оснований и солей
- •Формулы для вычисления концентрации ионов водорода или гидроксила в разбавленных растворах (без учета ионной силы раствора)
- •Окислительно-восстановительные индикаторы
- •Нормальные окислительно-восстановительные потенциалы (Ео) по отношению к нормальному водородному электроду
- •Численные значения коэффициента Стьюдента
Формулы для вычисления концентрации ионов водорода или гидроксила в разбавленных растворах (без учета ионной силы раствора)
|
Раствор |
Формулы |
Пример |
|
Сильная кислота разбавленная (например, НС1) |
[H+] ≈cкисл. рН = ‑ lgcкисл. |
сHCl= 0,1 моль-экв/л [H+] = 0,1 = 10-1;pH= 1 |
|
Сильная щелочь разбавленная (например, NaOH) |
[OH‾] ≈cосн. рOН = ‑lgcосн. рН = 14 ‑ рОН |
сNaOH = 0,1; OH‾ = 10-1 pOH = 1; pH = 14 ‑ 1 = 13 |
|
Слабая кислота (например, СН3СООН) |
|
|
|
Слабая щелочь (например, NH4OH) |
|
|
|
Слабая кислота в присутствии ее соли (например, СН3СООН+ + СН3СООNa)
|
|
|
|
Слабая щелочь в присутствии ее соли (например, NН4ОН+ + NН4Сl) |
|
|
|
Соль слабой кислоты и сильной щелочи (например, СН3СООNa)
|
|
|
|
Соль слабого основания и сильной кислоты (например, NH4Cl) |
|
|
|
Соль слабой двухосновной кислоты (например, Na2CO3 |
|
|
|
Кислая соль слабой двухосновнойкислоты (например, NaHCO3) |
|
|
Таблица 2
Интервалы перехода окраски кислотно-основных индикаторов
|
Индикатор |
Интервал перехода pH |
рКа |
Показатель титрования pT = рКа |
Окраска | |
|
в кислой среде, молекулярная форма |
в щелочной среде, ионная форма | ||||
|
Тимоловый голубой (1-й переход) |
1,2-2,8 |
1,7 |
2,0 |
Красный |
Желтый |
|
Метиловый оранжевый |
3,2-4,4 |
3,5 |
4,0 |
Красный |
Желтый |
|
Метиловый красный |
4,2-6,2 |
5,0 |
5,5 |
Красный |
Желтый |
|
Феноловый красный |
6,8—8,4 |
8,0 |
7,5 |
Желтый |
Красный |
|
Тимоловый голубой (2-й переход) |
8,0—9,6 |
9,2 |
8,5 |
Желтый |
Голубой |
|
Фенолфталеин |
8,2—10,0 |
9,5 |
9,0 |
Бесцветный |
Красный |
|
Тимолфталеин |
9,4‑10,6 |
9,6 |
10,0 |
Бесцветный |
Синий |
|
Ализариновый желтый |
9,7‑10,8 |
10,1 |
11,0 |
Желтый |
Сиреневый |
Таблица 3
Окислительно-восстановительные индикаторы
|
Индикатор |
Ео, В |
Цвет формы индикатора | |
|
окисленная |
восстановленная | ||
|
Нейтральный красный |
‑ 0,325 (рН 7) 0,240 (рН 0) |
красный |
бесцветный |
|
Индигокармин |
‑ 0,125 (рН 7) 0,291 (рН 0) |
синий |
» |
|
Метиленовая синяя |
0,011(рН 7) 0,532 (рН 0) |
» |
» |
|
Толуиленовый синий |
0,115(рН7) 0,601 (рН 0) |
» |
» |
|
Вариаминовый синий |
0,71 |
фиолетовый |
» |
|
Дифениламин |
0,76 |
» |
бесцветный |
|
Дифенилбензидин |
0,76 |
» |
» |
|
п-Этоксихризоидин |
0,76 |
бледно-желтый |
красный |
|
Дифениламин-4-сульфоновая кислота |
0,84 |
сине- фиолетовый |
бесцветный |
|
N-Фeнилaнтpaнилoвaя кислота |
1,00 |
фиолетовый |
» |
|
Ферроин |
1,06 |
бледно-голубой |
красный |
|
Нитроферроин |
1,25 |
» |
» |
Таблица 4

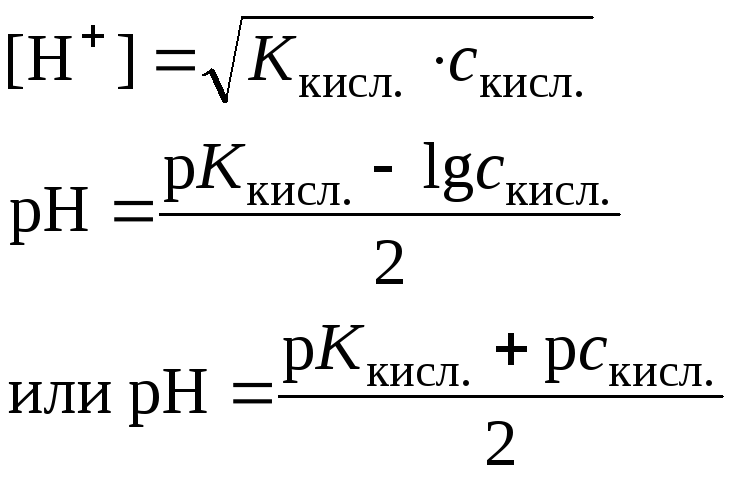
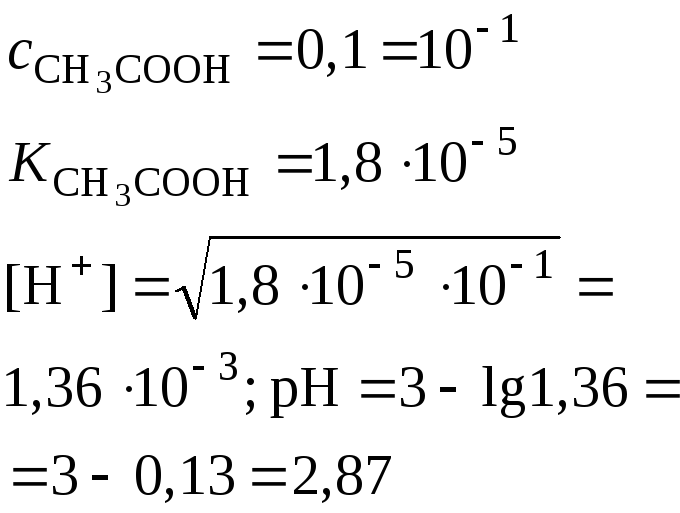
 рН
= 14 ‑ рОН
рН
= 14 ‑ рОН