- •Глава 7. Углеводы
- •7.1. Моносахариды
- •7.1.1. Изомерия, номенклатура
- •7.1.2. Химические свойства
- •7.1.3. Важнейшие представители моносахаридов и их производных
- •7.2. Олигосахариды
- •7.2.1. Классификация и номенклатура дисахаридов
- •7.2.2. Химические свойства дисахаридов
- •7.2.3. Важнейшие представители дисахаридов
- •7.3. Полисахариды
- •7.3.1. Целлюлоза
- •7.3.2. Амилоза и амилопектин
- •7.3.3. Гликоген
- •7.3.4. Декстраны
- •7.3.5. Хитин
- •7.3.6. Пектовая кислота
- •7.3.7. Гетерополисахариды
- •Вопросы и упражнения
Глава 7. Углеводы
Углеводы (или старое название сахарá) можно определить как полигидроксикарбонильные соединения и их производные природного происхождения. Название «углеводы» этим природным веществам было предложено в 1844 г. К. Шмидтом*, так как состав этих известных в то время соединений соответствовал формуле Сn(H2O)m.
Углеводы широко распространены в животном и растительном мире, они играют важную роль во многих жизненных процессах: и как источники энергии, и как структурные компоненты клеточных стенок растений и таких биологически важных веществ, как нуклеиновые кислоты. Углеводы составляют 80% от сухой массы растений и 2% от сухой массы животных организмов.
Все углеводы можно разделить на три группы: 1) моносахариды, 2) олигосахариды и 3) полисахариды. При этом моносахариды относят к простым углеводам, а олигосахариды и полисахариды к сложным.
7.1. Моносахариды
Моносахариды (или монозы) это полигидроксикарбонильные соединения и их производные с непрерывной углеродной цепью. Их молекулы содержат обычно одну карбонильную группу и несколько гидроксильных. Молекулы моносахаридов хиральны, содержат несколько асимметрических атомов углерода. Это определяет существование большого числа оптических изомеров.
В зависимости от характера карбонильной группы моносахариды подразделяют на 1) альдозы соединения, содержащие альдегидную группу, и 2) кетозы соединения, в состав которых входит кетонная группа. Например:

альдоза кетоза
В зависимости от количества атомов углерода в молекуле (от 3 до 10) моносахариды подразделяют на триозы, тетрозы, пентозы, гексозы, гептозы и т. д. Например:
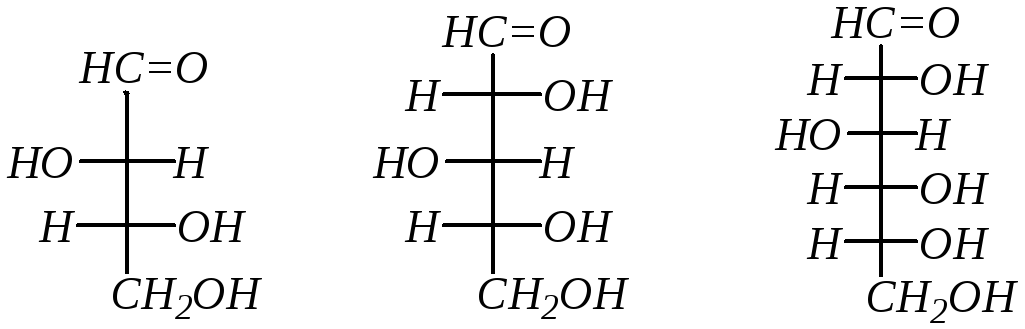
тетроза пентоза гексоза
Таким образом, с учётом классификации по одному и по другому признакам возможны следующие группы моносахаридов: альдотетрозы, альдопентозы, альдогексозы, кетопентозы, кетогексозы и т.д.
Кроме собственно моносахаридов, молекулы которых не содержат других функциональных групп, кроме карбонильной и гидроксильных, и называемых нейтральными сахарами, существуют производные моносахаридов. Наиболее распространёнными среди них являются аминосахара (или, правильнее, аминодезоксисахара), в молекулах которых вместо одной или нескольких гидроксогрупп присутствуют аминогруппы, и кислые сахара, содержащие карбоксильные группы в составе своих молекул.
7.1.1. Изомерия, номенклатура
Как уже было замечено, молекулы моносахаридов содержат асимметрические атомы углерода, с чем связано существование нескольких оптических изомеров. Так, в молекуле единственной альдотриозы – глицеринового альдегида (гл. 1.7.1) один хиральный атом углерода, поэтому возможны только два энантиомера.
Разных изомерных альдотетроз в соответствии с числом хиральных центров возможно уже четыре. Относительная конфигурация моносахаридов определяется по конфигурационному стандарту – глицериновому альдегиду. С конфигурацией его хирального центра сравнивается конфигурация наиболее удалённого от карбонильной группы хирального атома углерода. Каждой альдозе D-ряда соответствует энантиомер (веществоL-ряда) с противоположной конфигурациейвсехцентров хиральности. У диастереомеров в принятой номенклатуре углеводов будут другие тривиальные названия, причём суффикс с окончанием -оза является общим и используется для названий всех моносахаридов:
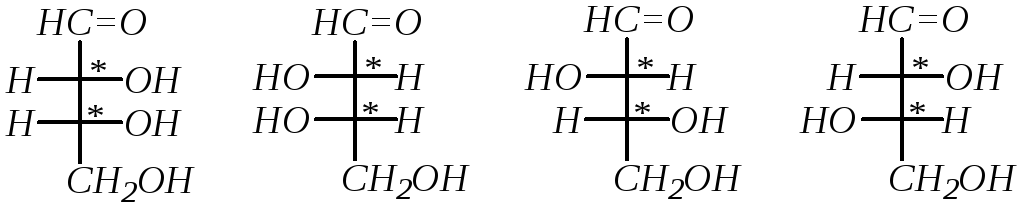
D-эритроза L-эритроза D-треоза L-треоза
Изомерные альдопентозы могут быть представлены следующими формулами Фишера:
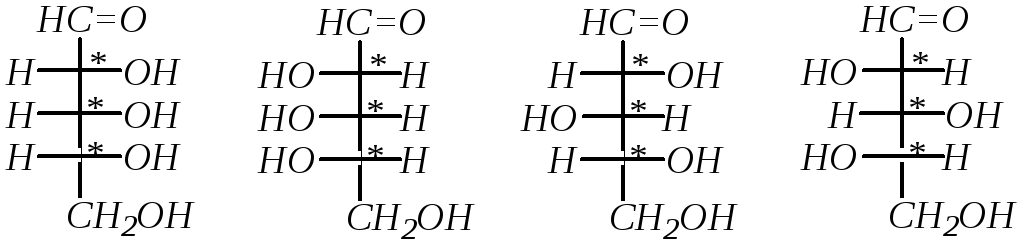
D-рибоза L-рибоза D-ксилоза L-ксилоза
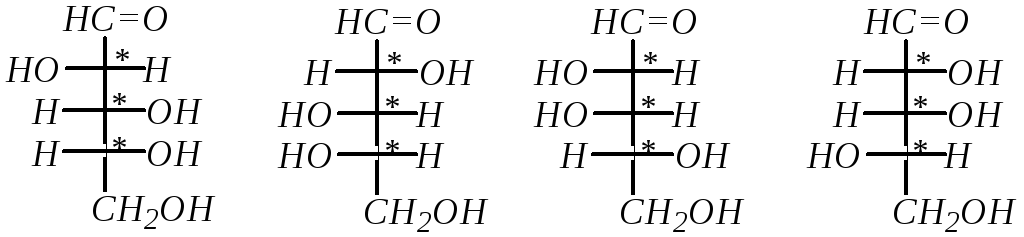
D-арабиноза L-арабиноза D-ликсоза L-ликсоза,
а изомерных альдогексоз будет ещё в 2 раза больше (здесь приведены только соединения D-стереохимического ряда):
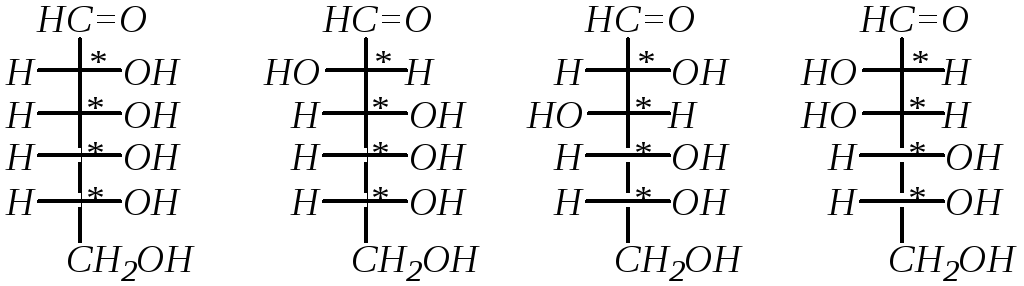
D-аллоза D-альтроза D-глюкоза D-манноза
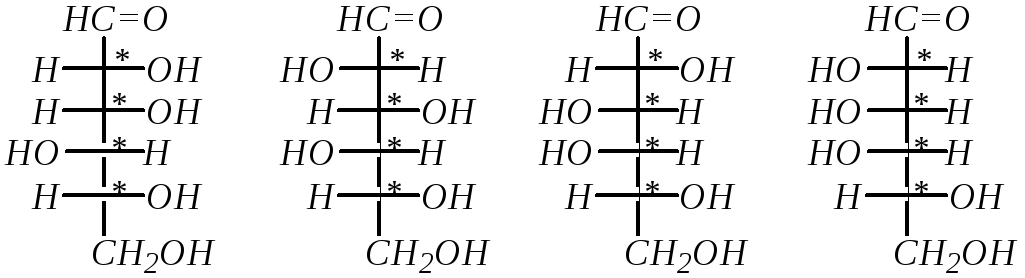
D-гулоза D-идоза D-галактоза D-талоза
Из кетоз наиболее широко распространены фруктоза и сорбоза:
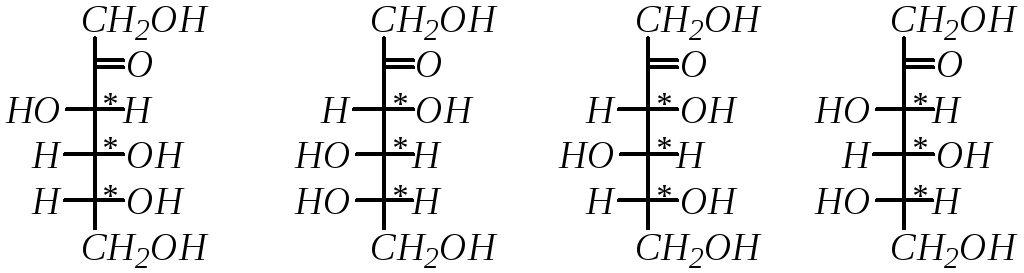
D-фруктоза L-фруктоза D-сорбоза L-сорбоза
Диастереомеры, различающиеся конфигурацией только одного асимметрического атома углерода, называются эпимерами. Эпимеры частный случай диастереомеров. Например, эпимерами являются D-рибоза и D-ксилоза, отличающиеся друг от друга только конфигурацией атома С3, а также D-глюкоза и D-манноза, различающиеся конфигурацией атома С2, и D-глюкоза и D-галактоза, различающиеся конфигурацией атома С4.
Так как по химической структуре альдопентозы, альдогексозы, кетогексозы являются одновременно -гидрокси- и -гидроксикарбонильными соединениями, то они должны легко образовывать циклические полуацетали. Например, для D-рибозы:
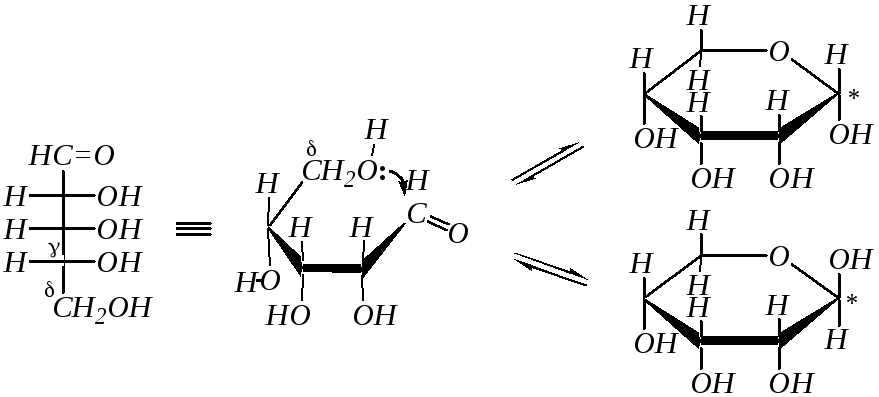
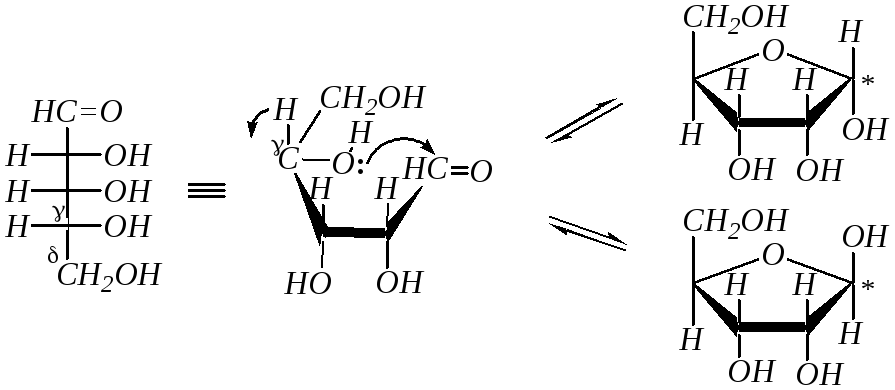
В результате этого образуются четыре циклических формы, что связано с появлением ещё одного хирального центра (атома углерода, связанного с полуацетальным гидроксилом — в схеме отмечен звёздочкой). Полуацетальную гидроксильную группу в химии углеводов называют также гликозидной. Для изображения циклических форм моносахаридов приняты перспективные (пространственные) формулы, предложенные У. Хеуорсом* в 1926 г. (как показано в схеме).
При построении формул Хеуорса цикл условно считают плоским (на самом деле шестичленный цикл может быть в конформации «кресла» или «ванны») и проецируют на плоскость под некоторым углом; при этом ближняя к наблюдателю часть кольца располагается снизу и обычно выделяется более жирной линией. Кислородный атом цикла располагают обычно на наибольшем удалении от наблюдателя. Атомы и группы атомов, изображаемые в формулах Фишера слева и справа, в формулах Хеуорса располагаются соответственно над и под плоскостью цикла. Боковые цепи при атомах С4 в альдопентозах и кетогексозах или С5 в альдогексозах изображают над плоскостью при D-конфигурации атома углерода и под плоскостью при L-конфигурации.
Образование циклического полуацеталя это пример таутомерного превращения. Такое явление в химии углеводов называется цикло-оксотаутомерией или кольчато-цепной таутомерией (о таутомерии — в гл. 3.8.2.1). В зависимости от того, за счёт какой гидроксильной группы (- или -) образуется та или иная циклическая форма, возможно существование пиранозных и фуранозных циклических форм, которые можно рассматривать как производные соответствующих гетероциклов пирана и фурана:
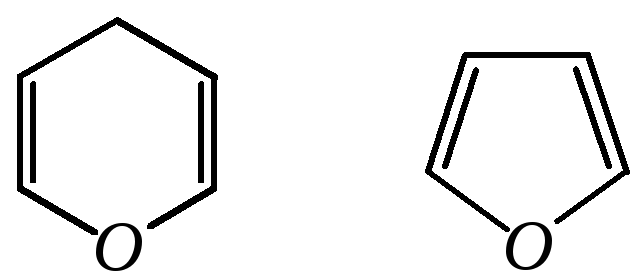
пиран фуран
Образование пяти- и шестичленных циклов связано с их термодинамической устойчивостью по сравнению с малыми циклами (трёх- и четырёхчленными) и циклами большего размера.
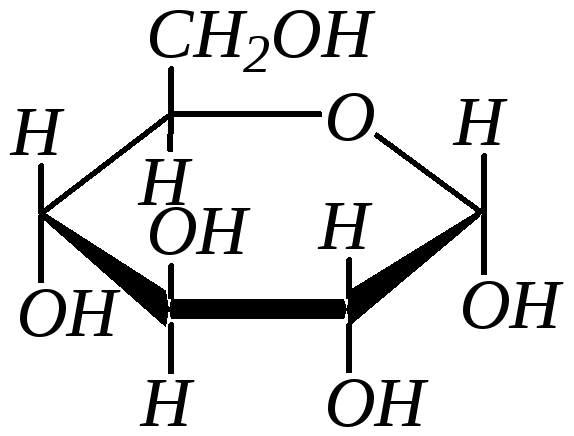
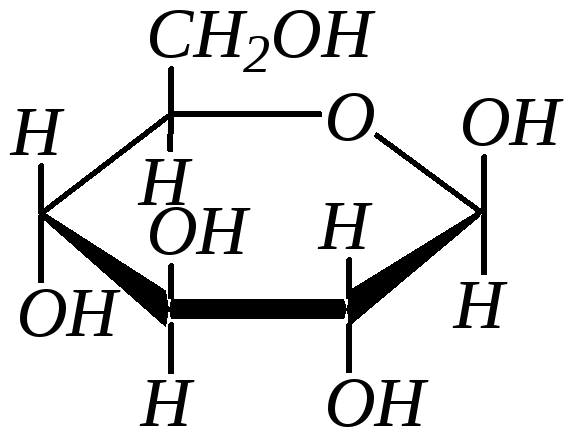
В зависимости от расположения гликозидной (полуацетальной) гидроксильной группы относительно усреднённой плоскости кольца возможна дополнительная пара оптических изомеров, называемых аномерами (-аномер и -аномер). Аномеры представляют собой частный случай эпимеров. Принадлежность к - или -форме определяется конфигурацией аномерного атома углерода (для альдоз – это С1, для кетоз – это, как правило, С2). В молекуле -аномера относительные конфигурации аномерного атома углерода и последнего асимметрического атома в углеродной цепи совпадают. В молекуле -аномера, наоборот, не совпадают. Или иначе принадлежность к - или -форме в формулах Хеуорса можно определить, сравнивая взаимное положение полуацетального гидроксила и группы атомов, не входящих в цикл (часто это СН2ОН-группа). Цис-расположение этих групп определяет -форму, транс-расположение -форму. Например, D-глюкоза существует в следующих пяти формах:
|
-аномер |
|
-аномер |
|
-аномер |
-аномер |
Полное название моносахарида включает обозначение конфигурации аномерного атома углерода (- или -) и размера цикла (пиранозный или фуранозный). Например:
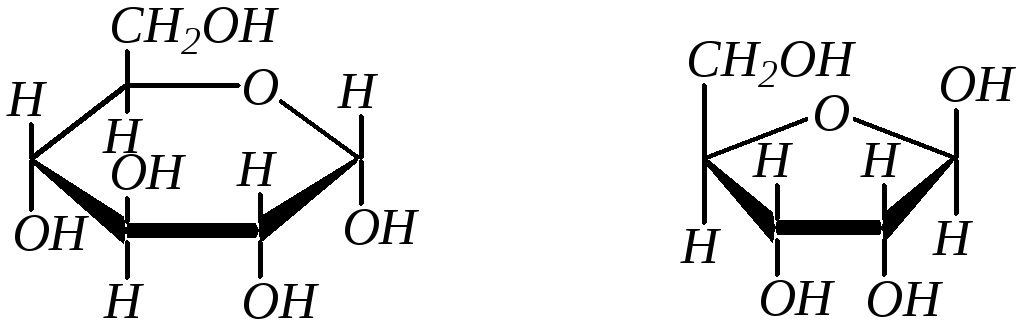
,D-глюкопираноза ,D-рибофураноза
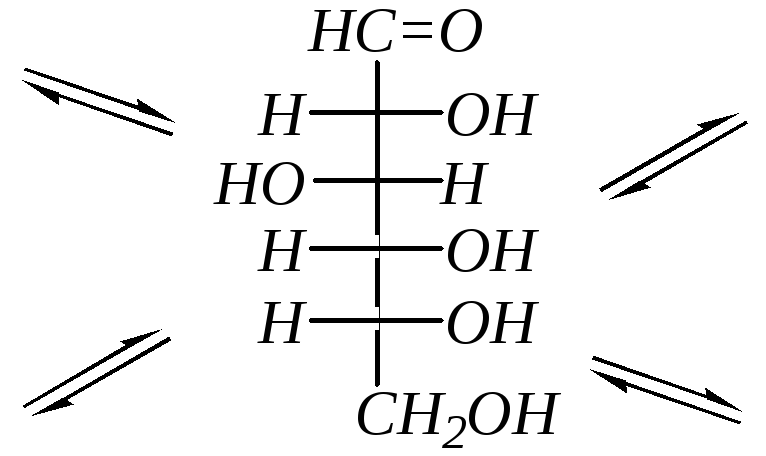
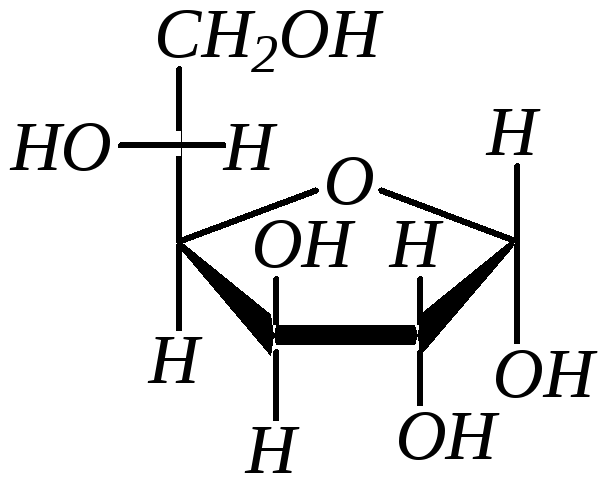
Для кетоз образование циклических форм происходит аналогично альдозам. Например, фуранозные формы фруктозы:
|
D-фруктоза |
,D-фруктофураноза
|
|
,D-фруктофураноза |
В твёрдом состоянии все моносахариды находятся преимущественно в пиранозной форме, как самой устойчивой из возможных циклических форм. При кристаллизации из чистого растворителя можно получить чистые препараты - и -аномеров, так при перекристаллизации D-глюкозы из спирта получают ,D-глюкопиранозу, а из пиридина — ,D-глюкопиранозу. Разные аномеры (- и -) D-глюкозы различаются величиной удельного вращения: у -аномера +112, у -аномера +19. У свежеприготовленного раствора каждого аномера со временем происходит изменение удельного вращения до некоторого постоянного значения. В растворах образуется равновесная смесь всех циклических форм и оксоформы. Для водных растворов D-глюкозы этот угол +52,5. Это происходит вследствие аномеризации, т.е. взаимопревращения - и -аномеров друг в друга через промежуточную оксоформу, и установления таутомерного равновесия. Связанное с этим явлением изменение угла вращения плоскости поляризованного света называется мутаротацией.
Различные конформации циклических форм моносахаридов можно рассматривать только для пиранозных циклов (фуранозное кольцо, аналогичное циклопентановому, почти плоское, и энергии конформационных переходов здесь минимальны). Пиранозное кольцо аналогично циклогексановому, для которого термодинамически более устойчива конформация «кресла». В целом на термодинамическую устойчивость пиранозных форм моносахаридов влияет пространственное расположение громоздких функциональных групп. С этим связано образование в большем или меньшем количестве того или иного аномера. Так, например, ,D-глюкопираноза моносахарид с полным экваториальным расположением заместителей:
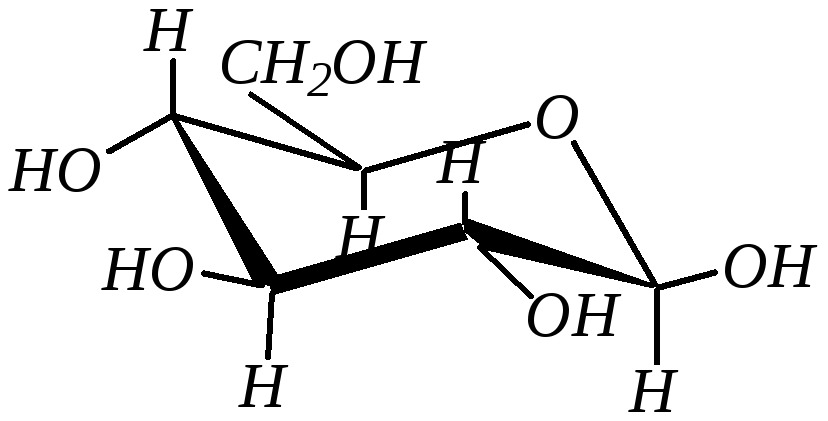
Поэтому, как считается, из-за высокой термодинамической устойчивости она обладает широкой распространённостью в природе.
Однако во многих случаях при оценке термодинамической устойчивости молекул моносахаридов для объяснения преобладания - или -аномерных форм и вообще распространённости в природе тех или иных моносахаридов необходимо учитывать возможность образования водородных связей, как внутримолекулярных, так и межмолекулярных.