- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.1. Номенклатура диазосоединений
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.8.1. Изомерия, номенклатура
- •10.8.2. Строение бензальдегида
- •10.8.3. Физические и химические свойства
- •10.8.4. Способы получения
- •10.8.5. Важнейшие представители
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.9.1. Классификация, номенклатура
- •10.9.2. Строение бензойной кислоты
- •10.9.3. Физические и химические свойства
- •10.9.4. Способы получения
- •10.9.5. Важнейшие представители
- •10.10. Физиологическая роль функциональных производных бензола
- •Вопросы и упражнения
Глава 10. Функциональные производные углеводородов ряда бензола
В этой главе рассматриваются соединения, содержащие одну или несколько функциональных групп. Такими группами могут быть атомы галогенов (-F, -Cl, -Br, -I), сульфо- (-SO3H), нитро- (-NO2), аминогруппы (-NH2), гидроксильная и алкоксильная группы (-OH, -OR), карбонильная и карбоксильная группы (-COR, -COOH) и другие.
Общую формулу монозамещённых бензолов можно представить в следующем виде:
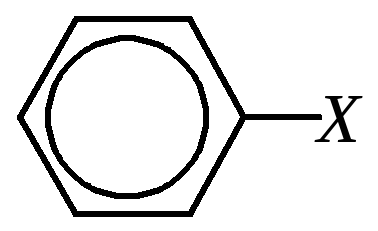
Однако в общем случае молекулы ароматических углеводородов могут содержать функциональные группы как в ароматическом кольце, так и в боковой алифатической цепи. Такие вещества, проявляющие свойства и ароматических соединений, и алифатических производных, также будут рассмотрены в этой главе.
10.1. Общность строения и свойств монозамещённых бензолов
В молекулах монозамещённых бензолов атом углерода ароматического кольца связан с одним из атомов функциональной группы. Несмотря на то, что эти атомы функциональных групп отличаются друг от друга по своей природе, заместители в целом проявляют как индуктивный, так и мезомерный эффект по отношению к бензольному кольцу. Поэтому в распределении электронной плотности в молекулах монозамещённых бензолов и в реакционной способности этих веществ можно отметить много общего.
10.1.1. Электронные эффекты заместителей
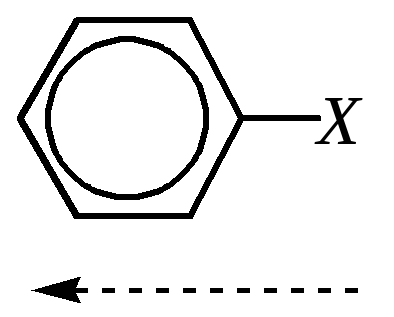
Индуктивный эффект таких заместителей, как галогены, аминогруппа, гидроксильная и другие группы, будет действовать в направлении понижения электронной плотности ароматической системы, поскольку атомы, непосредственно связанные с кольцом, в этом случае более электроотрицательны, чем углерод, с которым они связаны:
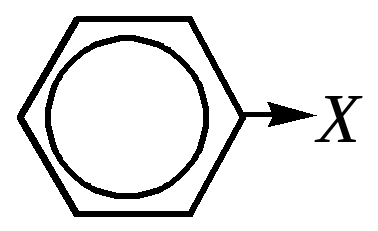
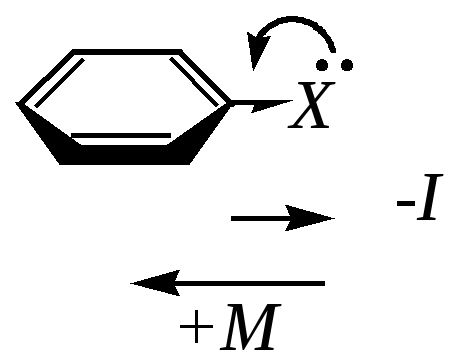
С другой стороны, непосредственно связанные с кольцом атомы таких элементов, как галогены, кислород или азот, содержат неподелённые пары электронов, которые могут взаимодействовать с делокализованными -электронами кольца, в результате чего возникает сопряжение -электронной системы ароматического фрагмента с р-орбиталью первого атома заместителя:
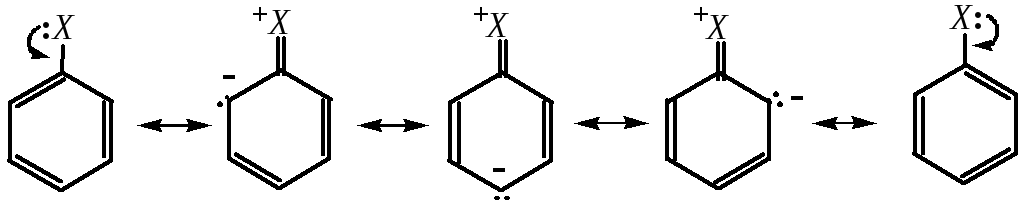
Для заместителей -OH, -OR, -NH2, -NR2 и т.д. величина электронодонорного мезомерного эффекта больше (по модулю) значения акцепторного индуктивного эффекта. Электронная плотность на кольце при этом возрастает. Такие заместители являются в целом электронодонорами.
|
|
+M > -I |
|
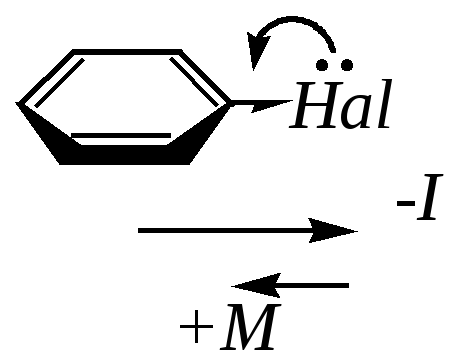
Атомы галогенов, проявляющие такие же по направлению индуктивный и мезомерный эффекты по отношению к бензольному кольцу, напротив, являются в целом электроноакцепторами за счёт бóльшего (по модулю) индуктивного эффекта по сравнению с мезомерным:
|
|
+M < -I |
|
Причины такого влияния атомов галогенов на бензольное кольцо изложены далее (гл. 10.2.2).
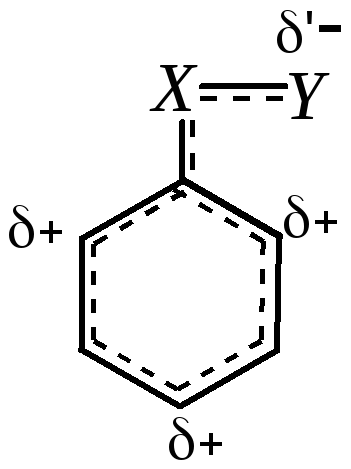
Однако если атом в заместителе, непосредственно соединённый с кольцом, связан кратной связью с ещё более электроотрицательным атомом, возникает сопряжение, приводящее к уменьшению электронной плотности кольца:
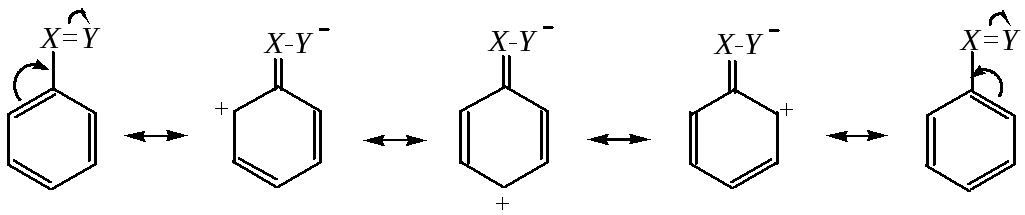
Это характерно для таких заместителей, как -СHO, -COOH, -SO3H, -CN, -NO2 и т.д. Индуктивный эффект, проявляемый этими заместителями, — тоже акцепторный. Такие заместители являются в целом электроноакцепторами. Электронная плотность на кольце в целом понижается:
|
|
|
|
Таким образом, все заместители в бензольном кольце условно можно разделить на две большие группы: электронодоноры и электроноакцепторы.
К донорным заместителям относятся и алкильные радикалы в молекулах аренов (гл. 9.3). Но величина суммарного донорного эффекта (индуктивный эффект и эффект сверхсопряжения, как, например, в толуоле) невелика по сравнению с электронодонорным мезомерным эффектом, обусловленным р--сопряжением таких групп, как -OH, -NH2 и др.
Таким образом, в порядке уменьшения суммарного электронного эффекта электронодоноры можно расположить в следующий ряд (приведены некоторые, наиболее типичные заместители):
-NH2 (-NHR, -NR2) > -OH (-OR) > -NHCOR > -R > -C6H5 > -CH2COOH
Электроноакцепторные заместители также по-разному влияют на ароматическое кольцо, уменьшая электронную плотность на нём в разной степени. По силе акцепторного влияния такие заместители в бензольном кольце можно выстроить в следующий ряд:
-NR3+ > -NO2 > -CN > -SO3H > -CHO > -CRO > -COOH > -COOR > -CONH2
У галогенов, как акцепторных заместителей, имеются свои особенности влияния на распределение электронной плотности бензольного кольца, и в общий ряд акцепторов поэтому они не включены.
Относительную силу влияния заместителей можно ориентировочно определить по величине дипольного момента ароматического соединения, содержащего этот заместитель (табл. 10.1).
Таблица 10.1
Направление и величины дипольных моментов некоторых монозамещённых бензолов
|
Заместитель X |
Дипольный момент , D |
Направление диполя |
|
-N(СH3)2 |
1.6 |
|
|
-OH |
1.6 | |
|
-NH2 |
1.5 | |
|
-OCH3 |
1.2 | |
|
-CH3 |
0.3 | |
|
H |
0 |
|
|
-COOH |
1.0 |
|
|
-I |
1.3 | |
|
-Br |
1.5 | |
|
-Cl |
1.6 | |
|
-COOR |
1.9 | |
|
-CHO |
2.8 | |
|
-SO3H |
3.8 | |
|
-CN |
3.9 | |
|
-NO2 |
4.0 |
Как и для бензола, для всех ароматических соединений должны быть характерны реакции электрофильного замещения (SE). Заместители, обладающие донорными или акцепторными электронными эффектами разной силы, могут облегчать взаимодействие с электрофилами или, наоборот, затруднять его, влияя, таким образом, на скорость реакции, а также на условия её протекания и полноту превращения.
Кроме того, наличие в бензольном кольце акцепторных заместителей может привести к понижению электронной плотности на атомах углерода настолько, что становятся возможными и реакции нуклеофильного замещения (SN).