
- •Глава 2. Алканы
- •2.1. Номенклатура. Изомерия
- •2.2. Строение
- •2.3. Физические свойства
- •2.4. Химические свойства
- •2.4.1. Реакции радикального замещения
- •2.4.2. Реакции дегидрирования и разложения
- •2.4.3. Реакции изомеризации
- •Способы получения и природные источники
- •2.6. Применение и физиологическая роль
- •Вопросы и упражнения
2.2. Строение
В молекуле метана атом углерода образует четыре равноценных -связи с четырьмя атомами водорода. Образование равноценных связей объясняют гибридизацией атомных орбиталей углерода. Здесь наблюдается sp3-гибридизация. Как уже ранее отмечалось, на возбуждение атома углерода и на гибридизацию требуется 400 + 255 кДж/моль. Образование молекулы метана из атомов сопровождается выделением такого количества энергии, которое с избытком компенсирует первоначально затраченную.
С (sp3) + 4 H (s) CH4 + 2317 кДж/моль
Выигрыш энергии составляет 2317 – 655 = 1662 кДж/моль или на каждую связь С–Н 1662 : 4 = 415.5 кДж/моль. Этот энергетический выигрыш стабилизирует sp3-гибридное состояние углерода.
Образование связей С–Н в молекуле метана происходит в направлении sp3-гибридных орбиталей атома углерода путём их перекрывания с s-орбиталями атомов водорода:

В результате этого перекрывания увеличивается электронная плотность в поле ядер взаимодействующих атомов, что и обуславливает сближение ядер этих атомов на расстояние, называемое длиной связи. Соединив между собой ядра атомов водорода, получим правильный тетраэдр, в центре которого находится ядро атома углерода.
В молекулах этана, пропана и более высших алканов каждый атом углерода образует четыре -связи, но в общем случае они неравноценны, так как это связи с разными атомами, и валентные углы неодинаковы. Как уже указывалось в главе 1.2, углы между связями центрального атома пропана составляют:
|
|
НСН = 107 |
|
ССС = 112 |
Тем не менее, каждый из атомов находится в центре тетраэдра, и углеродная цепь не может быть прямолинейной, она изогнута в пространстве. Это видно уже на примере бутана:
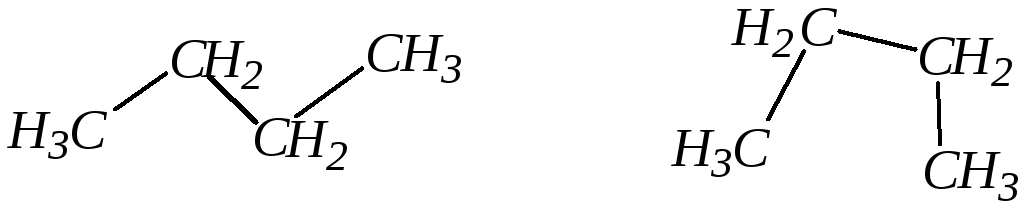
2.3. Физические свойства
Это неполярные или малополярные соединения, поэтому хорошо растворимы в неполярных растворителях; нерастворимы в воде и других полярных растворителях. Первые четыре представителя — газы; углеводороды, имеющие от 5 до 15 атомов углерода, — жидкости; высшие — твёрдые тела.
Газы не имеют вкуса, цвета и запаха. Жидкости — бесцветны, подвижны, с плотностью 0.8—0.9 г/мл. Твёрдые вещества — белого цвета, жирны на ощупь.
Агрегатное состояние алканов во многом определяется межмолекулярным взаимодействием типа ван-дер-ваальсового. Это взаимодействие увеличивается с ростом углеродной цепи и количеством соприкасающихся атомов. Поэтому температуры кипения и плавления возрастают от низших алканов к высшим, причём разветвлённые изомеры кипят и плавятся при более низкой температуре, чем изомеры нормального строения.
В общем, алканы с разветвлённой цепью имеют точки кипения ниже, чем их неразветвлённые изомеры, поскольку у них более нерегулярная структура и меньшая поверхность (меньше ван-дер-ваальсовы силы). Неполярные молекулы, как, например, метан, неопентан и гексаметилэтан (2,2,3,3-тетраметилбутан), у которых строение близко к сферическому, имеют точки плавления и кипения сравнительно близкие друг к другу.
Температуры плавления нормальных алканов с чётным числом атомов углерода сравнительно выше, чем алканов с нечётным числом атомов углерода. Это является следствием упаковки в кристаллической решётке, которая плотнее для алканов с чётным числом углеродных атомов.
Плотность и вязкость жидкостей по этой же причине также должна возрастать с увеличением числа углеродных атомов в молекуле:
|
температура кипения,C |
Число атомов углерода в н-алкане |
|
температура плавления, C |
Число атомов углерода в н-алкане |
|
Плотность, г/мл |
Число атомов углерода в н-алкане |




