
- •(ЧитГу)
- •Индивидуальные домашние задания по химии
- •1. Классы неорганических соединений
- •12,73 Г г раствора, тогда г
- •Вариант 2
- •Вариант 5
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 18
- •Вариант 19
- •Вариант 20
- •Вариант 21
- •Вариант 22
- •Вариант 23
- •Вариант 24
- •Вариант 25
- •2. Химический эквивалент
- •Решение. Эквивалент есть количество вещества и выражается в молях.
- •Решение. Эквивалентную массу koh рассчитаем по формуле:
- •Решение. Эквивалент (эквивалентная масса) химического соединения равен сумме эквивалентов (эквивалентных масс) составляющих его частей.
- •3. Строение атома
- •Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 1
- •Вариант 5
- •Вариант 17
- •Вариант 18
- •5. Химическая термодинамика
- •Вариант 9
- •Вариант 1
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 9
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Вариант 16
- •Вариант 18
- •11. Свойства металлов
- •Вариант 11
- •Вариант 21
- •Библиографический список
- •672039, Чита, ул. Александрово-Заводская, 30
Решение. Эквивалентную массу koh рассчитаем по формуле:
mэ(KOH) = М(KOH)/кислотность = 56/1 = 56 г/моль.
Эквивалентную массы кислоты определим исходя из закона эквивалентов: m(KOH)/m(кислоты) =mэ(KOH)/mэ(кислоты)
![]() =
=
![]()
![]() =
=
![]() = 49 г/моль
= 49 г/моль
Пример 4. Определите массу металла, вступившего в реакцию с кислотой, если при этом выделился водород объёмом 260 мл при нормальных условиях. Эквивалентная масса металла mэ(Ме) = 9 г/моль.
Решение. Согласно закону эквивалентов массы (объёмы) реагирующих друг с другом веществ пропорциональны их эквивалентным массам (объёмам).
![]() =
=![]() ,
,
где VЭ(H2) – эквивалентный объём водорода равный 11,2 л.
m(Me)
=
![]() = 90,26/11,2
= 0,2 г.
= 90,26/11,2
= 0,2 г.
Пример 5. Эквивалентная масса металла составляет 63,5 г/моль. Вычислите массовую долю металла (Ме) в его оксиде.
Решение. Массовая доля кислорода в оксиде металла будет равна
100 −
(Ме). Согласно закону эквивалентов:
![]() .
.
Эквивалентная масса кислорода mэ(О) = 16/2 = 8 г/моль.
Из уравнения выразим массовую долю металла
![]() =
=
![]()
8(Ме) = 6350 – 63,5 (Ме)
71,5(Ме) = 6350
(Ме) =
![]() =
88,8 %
=
88,8 %
Пример 6. Из 3,85 г нитрата металла получено 1,60 г его гидроксида. Вычислите эквивалентную массу металла.
Решение. Эквивалент (эквивалентная масса) химического соединения равен сумме эквивалентов (эквивалентных масс) составляющих его частей.
Эквивалент (эквивалентная масса) гидроксида равен сумме эквивалентов (эквивалентных масс) металла и гидроксильной группы.
Эквивалент (эквивалентная масса) соли равен сумме эквивалентов (эквивалентных масс) металла и кислотного остатка.
Согласно закону эквивалентов:
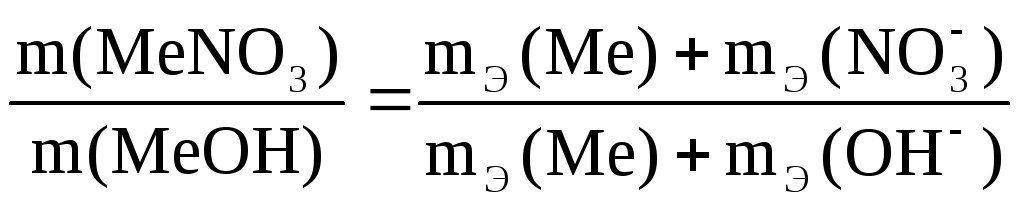
![]()
![]()
![]()
![]()
Вариант 1
Определите эквивалентную массу металла в следующих соединениях: Mn2O7, Ba(OH)2, Ca3(PO4)2, FeSO47H2O.
При восстановлении водородом 1,34 г оксида металла до металла образовалось 0,324 г воды. Определите эквивалентную массу металла.
Алюминий массой 0,752 г при взаимодействии с кислотой вытеснил водород объёмом 0,936 л (н.у.). Определите эквивалентную массу алюминия.
Вариант 2
Вычислите эквивалентную массу гидроксида висмута(III) в реакциях взаимодействия с HCl при получении хлорида висмута и гидрохлорида висмута.
Элемент образует гидрид, где его массовая доля 75 %. Определите эквивалентную массу элемента.
При растворении в кислоте металла массой 11,9 г выделился водород объёмом 2,24 л (н.у.). Определите эквивалентную массу металла.
Вариант 3
Чему равна эквивалентная масса ZnSO4 в реакциях со щелочью, идущих с образованием Zn(OH)2, (ZnOH)2SO4, Na2[Zn(OH)4].
Для растворения металла массой 16,86 г потребовалась серная кислота массой 14,7 г. Вычислите эквивалентную массу металла.
На сжигание 0,5 г двухвалентного металла требуется 0,23 л кислорода (н.у.). Определите эквивалентную массу металла, укажите какой это металл.
Вариант 4
Определите эквивалент и эквивалентную массу серы в следующих соединениях: H2S, SO2, H2SO4.
Металл массой 0,150 г вытесняет из раствора никелевой соли никель массой 0,367 г, а из раствора кислоты – водород объёмом 140 мл (н.у.). Определите эквивалентную массу никеля.
Оксид марганца содержит 22,56 % кислорода. Вычислите эквивалентную массу марганца в оксиде и составьте его формулу.
Вариант 5
Эквивалентная масса некоторого элемента равна 24,99 г/моль. Вычислите: а) массовую долю кислорода в оксиде этого элемента; б) объём водорода, который потребуется для восстановления 4,95 г его кислородного соединения.
Вычислите эквивалентную массу H3PO4 в реакциях взаимодействия с КОН при получения: а) фосфата калия; б) дигидрофосфата калия; в) гидрофосфата калия.
На нейтрализацию 1 г основания израсходовано 2,14 г соляной кислоты. Определите эквивалентную массу основания.
Вариант 6
Мышьяк образует два оксида, массовая доля мышьяка в которых соответственно равна 65,2 и 75,7 %. Рассчитайте эквивалентную массу мышьяка в этих оксидах.
Найдите эквивалентную массу воды при реакции её а) с металлическим натрием; б) с оксидом натрия.
Вычислите эквивалентную массу цинка, если 1,168 г его вытеснили из кислоты 43,8 мл водорода, измеренного при н.у.
Вариант 7
На нейтрализацию 0,943 г фосфористой кислоты H3PO4 израсходовано 1,291 г гидроксида калия. Вычислите эквивалентную массу кислоты и её основность.
Вычислите эквивалент и эквивалентную массу хлорида алюминия в реакциях:
а) AlCl3 + 2NaOH = Al(OH)2Cl + 2NaCl;
б) AlCl3 + 3NaOH = Al(OH)3 + 3 NaCl.
3. Чему равна эквивалентная масса металла, если его навеска массой 20 г вытесняет из кислоты водород объемом 7,01 л при н.у.
Вариант 8
На осаждение хлорида, содержащегося в 0,666 г соли, израсходовано 1,088 г. Вычислите эквивалентную массу соли.
2. Определите эквивалент и эквивалентную массу гидроксида никеля в реакциях:
а) Ni(OH)2 + H2SO4 = NiSO4 + 2H2O;
б) 2Ni(OH)2 + H2SO4 = (NiOH)2SO4 + 2H2O.
3. Эквивалентная масса металла равна 29,36 г/моль. Сколько граммов этого металла необходимо для вытеснения 105 мл водорода (н.у.) из кислоты?
Вариант 9
Определите эквивалентную массу двухвалентного металла, если из 48,15 г его оксида можно получить 88,65 г его нитрата. Укажите, какой это металл.
Вычислите эквивалентную массу металла в следующих соединениях: Ag2O, Al2(SO4)318H2O, CuCl.
Сколько эквивалентных масс кислорода содержится в 33,6 л его (н.у.)?
Вариант 10
Массовые доли галогена в галогениде металла соответственно равны 64,5 и 15,4 %. Определите эквивалентную массу металла, массу металла и объём выделившегося водорода (н.у.).
Для растворения 16,8 г металла потребовалось 14,7 г серной кислоты. Определите эквивалентную массу металла и объём выделившегося водорода (н.у.).
В каком количестве Cr(OH)3 содержится столько же эквивалентов, сколько в 174,96 г Mg(OH)2?
Вариант 11
Определите эквивалент и эквивалентную массу фосфора, кислорода и брома в соединениях PH3, H2O, HBr.
При пропускании H2S через раствор, содержащий 2,98 г хлорида некоторого одновалентного металла, образуется 2,2 г его сульфида. Вычислите эквивалентную массу металла.
Сколько металла, эквивалентная масса которого 12,16 г/моль, взаимодействует с 310 см3 кислорода (н.у.).
Вариант12
В состав оксида серебра входит 93,09 % серебра, а в состав иодида серебра – 45,95 % серебра. Найдите эквивалентную массу йода.
В какой массе гидроксида натрия содержится столько же эквивалентных масс, сколько содержится в 140 г КОН.
На сжигания 1,5 г двухвалентного металла требуется 0,69 л кислорода (н.у.). Вычислите эквивалентную массу и атомную массу этого металла.
Вариант 13
Напишите уравнения реакций Fe(OH)3 с соляной кислотой, при которых образуется: а) хлорид дигидроксожелеза; б) хлорид железа (III). Вычислите эквивалент и эквивалентную массу Fe(OH)3 в этих реакциях.
Определите эквивалентную массу серы, если 6,48 г металла образует 6,96 г оксида и 7,44 г сульфида.
При взаимодействии 3,24 г трёхвалентного металла с кислотой выделяются 4,03 л водорода (н.у.). Вычислите эквивалентную и атомную массы металла.
Вариант 14
Из 1,35 г оксида металла получается 3,15 г его нитрата. Вычислите эквивалентную массу этого металла.
Избытком соляной кислоты подействовали на растворы: а) гидрокарбоната кальция; б) дихлорида гидроксоалюминия. Напишите уравнения реакций этих веществ с HCl и определите их эквивалентные массы.
Сколько граммов металла, эквивалентная масса которого 12 г/моль, взаимодействует с 3,1 л кислорода (н.у.).
Вариант 15
4,086г металла вытесняют из кислоты 1,4 л водорода, измеренного при н.у. Эта же масса металла вытесняет 12,95 г свинца из растворов его солей. Вычислите эквивалентную массу свинца.
Вычислите эквивалент и эквивалентную массу бора, хрома и кальция в соединениях: B2O3; Cr(OH)3; Ca3(PO4)2.
Сколько эквивалентных масс содержится в 340 г нитрата серебра?
Вариант 16
При восстановлении 4,34 г оксида марганца алюминием получено 3,4 г оксида алюминия Al2O3. Вычислите эквивалентную массу марганца, его валентность и составьте формулу оксида марганца.
При окислении 0,24 г металла израсходовано 112 мл кислорода (н.у.). Определите эквивалентные массы металла и его оксида.
Эквивалентная масса элемента составляет 24,99 г/моль. Вычислите, сколько граммов водорода требуется для восстановления 4,95 г его соли.
Вариант 17
Эквивалентная масса металла равна 56,2 г/моль. Вычислите процентное содержание этого металла в его оксиде.
2. Определите эквивалент и эквивалентную массу гидроксида алюминия в реакциях:
а) Al(OH)3 + HNO3 = AlOH(NO3)2 + H2O;
б) Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O.
3. Одна и та же масса металла соединяется с 1,591 г галогена и с 70,2 мл кислорода (н.у.). Вычислите эквивалент галогена.
Вариант 18
На восстановление 2,33 г хлорида циркония до свободного израсходовано 0,48 г магния. Эквивалентная масса магния равна 12 г/моль. Определите эквивалент циркония и его валентность.
Вычислите эквивалентную массу KHSO4 в следующих реакциях:
а) KHSO4 + BaCl2 = BaSO4 + KCl + HCl;
б) KHSO4 + KOH = K2SO4 + H2O.
3. Элемент образует оксид, содержащий 31,58 % кислорода. Вычислите эквивалент элемента.
Вариант 19
Определите эквивалентные массы следующих кислот: HClO; H2SiO3; HMnO4; H2SnO3.
Вещество содержит 39 % серы, эквивалентная масса которой 16 г/моль и мышьяк. Вычислите эквивалентную массу и валентность мышьяка, составьте формулу этого вещества.
1 г металла соединяется с массой хлора, занимающей объём 336 мл (н.у.). Вычислите эквивалент металла.
Вариант 20
При сгорании серы в кислороде образовалось 12,8 г SO2. Сколько эквивалентов кислорода требуется на эту реакцию. Чему равны эквиваленты серы и её оксида.
Определите эквивалентную массу H2SO3 в реакциях образования: а) сульфита лития; б) гидросульфита лития.
0,934 г металла вытеснили из соляной кислоты 348 мл водорода (н.у.). Вычислите эквивалент металла.
Вариант 21
Путём разложения нагреванием 0,26 г оксида серебра получено 0,243 г металлического серебра. Определите эквивалентную массу серебра.
Вычислите эквивалентную массу гидроксида меди(II) в реакциях взаимодействия с HCl при получении а) хлорида меди; б) гидроксохлорида меди.
Эквивалент металла равен 8,99. Какой объём водорода (н.у.) выделится при взаимодействии 0,4495 г металла с соляной кислотой.
Вариант 22
При взаимодействии ортофосфорной кислоты со щелочью образовалось соль Na2HPO4. Найти для этой реакции эквивалентную массу ортофосфорной кислоты.
В состав метана входит 25 % водорода и 75 % углерода. Чему равна эквивалентная масса углерода.
Вычислите эквивалент металла и его оксида, зная, что 0,304 г металла вытесняет из кислоты 0,282л кислорода (н.у.).
Вариант 23
Определите эквивалентную массу гидроксида магния в реакциях:
а) Mg(OH)2 + HBr = MgOHBr +H2O;
б) Mg(OH)2 + 2HBr = MgBr2 + 2 H2O.
2. При восстановлении 1,506 г оксида олова водородом образовалось 0,36 г воды. Определите эквивалентную массу олова и его валентность. Напишите формулу оксида олова.
3. Какой объём водорода (н.у.) выделится при взаимодействии 3,6 г металла с кислотой, эквивалентная масса которого равна 12 г/моль?
Вариант 24
Определите эквивалентные массы следующих солей: NaNO2, Cr2(SO4)3, CH3COOH, MgOHNO3, LiHSO4.
Эквивалентная масса металла равна 56,2 г/моль. Вычислите процентное содержание этого металла в его оксиде.
При взаимодействии 3,182 г галогена израсходовано 140,4 мл кислорода (н.у.). Вычислите эквивалент галогена и назовите его.
Вариант 25
Эквивалентная масса металла равна 29,36 г/моль. Сколько граммов этого металла необходимо для вытеснения 105 мл водорода (н.у.)?
Определите эквивалент фосфора в соединениях: PH3, P2O5, P2O3, H3PO3.
Одна и та же масса металла соединяется с 1,591 г галогена и 70,2 см3 кислорода при н.у. Вычислите эквивалентную массу галогена.
