- •Кафедра химической технологии
- •Химия и биохимия углеводов.
- •Раздел I. Химия моносахаридов.
- •Содержание
- •Введение
- •1 Классификация и номенклатура
- •2 Химическое строение моносахаридов
- •3 Стереохимия
- •Цифры 4,3,2,1 означают падение старшинства атомных
- •4 Таутомерия моносахаридов в растворах
- •1) Кето-енольную и 2) кольчато-цепную или оксо-окси-таутомерию.
- •Мутаротация
- •6 Способы получения моносахаридов
- •7 Физические свойства моносахаридов
- •8 Химические свойства моносахаридов
- •Литература
- •Научный редактор профессор г.Н. Роганов
3 Стереохимия
Для углеводов свойственна оптическая изомерия. Рассмотрим сначала открытые формы моносахаридов. В молекулах моносахаридов имеются асимметрические атомы углерода (хиральные центры), что служит причиной существования большого числа стереоизомеров, соответствующих одной и той же структурной формуле. Вспомним, что ассиметрический атом углерода - это атом углерода, связанный с четырьмя разными заместителями. Альдотриозы содержат один хиральный центр, альдотетрозы - два, альдопентозы - три, альдогексозы - четыре. Кетозы содержат на один хиральный центр меньше, чем альдозы с тем же числом атомов углерода.
-
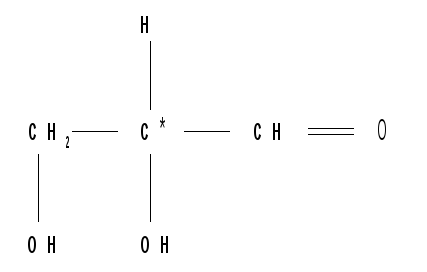
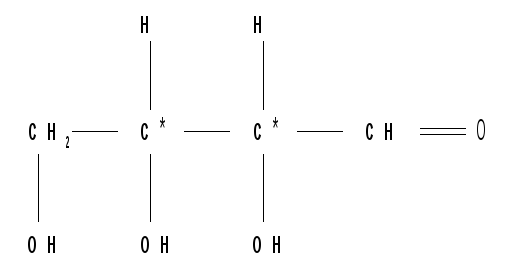
альдотриоза
Альдотетроза
|
|
|
альдопентоза |
|
|
|
альдогексоза |
-

кетогексоза
Количество стереоизомеров связано с числом асимметрических атомов углерода формулой N = 2 n .
Для альдогексозы, имеющей четыре хиральных центра число стереоизомеров в соответствии с формулой N = 2n ( где n- число асимметрических атомов углерода ), будет равно 24 = 16, т. е. 8 пар энантиомеров, антиподов, а для кетогексозы, имеющей три хиральных центра, число стереоизомеров будет меньше : N = 23 = 8 ( 4 пары энантиомеров ).
3.1 Проекционные формулы Фишера, Д- и L - ряды
Для изображения стереоизомеров удобно пользоваться проекционными формулами Фишера. Для получения проекционной формулы углеродную цепь моносахарида располагают по вертикали с оксогруппой в верхней части цепи, а сама цепь должна иметь форму полукольца, обращенного выпуклостью к наблюдателю. Все асимметрические углеродные атомы находятся в заслоненной конформации, и группы Н и ОН направлены к наблюдателю:

Получение проекционной формулы тетрозы ( эритрозы ).
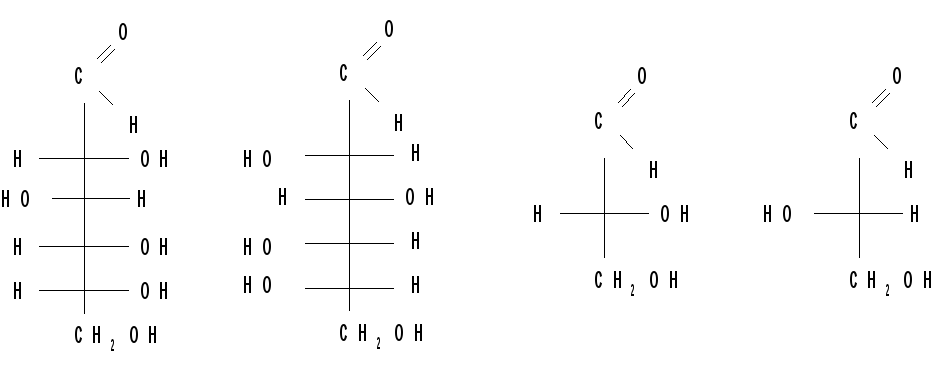
Так как энантиомеры - это пространственные изомеры, являющиеся зеркальным отражением друг друга, то каждой паре энантиомеров дано одно название и указывается их противоположная конфигурация (Д и L). Буквы Д и L указывают на принадлежность сахаров Д- и L-стехиометрическим рядам. Например, для глюкозы:
-
Д(+)-глюкоза
L(-)-глюкоза
Д(+)-глицериновый
Альдегид
L(-)-глицериновый
альдегид
Относительная конфигурация моносахаридов (отношение к Д- или L- ряду) определяется по конфигурационному стандарту - глицериновому альдегиду. С конфигурацией его хирального центра сравнивается конфигурация наиболее удаленного от карбонильной группы (“концевого”) асимметрического атома углерода, имеющего наибольший номер. В альдопентозах таким атомом будет С4, а в альдогексозах - С5, в кетогексозах - С5и т. д. Если у моносахарида эта ОН- группа находится справа, как у Д - глицеринового альдегида, то моносахарид относится к Д- ряду. Для указания направления вращения раствором моносахарида плоскости поляризации поляризованного света используются знаки (+) - правовращающий и (-) - левовращающий или, соответственно, маленькие латинские буквы d и l , которые в настоящее время не употребляются. Знак вращения плоскости поляризации поляризованного света моносахаридами непосредственно нельзя связать с их принадлежностью к Д- и L- ряду, он определяется экспериментально. Так, среди альдопентоз и альдогексоз Д - стереохимического ряда имеются как лево-, так и правовращающие соединения. Например, природные фруктоза и глюкоза обозначается : Д (-) - фруктоза (или раньше Д,l - фруктоза), т. е. фруктоза обладает левым вращением; Д(+) - глюкоза (или раньше Д,d - глюкоза), т.е. глюкоза обладает правым вращением. Д(+)- и L(-)-глицериновые альдегиды являются родоначальниками генетических рядов сахаров (альдоз). От Д(+)- глицеринового альдегида образуется Д-ряд сахаров, а от L(-) - глицеринового альдегида - L-ряд сахаров. Каждый моносахарид в этом ряду, начиная с глицеринового альдегида, при введении еще одного атома углерода дает два стереоизомера (диастереомера) - (см. схему). Семейство кетоз формально можно произвести от дигидроксиацетона путем последовательного наращивания цепи на один атом углерода.
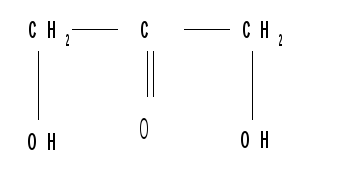
(кетотриоза)
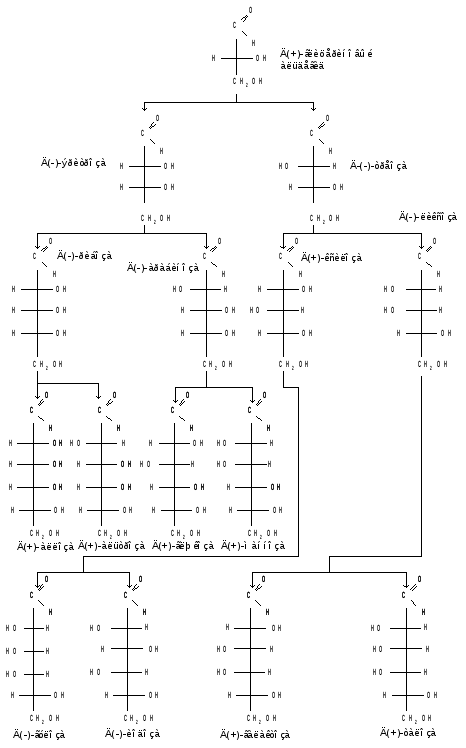
Генетический Д-ряд альдоз
Подавляющее большинство природных моносахаридов принадлежит к Д-ряду. Каждой альдозе Д-ряда соответствует энантиомер L-ряда с противоположной конфигурацией всех ( ! )центров хиральности.
Как следует из схемы, восемь стереоизомеров Д-альдогексоз имеют одинаковое химическое строение, но отличаются конфигурацией одного или нескольких асимметрических атомов углерода, т. е. являются диастереоизомерами и поэтому каждый из них имеет свое название (глюкоза, манноза, галактоза и т. д. ). Соответственно альдопентозы имеют четыре диастереоизомера. Альдозы, отличающиеся одна от другой конфигурацией только одного соседнего с карбонильной группой асимметрического атома углерода, называются эпимерами. Так, глюкоза и манноза, рибоза и арабиноза являются эпимерами. Эпимеры - частный случай диастереоизомеров.
3.2 Понятие о конформационной изомерии
Для сахаров в циклической форме возможен еще один вид пространственной изомерии - конформационная изомерия, связанная с расположением в пространстве углеродных атомов шестичленного цикла. Однако, если для циклогексана известно всего две конформации - “ кресло “ и “ванна”, то для моносахаридов в пиранозной форме известно 8 конформаций - две креслообразных и шесть типа ванны ввиду присутствия в шестичленном цикле гетероатома - кислорода. Шесть ваннообразных конформаций энергитически менее выгодны и их существование можно не учитывать. Из двух креслообразных конформаций

С1 - изомер более предпочтителен, так как подавляющее число заместителей в нем ориентировано в экваториальном, совпадающем с плоскостью цикла, направлении. Именно в виде С1 - конформации существует большинство моносахаридов, например, для Д-глюкопиранозы в этой конформации первичноспиртовая СН2ОН - группа и гидроксильные группы занимают экваториальные положения. При этом полуацетальный гидроксил у -аномера находится в экваториальном, а у -аномера - в оксиальном положениях. Поэтому -аномер Д-глюкозы преобладает в равновесной смеси над -аномером:
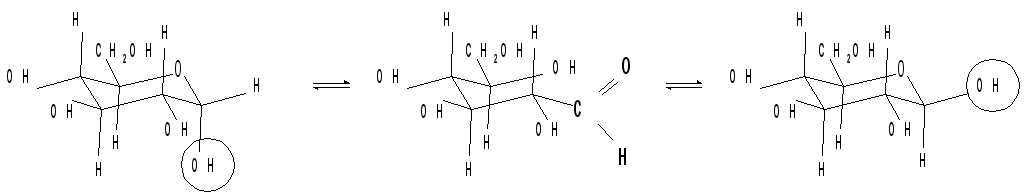
|
-Д-глюкопираноза (36%) |
Д-глюкоза |
-Д-глюкопираноза (64%) |
Аномеры образуются не в равных количествах, а с преобладанием термодинамически более устойчивого диастереоизомера.
Конформационное строение Д-глюкопиранозы обьясняет уникальность этого моносахарида. -Д-глюкопираноза- моносахарид с полным экваториальным расположением объемных заместителей. Обусловленная этим высокая термодинамическая устойчивость - основная причина широкой распространенности ее в природе.
У Д-галактопиранозы ОН-группа при С4 находится в аксиальном положении. Соотношение - и -аномеров в равновесной смеси приблизительно такое же, как и у Д-глюкопиранозы :
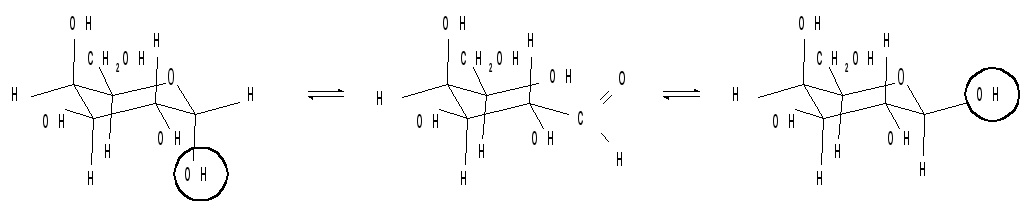
|
-Д-галактопираноза (30%) |
Д-галактоза |
-Д-галактопираноза (70%) |
У Д-маннопиранозы ОН-группа при С2 занимает аксиальное положение и в смеси таутомеров преобладает -аномер. У -аномера в пространстве оказываются сближенными орбитали с электронными парами трех атомов кислорода (циклического и двух гидроксильных групп при С1 и С2). Возникающее отталкивание электронов делает -форму невыгодной. В -аномере гидроксильные группы при С1 и С2 находятся в наибольшем удалении друг от друга, чем и объясняются его преобладание. Следует отметить, что -Д- маннопираноза имеет сладкий, а ее -аномер - горький вкус.

-Д- маннопираноза
Конформационное строение моносахаридов обуславливает формирование пространственного строения длинных полисахаридных цепей, т. е. вторичную структуру.
Наличие в пиранозном цикле атома кислорода определяет ряд дополнительных факторов, влияющих на устойчивость аномеров. Например, при замещении в молекуле Д-глюкопиранозы полуацетальной гидроксильной группы на алкоксильную (при образовании гликозидов) более выгодной может стать -аномерная форма. Стремление алкоксильной группы занять аксиальное положение связано с так называемым аномерным эффектом, который проявляется как результат отталкивания между сближенными в пространстве электронными парами двух атомов кислорода - циклического и входящего в состав алкосиальной группы. В -аномере такое отталкивание электронных пар отсутствует, т.к. атомы кислорода пространственно удалены.
3.3 R -,S- номенклатура моносахаридов
Д,L - система обозначений для моносахаридов не вполне универсальна, так как основывается на конфигурации одного из многих центров хиральности. Однако она используется в химии углеводов и лишь в редких случаях заменяется R-,S- номенклатурой.
Например, Д-глюкоза получает название (2 R, 3 S, 4 R 5 R)-2,3,4,5,6 - пентагидроксигексаналь .
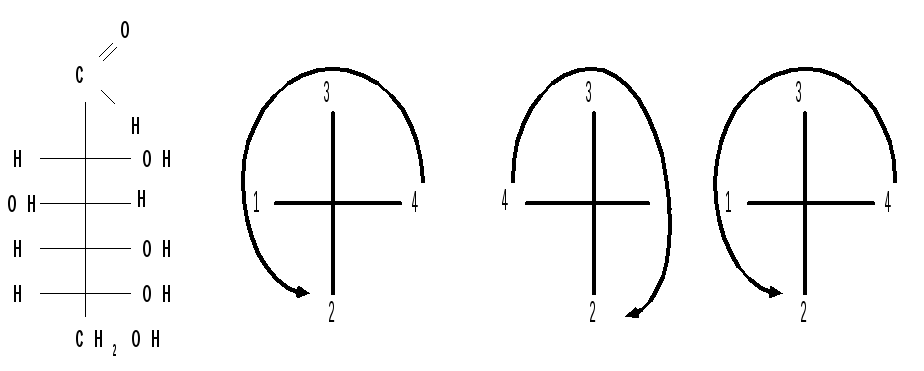
-
Д-глюкоза
R по С2
S по С3
R по С4 и С5