
- •Кафедра химической технологии
- •Химия и биохимия углеводов.
- •Раздел I. Химия моносахаридов.
- •Содержание
- •Введение
- •1 Классификация и номенклатура
- •2 Химическое строение моносахаридов
- •3 Стереохимия
- •Цифры 4,3,2,1 означают падение старшинства атомных
- •4 Таутомерия моносахаридов в растворах
- •1) Кето-енольную и 2) кольчато-цепную или оксо-окси-таутомерию.
- •Мутаротация
- •6 Способы получения моносахаридов
- •7 Физические свойства моносахаридов
- •8 Химические свойства моносахаридов
- •Литература
- •Научный редактор профессор г.Н. Роганов
Цифры 4,3,2,1 означают падение старшинства атомных
номеров заместителей.
В циклических формах моносахаридов независимо от размера кольца (пиранозное или фуранозное) атом углерода карбонильной группы становится асимметрическим и он также имеет 2 зеркальные конфигурации. Например, для Д - глюкозы :
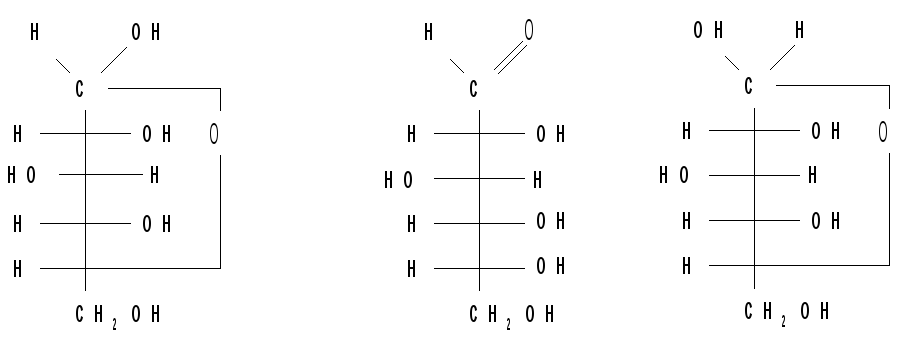
|
-Д-глюкопираноза |
Д-глюкоза |
-Д-глюкопираноза |
С1 - новый хиральный центр, этот атом называют аномерным. Две стереоизомерные формы глюкозы отличаются конфигурацией одного хирального центра С1 и называются - и -формами, - и -аномерами. У -аномера конфигурация аномерного центра одинакова с конфигурацией “концевого ” хирального центра, определяющего принадлежность к Д- или L- ряду, а у -аномера - противоположна, т. е. эти ОН-группы находятся на противоположных сторонах. Аномерные префиксы - и - используют только в сочетании с конфигурационными префиксами ( Д- и L- ). Таким образом, в проекционных формулах Фишера у моносахаридов Д-ряда в -аномере полуацетальный (гликозидный) гидроксил располагается справа, а в -аномере - слева от углеродной цепи. Следует отметить, что -аномер имеет R-конфигурацию по С1, а -аномер - S-конфигурацию по С1, т. е. аномерные атомы углерода в - и -формах имеют противоположные конфигурации . Но в целом - и -аномеры из-за наличия еще нескольких центров хиральности являются не энантиомерами (зеркальными изомерами), а диастереоизомерами. Циклические формы моносахаридов, следовательно, содержат на один асимметрический атом углерода больше, чем открытые, поэтому у них в два раза больше оптически активных изомеров, т. е. N=25=32.
3.4 Перспективные формулы Хеуорса
Для изображения циклических форм моносахаридов можно пользоваться более наглядными перспективными формулами Хеуорса. Формулы Хеуорса представляют собой шестиугольники и пятиугольники, изображенные в перспективе - цикл лежит в горизонтальной плоскости, связи, расположенные ближе к наблюдателю, изображаются более жирными линиями. Атом кислорода располагается в пиранозном цикле в правом верхнем углу, в фуранозном - за плоскостью цикла, углеродные атомы, входящие в цикл, не пишутся, а только нумеруются от кислорода по часовой стрелке. Через атомы углерода проводят вертикальные линии, на концах которых пишут водородные атомы и ОН-группы. Рассмотрим взаимоотношения проекционных формул Фишера и перспективных формул Хеуорса. Все группы (Н и ОН), расположенные справа в формуле Фишера, пишут под плоскостью цикла, а расположенные слева - над плоскостью цикла, концевая СН2-ОН группа располагается сверху от плоскости молекулы, если моносахарид относится к Д-ряду, и снизу от плоскости, если он относится к L-ряду.
Таким образом, в формулах Хеуорса полуацетальный гидроксил и концевая СН2-ОН группа располагаются у -аномеров по разные стороны кольца, а у -аномеров - по одну сторону (кружком обведены полуацетальные гидроксилы).

-
-Д-глюкофураноза

-
-Д-глюкопираноза
Аналогично можно осуществить переход от формул Фишера к формулам Хеуорса на примере одного из аномеров фуранозной формы Д-фруктозы :
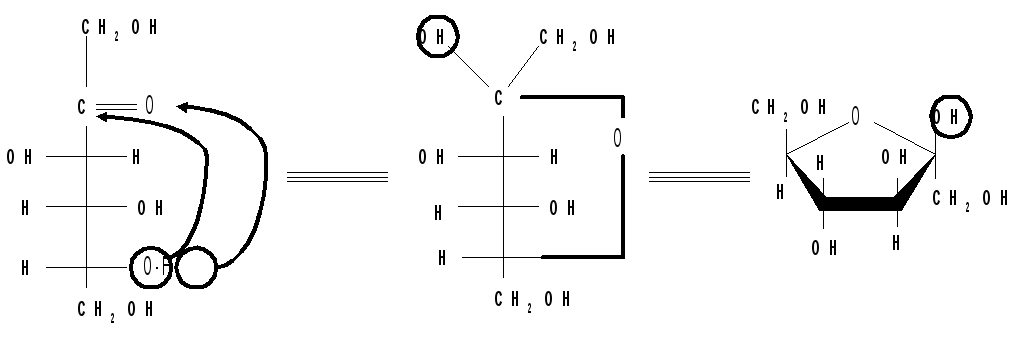
-
-Д-фруктофураноза
