
- •Кафедра химической технологии
- •Химия и биохимия углеводов.
- •Раздел I. Химия моносахаридов.
- •Содержание
- •Введение
- •1 Классификация и номенклатура
- •2 Химическое строение моносахаридов
- •3 Стереохимия
- •Цифры 4,3,2,1 означают падение старшинства атомных
- •4 Таутомерия моносахаридов в растворах
- •1) Кето-енольную и 2) кольчато-цепную или оксо-окси-таутомерию.
- •Мутаротация
- •6 Способы получения моносахаридов
- •7 Физические свойства моносахаридов
- •8 Химические свойства моносахаридов
- •Литература
- •Научный редактор профессор г.Н. Роганов
6 Способы получения моносахаридов
1. Основным способом получения моносахаридов, имеющим практическое значения, является гидролиз ди- и полисахароидов, который происходит под действием кислот или ферментов, водные растворы щелочей не способствуют гидролизу :
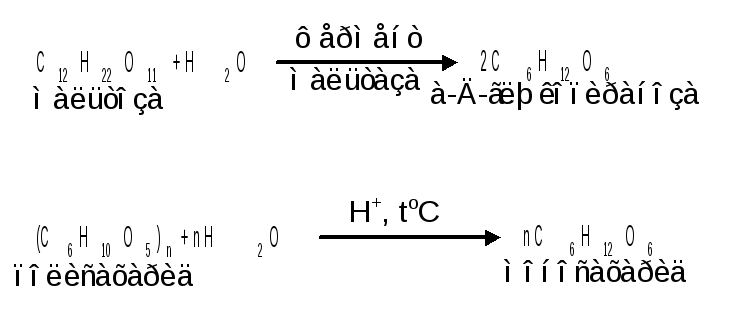
2. Альдольная конденсация формальдегида - первый синтез сахаров был произведен еще А. М. Бутлеровым, который в качестве катализатора альдольной конденсации использовал гидроксид кальция :
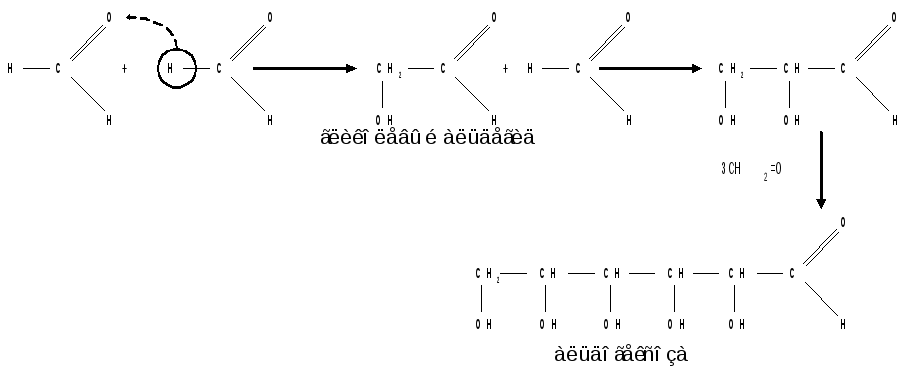
Полученная альдогексоза оптически недеятельна и представляет собой рацемическую смесь Д - и L - альдогексоз.
3. Присоединение синильной кислоты (оксинитрильный синтез) используется для удлинения цепи моносахаридов и перехода от низших моносахаридов к высшим. Этот метод был разработан более ста лет назад (Киллани, Фишер), но до сих пор остается важнейшим методом наращивания цепи моносахаридов, несмотря на свою многостадийность :

Первая стадия - получение оксинитрилов приводит к смеси диастереоизомеров. В результате гидролиза образуется смесь диастереоизомерных амидов, которые омыляют затем гидроксидом бария с образованием смеси диастереомерных солей. Разделение двух диастереомеров проводят на этой стадии методом дробной кристаллизации солей, после чего каждую соль переводят в кислоту. Кислоты нагреванием с разбавленной серной кислотой превращают в соответствующие -лактоны, которые восстанавливают амальгамой натрия в моносахариды : Д- глюкозу и Д- маннозу, содержащие на один углеродный атом больше, чем исходная Д - арабиноза.
4. Метод укорачивания цепи основан на окислении моносахаридов, содержащих на один атом углерода больше, чем в нужном моносахариде. Например, при окислении альдогексозы пероксидом водорода в присутствии ацетата железа (III) образуется альдоновая кислота, которая затем декарбоксилируется с образованием соответствующей альдопентозы :
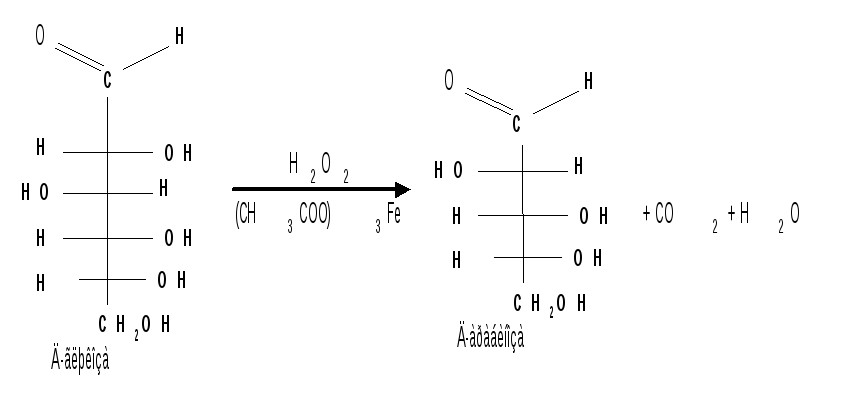
Механизм этой реакции, называемой распад по Руффу, остался невыясненным.
7 Физические свойства моносахаридов
Моносахариды являются твердыми кристаллическими веществами. Все они гигроскопичны, хорошо растворимы в воде, легко образуют сиропы. Растворимость моноз в спирте низкая, в эфире они практически нерастворимы. Растворы моносахаридов имеют нейтральную реакцию по лакмусу и обычно обладают сладким вкусом. Сладость разных моноз различна. Например, фруктоза приблизительно в три раза слаще глюкозы. Растворы моносахаридов обладают оптической активностью, для них характерно явление мутаротации.
8 Химические свойства моносахаридов
В соответствии с химическим строением моносахариды могут проявлять свойства карбонильных соединений, спиртов и полуацеталей. Поскольку циклические и открытые формы моносахаридов в растворе находятся в равновесии друг с другом, то расходование одной из них в ходе реакции сдвигает таутомерное равновесие в сторону реагирующей формы. Рассматривая различные реакции моносахаридов, мы будем приводить формулу лишь той таутомерной формы, которая непосредственно участвует в данной реакции.
8.1 Реакции карбонильных форм моносахаридов
а) Окисление. Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов. Монозы легко окисляются, причем в зависимости от условий окисления образуются различные продукты. Окисление альдоз без деструкции (разрушения) углеродного скелета проводят в нейтральной или кислой среде и получают различные кислоты. При использовании мягких окислителей типа бромной воды, гипохлоритов, разбавленной азотной кислоты окисляется только альдегидная группа и образуются гликоновые (альдоновые ) кислоты :
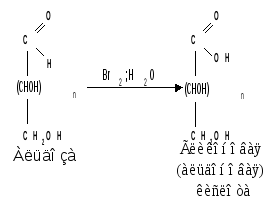
Пример окисления глюкозы :
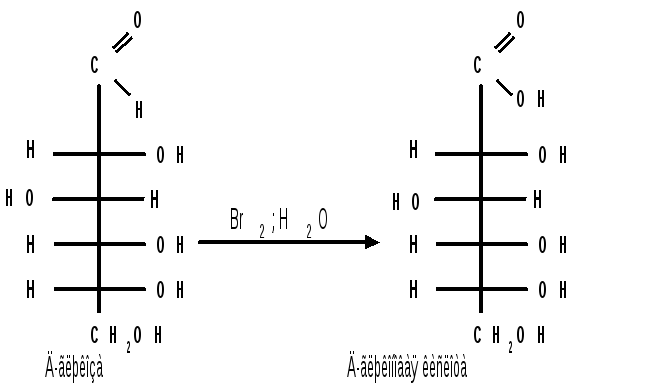
С помощью сильного окислителя - концентрированной азотной кислоты - концевые группы альдоз (альдегидная и первичноспиртовая) одновременно окисляются в карбоксильные группы, образуя гликаровые кислоты (называемые также сахарными):


-
Д-глюкоза
Д-глюкаровая кислота
Получающаяся из Д-галактозы галактаровая (слизевая) кислота трудно растворима в воде, что используется для обнаружения галактозы методом окисления ее азотной кислотой.
Если предварительно защитить склонную к окислению альдегидную группу (например, превращением альдозы в гликозид), то становится возможным избирательное окисление первичной спиртовой группы и образуются гликуроновые (уроновые) кислоты.
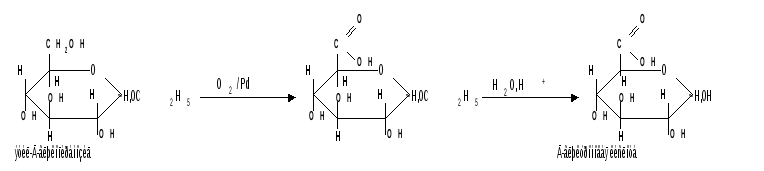
Уроновые кислоты при нагревании их солей с металлами (никель, магний) подвергаются декарбоксилированию. При этом из гексуроновых кислот образуются пентозы. В организме за счет ферментативной реакции декарбоксилирования Д-глюкуроновой кислоты получается Д-ксилоза.

Приведенная реакция показывает генетическую связь пентоз с гексозами, являющимися продуктами фотосинтеза.
Пектиновые вещества плодов и ягод представляют собой продукты поликонденсации Д-галактуроновой кислоты.
Уроновые кислоты выполняют в организме важную функцию : они образуют с лекарственными веществами, их метаболитами, токсичными веществами водорастворимые гликозиды и выводят их из организма.
Кетозы не окисляются слабыми окислителями. При действии сильных окислителей происходит расщепление молекул. Так, например, при окислении фруктозы получаются винная и щавелевая кислоты :
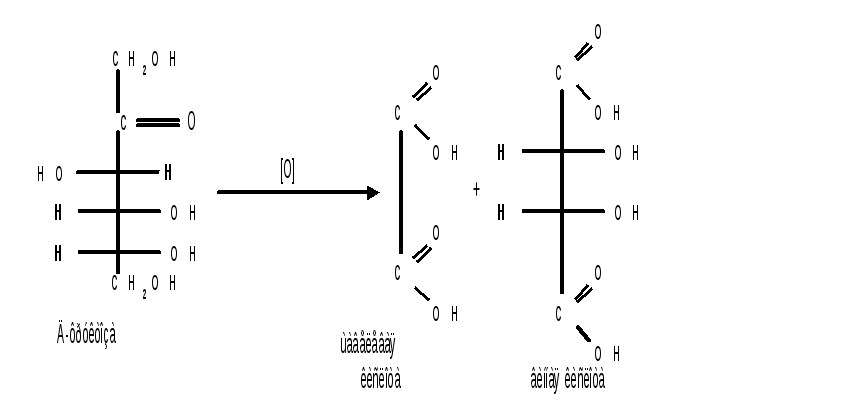
Слабые окислители в щелочной среде (аммиачный раствор оксида серебра, соединения Сu2+ ) превращают монозы в сложную смесь продуктов окисления и служат для качественного и количественного определения альдоз и кетоз .
Подобно обычным альдегидам, альдозы легко дают реакцию “серебряного зеркала” с аммиачным раствором оксида серебра (реактив Толленса) :
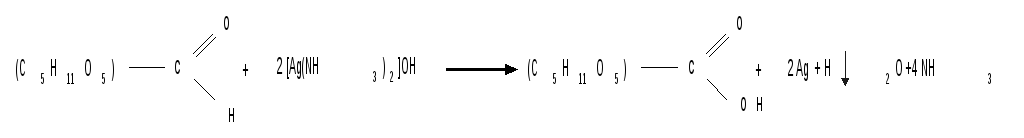
При нагревании реактива Фелинга (смесь равных обьемов водного раствора сульфата меди и щелочного раствора натрий-калиевой соли винной кислоты) в присутствии альдозы выпадает красный осадок Сu2О. Реакцию используют для количественного определения сахаров :
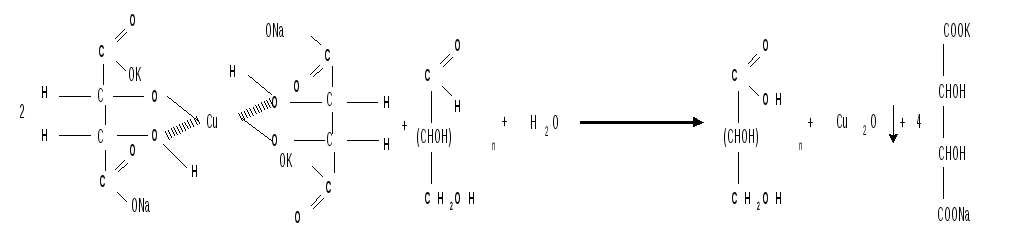
Кетозы тоже способны восстанавливать катионы металлов, так как они в щелочной среде изомеризуются в альдозы.
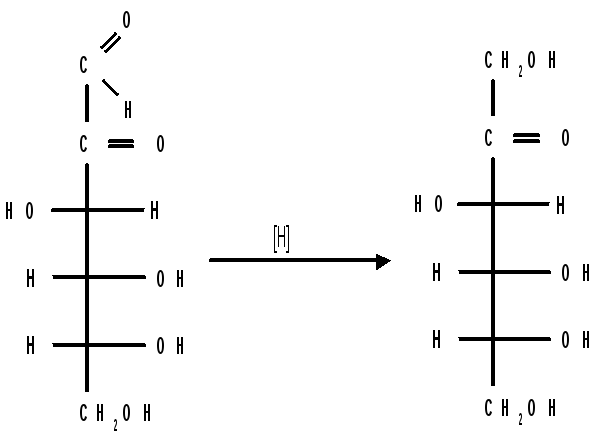
б) Восстановление. При восстановлении моноз образуются многоатомные спирты, называемые альдитами (глицитами). Эти кристаллические, легко растворимые в воде вещества обладают сладким вкусом и часто используются как заменители сахара (ксилит, сорбит).
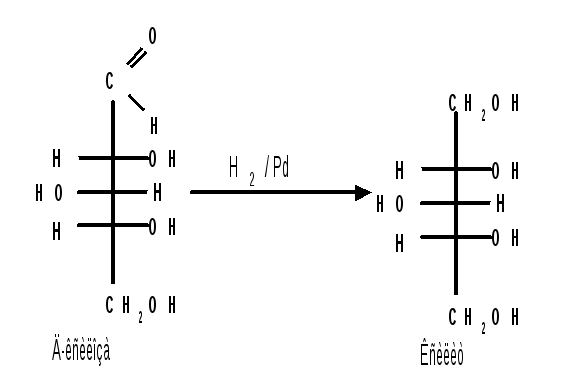
Восстановление моносахаридов проводят водородом в присутствии металлических катализаторов (палладий, никель).
Шестиатомные спирты - глюцит (сорбит), дульцит и маннит - получаются при восстановлении соответственно глюкозы, галактозы и маннозы. Восстановление глюкозы в сорбит является одной из стадий промышленного синтеза аскорбиновой кислоты .
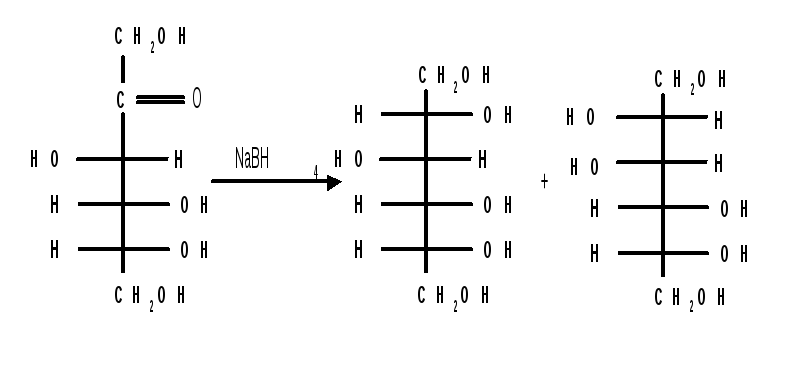
При восстановлении альдоз получается лишь один полиол , кетоз - смесь двух полиолов, например, при восстановлении Д-фруктозы борогидридом натрия NaBН4 образуются Д- глюцит (сорбит) и Д- маннит :
-
Д-фруктоза
Д-глюцит
Д-маннит
в) Присоединение синильной кислоты.
Монозы присоединяют синильную кислоту, образуя нитрилы высших глюконовых кислот (Килиани, 1887) :
![]()
Этим методом можно удлинять углеродную цепь и переходить от низших моносахаридов к высшим (см. способы получения моноз).
г) Действие гидроксиламина. Реакция с гидроксиламином используется для установления строения сахаров и для перехода от высших моносахаридов к низшим :
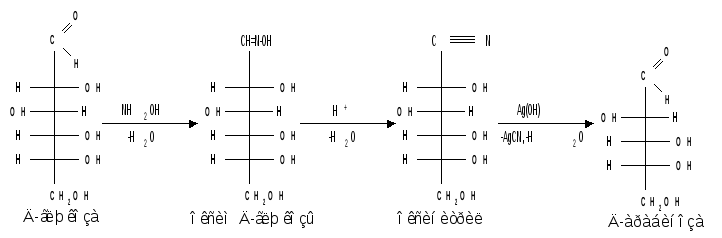
д) Действие фенилгидразина. Одной из наиболее важных реакций, которая позволяет выделять в чистом виде отдельные монозы, а также устанавливать тождество моноз различного происхождения, является взаимодействие моноз с фенилгидразином. Сначала фенилгидразин действует на монозы так же, как на простейшие альдегиды и кетоны, т. е. с выделением воды и образованием фенилгидразона:
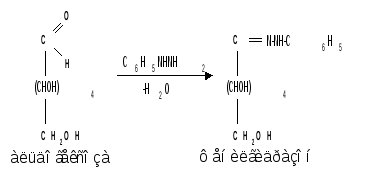
Затем при нагревании полученного гидразона с фенилгидразином соседняя с карбонильной группой первичная или вторичная спиртовая группа окисляется в карбонильную, причем фенилгидразин восстанавливается до анилина и аммиака. Вновь образовавшаяся карбонильная группа (для кетоз - альдегидная, а для альдоз - кетонная) вступает в реакцию с третьей молекулой фенилгидразина и получается озазон монозы :
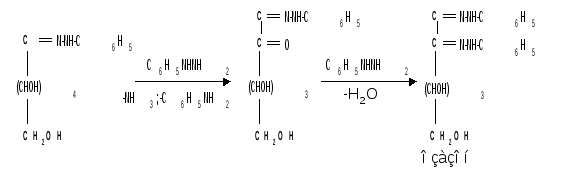
Из альдоз и кетоз могут получиться озазоны одинакового строения. Поскольку реакция образования озазона затрагивает только углероды С1 и С2 моносахаридов, то, следовательно, эпимерные альдозы и изомерные им кетозы дают один и тот же озазон.
Озазоны представляют собой кристаллические вещества, трудно растворимые в воде, благодаря чему их легко выделить в кристаллическом виде из водных растворов моноз.
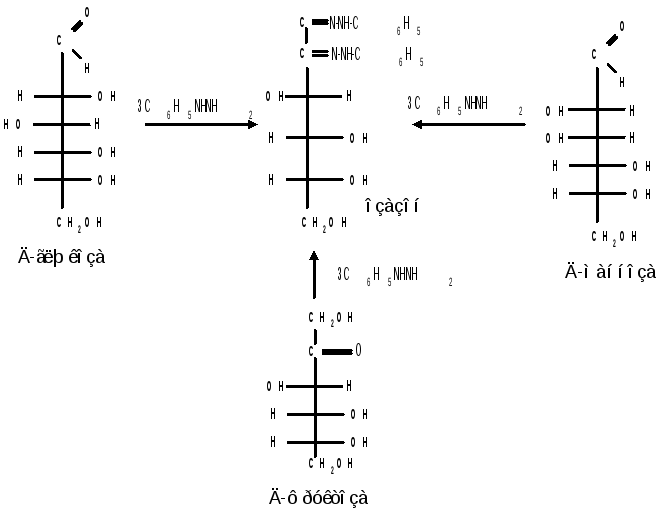
Озазоны при действии кислот гидролизуются в озоны :
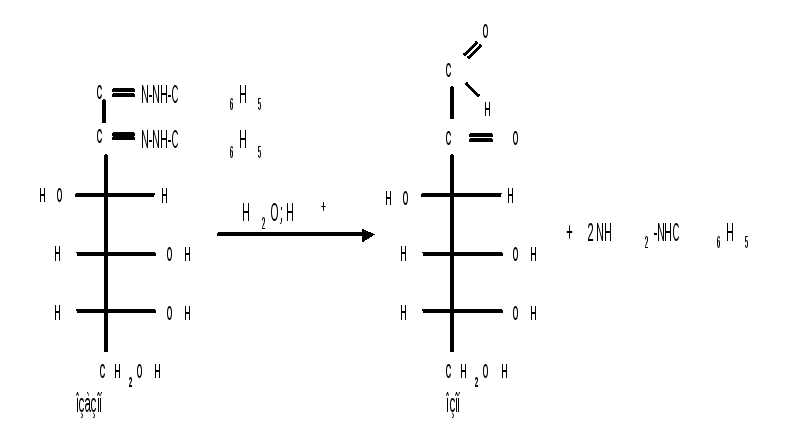
При восстановлении озонов амальгамой натрия в слабокислой среде происходит избирательное восстановление альдегидной группы до первичной спиртовой группы. Этим методом можно осуществлять переход от альдоз к кетозам через озазоны и озоны.
-
озон
кетогексоза
е) Действие щелочей. В разбавленных растворах щелочей при комнатной температуре происходит изомеризация моносахаридов, т.е. получение из одного моносахарида равновесной смеси моноз, отличающихся конфигурацией первого и второго атомов углерода.
Так, водный раствор Д-глюкозы после добавления к нему известковой воды через пять суток имеет состав : Д- глюкозы - 63,5 % , Д- маннозы - 2,5 % и Д-фруктозы - 31 %. Процесс изомеризации проходит через стадию образования промежуточного продукта - ендиола, который для глюкозы, маннозы и фруктозы является общим :
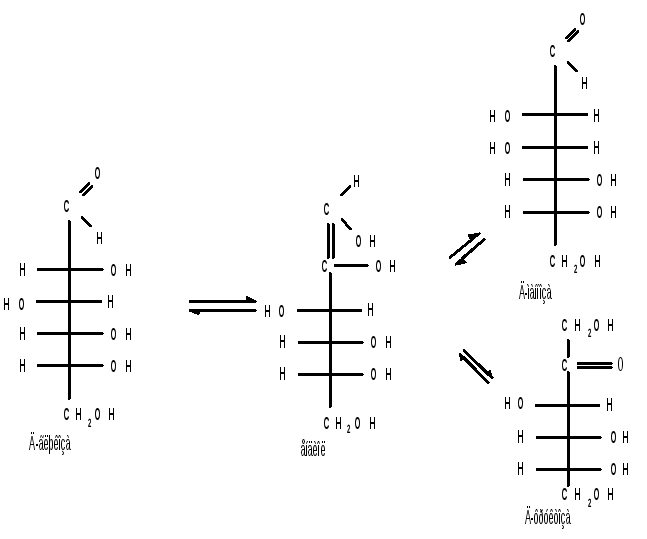
Происходящие при этих превращениях изменения конфигурации у второго углеродного атома альдоз носит название эпимеризации, а альдозы, отличающиеся лишь конфигурацией второго углеродного атома, называются эпимерами.
Способностью альдоз и кетоз к взаимному переходу друг в друга в слабощелочной среде обьясняются некоторые необычные свойства фруктозы, в частности - способность к положительным реакциям с реактивом Толленса и фелинговой жидкостью.
Превращение 6-фосфата-Д-глюкопиранозы в 6-фосфат-Д-фруктозы протекает в организме под действием фермента фосфоглюкоизомеразы и является одной из стадий катаболизма глюкозы.
8.2. Реакции с участием гидроксильных групп
Гидроксильные группы имеются в открытых и циклических формах моноз, но содержание циклических форм значительно выше, поэтому реакции идут в циклических ( полуацетальных ) формах :

Гидроксилы отличаются по реакционной способности : С1-ОН-гликозидный (наиболее реакционноспособный) ; С6 - первичный; С2-С4 - вторичные.
8.2.1 Реакции с участием гликозидного гидроксила
При взаимодействии моносахаридов с гидроксилсодержащими соединениями (спиртами, фенолами и др.) в условиях кислотного катализа образуются производные только по гликозидной ОН-группе - циклические ацетали, называемые гликозидами. Cпиртовые гидроксилы моноз в этих условиях не реагируют.
В зависимости от размера оксидного цикла гликозиды делятся на пиранозиды и фуранозиды. Ацетали глюкозы называют глюкозидами, рибозы - рибозидами, фруктозы - фруктозидами и т.п. (окончание - оза монозы заменяется на - озид). Растворы гликозидов не мутаротируют.
Удобным способом получения гликозидов является пропускание газообразного хлороводорода ( катализатор ) через раствор моносахарида в спиртах, например, этаноле, метаноле и т.д. При этом соответственно получаются этил- или метилгликозиды. В названии гликозидов указываются сначала наименования введенного радикала, затем конфигурация аномерного центра и название углеводного остатка с суффиксом - озид.
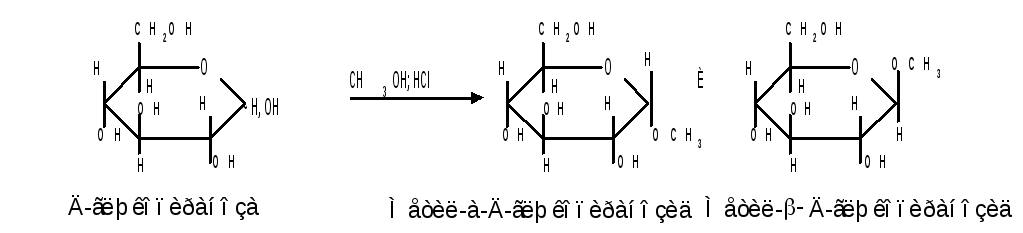
Вследствие таутомерии и обратимости реакции образования гликозида в растворе в равновесии в общем случае могут находиться таутомерные формы исходного моносахарида и соответственно 4 диастереомерных гликозида (- и-аномеры фуранозидов и пиранозидов).
Как и все ацетали, гликозиды легко гидрализуются разбавленными кислотами, но проявляют устойчивость к гидролизу в слабощелочной среде. Более напряженные пятичленные циклы фуранозидов расщепляются гидролитическим путем быстрее пиранозидов. Гидролиз гликозидов в кислой среде приводит к соответствующим спиртам и моносахаридам и представляет собой реакцию, обратную их образованию.
Для гидролитического расщепления гликозидов широко применяется ферментативный гидролиз, преимущество которого заключается в его специфичности. Например, фермент -глюкозидаза из дрожжей расщепляет только -глюкозидную связь; -глюкозидаза из миндаля - только -глюкозидную связь. На этом основании ферментативный гидролиз часто применяется в целях установления конфигурации аномерного атома углерода. Гидролиз гликозидов лежит в основе гидролитического расщепления полисахаридов, осуществляемого в организме, а также используется во многих промышленных процессах .
Молекулу гликозида формально можно представить состоящей из двух частей - углеводной и агликоновой. В роли гидроксилсодержащих агликонов могут выступать и сами моносахариды. Гликозиды, образованные с ОН- содержащими агликонами, называют О-гликозидами. В свою очередь гликозиды, образованные с NH- содержащими соединениями (например, аминами), называют N-гликозидами. К ним принадлежат нуклеозиды, имеющие важное значение в химии нуклеиновых кислот.
8.2.2 Реакции с участием всех гидроксильных групп
а) Алкилирование.
При действии на моносахариды более сильных алкилирующих агентов, например алкилгалогенидов, наряду с гликозидным гидроксилом в реакцию вступают все спиртовые гидроксилы монозы с образованием простых эфиров. Простые эфиры не гидролизуются, а гликозидная связь легко подвергается гидролитическому расщеплению в кислой среде.
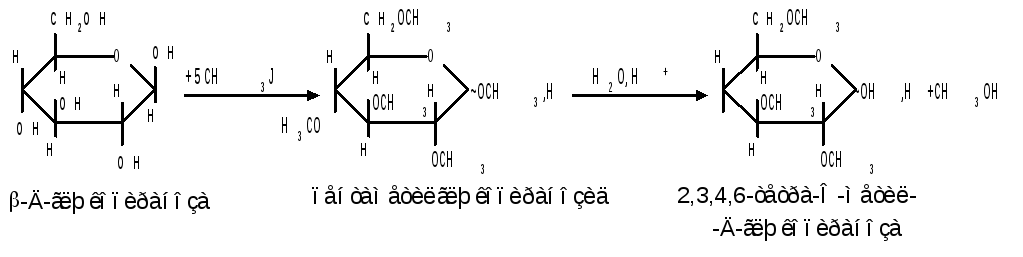
Большое практическое значение имеют триметилсилиловые эфиры моносахаридов (ТМС-эфиры). Моносахариды - нелетучие соединения, поэтому для анализа методами ГЖХ или масс - спектрометрии их необходимо перевести в летучие производные, например ТМС - эфиры, путем взаимодействия с триметилхлорсиланом (СН3)3SiCl.

б) Образование сложных эфиров. Моносахариды легко ацилируются ангидридами и галогенангидридами органических кислот, образуя сложные эфиры с участием всех гидроксильных групп. Например, при действии с уксусным ангидридом получаются ацетильные производные моносахаридов:
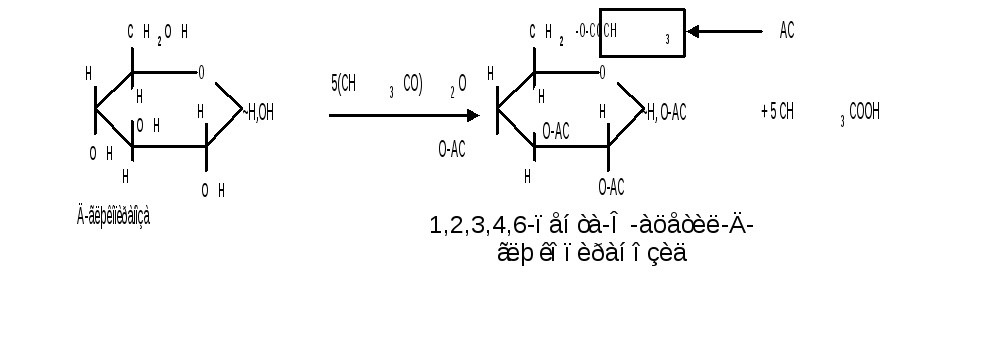
Сложные эфиры моноз гидролизуются как в кислой, так и щелочной средах.
Большое значение имеют эфиры неорганических кислот, в частности, эфиры фосфорной кислоты - фосфаты. Они содержатся во всех растительных и животных организмах и представляют собой метаболически активные формы моносахаридов. К ним прежде всего относят фосфаты Д-глюкозы и Д-фруктозы :
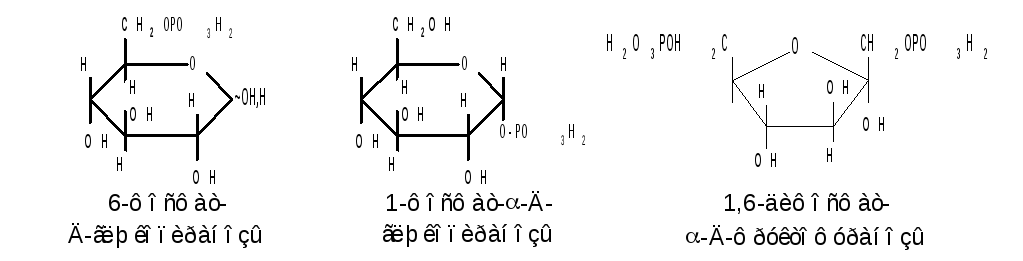
Фосфаты Д-рибозы и 2-дезокси-Д-рибозы служат структурными элементами нуклеиновых кислот и ряда коферментов.
8.3 Действие кислот
Действие кислот на пентозы и гексозы может быть использовано для их распознования, а именно: при нагревании пентоз с разбавленными кислотами легко происходит их дегидратация (отщепление трех молекул воды ) и образуется летучий гетероциклический альдегид - фурфурол :
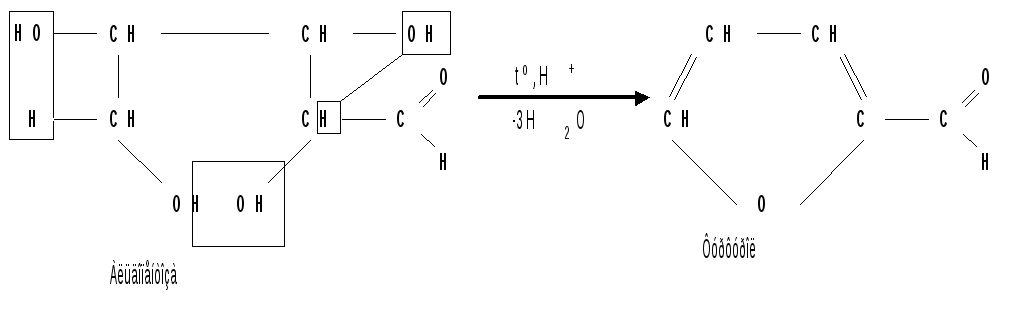
Действие кислот на гексозы ведет сначала к образованию 5-гидроксиметилфурфурола, который при кипячении с разбавленными кислотами разлагается с образованием левулиновой и муравьиной кислот:
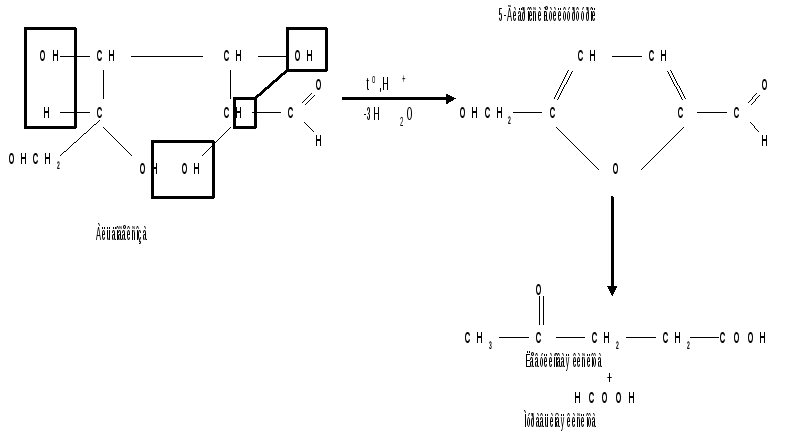
Фурфурол и 5-гидроксиметилфурфурол способны вступать в реакции конденсации с фенолами (-нафтол, резорцин, флороглюцин) и ароматическими аминами (анилин, дефиниламин) с образованием окрашенных продуктов. Фурфурол дает красное окрашивание с анилином (качественная реакция на пентозы); 5-гидроксиметилфурфурол - красное окрашивание с резорцином (реакция Селиванова).
Некоторые цветные качественные реакции используются в количественном (колориметрическом) определении сахаров, а также хроматографии для обнаружения моносахаридов.
8.4 Брожение сахаров
Брожение - это сложный процесс расщепления моносахаридов с выделением СО2 под действием ферментов. Брожению подвергаются сахара, у которых число атомов углерода кратно трем (гексозы).
Брожение гексоз различной конфигурации происходит с неодинаковой легкостью. Различают разные виды брожения :

Существуют и другие виды брожения.
Процессы брожения сахаров играют важную роль и широко используются в промышленности.
