
- •Кафедра химической технологии
- •Химия и биохимия углеводов.
- •Раздел I. Химия моносахаридов.
- •Содержание
- •Введение
- •1 Классификация и номенклатура
- •2 Химическое строение моносахаридов
- •3 Стереохимия
- •Цифры 4,3,2,1 означают падение старшинства атомных
- •4 Таутомерия моносахаридов в растворах
- •1) Кето-енольную и 2) кольчато-цепную или оксо-окси-таутомерию.
- •Мутаротация
- •6 Способы получения моносахаридов
- •7 Физические свойства моносахаридов
- •8 Химические свойства моносахаридов
- •Литература
- •Научный редактор профессор г.Н. Роганов
4 Таутомерия моносахаридов в растворах
Характерной особенностью моносахаридов является их ярко выраженная способность к таутомерным превращениям. Углеводы были исторически одними из первых веществ, для которых наблюдалось явление таутомерии. Вспомним, что таутомерия - это равновесная, обратимая, самопроизвольная изомерия, т.е. частный случай изомерии. Различают два вида изомерии моносахаридов в растворах :
1) Кето-енольную и 2) кольчато-цепную или оксо-окси-таутомерию.
Кето-енольная таутомерия моносахаридов. Происходит при действии щелочей и состоит в переходе карбонильной формы (альдегидной или кетонной) в енольную форму (точнее ендиольную) с двумя ОН-группами при атомах углерода, связанных двойной связью, т.е. в образовании ендиола общего для эпимерных моносахаридов. Благодаря кето-енольной таутомерии, эпимерные моносахариды могут превращаться друг в друга. Например, в щелочной среде фруктоза претерпевает таутомерное превращение в глюкозу, которая и реагирует с фелинговой жидкостью:
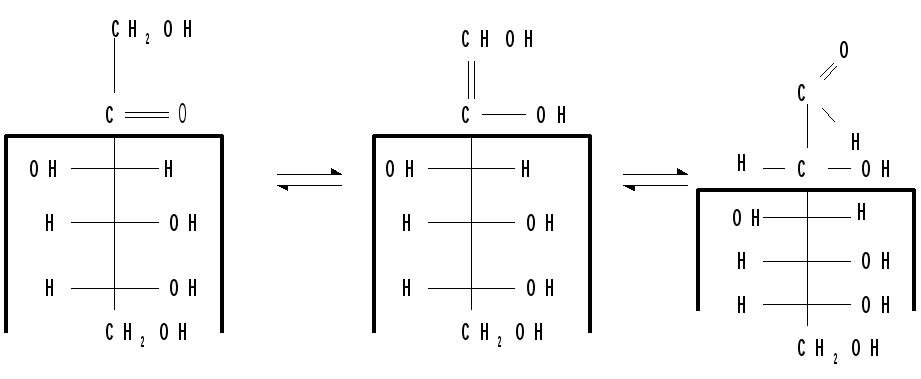
-
Д-фруктоза
Енол (ендиол)
Д-глюкоза
Кольчато- цепная (оксо-окси-) таутомерия моносахаридов. Заключается в существовании кольчатых (циклических) форм и цепной (т.е. с открытой углеродной цепью) формы моносахарида, находящихся в растворе в динамическом равновесии. Обычно циклические формы моносахаридов преобладают над открытой цепной формой. Например, известно, что в водных растворах глюкоза находится, главным образом, в виде - и- глюкопираноз, в меньшей степени - в виде- и-глюкофураноз и совсем небольшое количество глюкозы - в виде открытой, альдегидной формы (0.024 %). В целом пиранозные формы резко преобладают над фуранозными формами.
В растворах установление равновесия между четырьмя циклическими таутомерами моносахаридов протекает через открытую форму - оксо-форму:
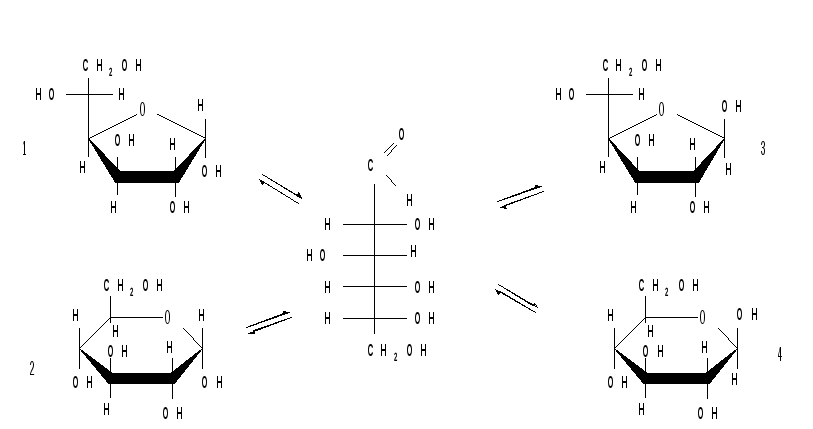
|
1 |
-Д-глюкофураноза |
2 |
-Д-глюкопираноза |
|
3 |
-Д-глюкофураноза |
4 |
-Д-глюкопираноза |
В зависимости от условий реакции и примененных реагентов моносахариды реагируют в одной из таутомерных форм : пиранозной, фуранозной или ациклической, оксо-форме, так как расходование одной из них в ходе реакции сдвигает таутомерное равновесии в сторону реагирующей формы. Например, несмотря на незначительное содержание оксо-формы, глюкоза вступает в реакции, характерные для альдегидной группы. Таутомерия лежит в основе множественности химических свойств моносахаридов. Аналогичные таутомерные превращения происходят в растворах со всеми моносахаридами и большинством известных дисахаридов. Так, для важнейшего представителя кетогексоз Д-фруктозы схема таутомерных превращений имеет следующий вид:

|
1 |
-Д-фруктопираноза |
2 |
-Д-фруктофураноза |
|
3 |
-Д-фруктопираноза |
4 |
-Д-фруктофураноза |
Мутаротация
Кольчато-цепная таутомерия моносахаридов является причиной любопытного свойства простых углеводов. В кристаллическом состоянии моносахариды находятся только в циклической форме. В зависимости от условий кристаллизуется либо -, либо -форма. Так, при кристаллизации из воды глюкоза получается в виде -Д-глюкопиранозы, а при кристаллизации из пиридина - в виде -Д-глюкопиранозы. После растворения -Д-глюкопиранозы в воде вначале наблюдается характерное для нее значение удельного вращения, равное [] = + 112,2 0. Однако при стоянии раствора эта величина постепенно снижается и наконец достигает устойчивого значения +52,50 . Это явление получило название мутаротации.
Мутаротация - явление самопроизвольного изменения угла вращения плоскости поляризации или изменение оптической активности при стоянии свежеприготовленного раствора сахара. Оно связано с тем, что в растворе устанавливается равновесие между циклическими - и -пиранозными формами, которые переходят друг в друга в результате раскрытия пиранозного цикла с образованием открытой оксо-формы. Следует отметить, что -Д- глюкопираноза имеет удельное вращение равное [] = +19,30 , а равновесная смесь обладает средним значением удельного вращения (+ 52,50) :
-
форма ![]() оксоформа
оксоформа ![]()
- форма
- форма
(+ 112,2 0) ( +52,50) ( + 19,3 0)
Взаимопревращение - и-аномеров друг в друга через промежуточную оксо-форму называется аномеризацией.
Конечное значение удельного вращения (+ 52,5 0) определяется равновесной смесью этих форм, при этом содержание оксо-формы мало и составляет лишь доли процента. Положение равновесия не зависит от того, из какой таутомерной формы - или - мы исходим.
