
- •Федеральное агентство по образованию Волгоградский государственный архитектурно-строительный университет
- •Волгоград 2010
- •Введение
- •Правила по технике безопасности
- •Лабораторная работа «комплексные соединения»
- •1. Теоретическая часть
- •1.1. Общие сведения о комплексных соединениях
- •1.2. Природа химической связи в комплексных соединениях
- •1.3. Устойчивость комплексного иона
- •1.4. Номенклатура комплексных соединений
- •2. Экспериментальная часть
- •Контрольные вопросы
- •Лабораторная работа «скорость химических реакций»
- •1. Теоретическая часть
- •1.1. Скорость гомогенных и гетерогенных реакций
- •1.2. Зависимость скорости химической реакции от концентрации
- •1.3. Зависимость скорости реакции от температуры
- •1. 4. Примеры решения задач
- •2. Экспериментальная часть
- •Контрольное задание
- •Контрольные вопросы
- •Лабораторная работа «катализ»
- •1. Теоретическая часть
- •1.1. Общие сведения о катализе
- •1.2. Гомогенный катализ
- •1.2. Гетерогенный катализ
- •2. Экспериментальная часть
- •Контрольные вопросы
- •Лабораторная работа «химическое равновесие»
- •1. Теоретическая часть
- •1.1. Обратимые и необратимые реакции
- •1.2. Химическое равновесие и вывод константы равновесия
- •1.3. Смещение химического равновесия. Принцип Ле Шателье
- •1. 4. Примеры решения задач
- •2. Экспериментальная часть
- •Контрольное задание
- •Контрольные вопросы
- •Лабораторная работа «ионообменные реакции»
- •1. Теоретическая часть
- •1.1. Электролитическая диссоциация; сильные и слабые электролиты
- •1.2. Принципы протекания ионообменных реакций
- •1. 3. Примеры решения задач
- •2. Экспериментальная часть
- •Контрольное задание
- •1.2. Влияние одноименных ионов на растворимость и солевой эффект
- •1.3. Растворимость осаждаемого соединения и образование осадков
- •1. 4. Примеры решения задач
- •2. Экспериментальная часть
- •Контрольные вопросы
- •Лабораторная работа «водородный показатель. Гидролиз солей»
- •1. Теоретическая часть
- •1.1. Диссоциация воды. Ионное произведение воды. Водородный показатель
- •1.2. Гидролиз солей
- •1.2. Степень гидролиза и константа гидролиза
- •1. 4. Примеры решения задач
- •2. Экспериментальная часть
- •Контрольные вопросы
- •Список рекомендуемой литературы
- •Дополнительная
- •400074, Волгоград, ул. Академическая, 1
Контрольные вопросы
Что такое гидролиз? В каких случаях и почему раствор соли имеет: а) нейтральную; б) кислую; в) щелочную реакцию?
Чем отличается гидролиз солей: а) многоосновных кислот от гидролиза солей одноосновных кислот; б) многовалентных металлов от гидролиза солей одновалентных металлов?
Какими способами можно усилить гидролиз, подавить гидролиз?
Вычислить рН растворов, содержащих: а)
 моль/л
Н+;
б) 0,008 моль/л
ОН–.
Ответ: а) 3,7; б) 11,9.
моль/л
Н+;
б) 0,008 моль/л
ОН–.
Ответ: а) 3,7; б) 11,9.Чему равны рН: а) 0,02н раствора НСООН (
 );
б) 0,05н раствораNH4OH
(
);
б) 0,05н раствораNH4OH
( )?
Ответ: а) 3,22; б) 10,98.
)?
Ответ: а) 3,22; б) 10,98.Как изменится рН 0,1н растворов HCl и КОН при разбавлении их в 100 раз?
Вычислите величину константы гидролиза: а) NH4Cl, б) NH4CN. Ответ: а)
 ;
б) 0,78.
;
б) 0,78.Вычислите степень гидролиза солей: а) NH4Cl, б)NH4CN, если концентрация их 0,1М. Ответ: а)0,0074; б)46,8.
Вычислите рН: а) 0,1н раствора НСN, если
 и б) 1н раствораNH4ОН,
и б) 1н раствораNH4ОН,
 .
Ответ: а) 5,15; б) 11,62.
.
Ответ: а) 5,15; б) 11,62.Определите концентрации ионов Н+ и ОН– в растворах, водородный показатель которого равен 3,2. Ответ:
 моль/л;
моль/л;
 моль/л.
моль/л.Рассчитайте рН раствора, содержащего в 1л 0,02 моля HCl и 0,15 моля KCl. Ответ: 1,78.
Найдите водородные показатели следующих концентрированных растворов сильных электролитов: а) 0,15М HСlO3; б) 0,205н HCl. Ответ: а) 0,9; б) 0,77.
Вычислите рН 0,05 раствора HNO3. Плотность раствора и степень диссоциации HNO3 считать равными единице. Ответ: 2,1.
Сколько граммов НСООН (
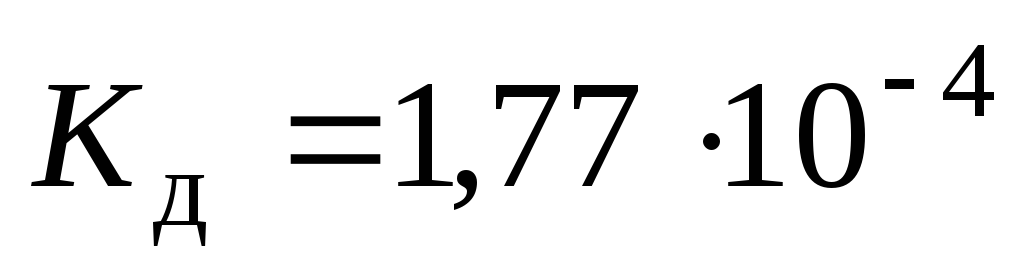 )содержится
в 0,3 л раствора этой
кислоты, имеющей рН=6,04? Ответ:
)содержится
в 0,3 л раствора этой
кислоты, имеющей рН=6,04? Ответ:
 г.
г.Рассчитайте молярность раствора СН3СООН, рН которого равна 3 (
 ).
Ответ: 0,06М.
).
Ответ: 0,06М.Определите рН раствора 0,3 л которого содержит
 моль
ионов ОН–.
Ответ: 9,2.
моль
ионов ОН–.
Ответ: 9,2.Рассчитайте рН раствора, в 0,4 л которого содержится 0,39 моля NH3, если
 .
Ответ: 11,6.
.
Ответ: 11,6.
Список рекомендуемой литературы
1. Коровин Н. В. Общая химия : Учеб. для технич. направ. и спец. вузов. — М. : Высш. шк., 2007. — 556 с. (также предыдущие издания)
2. Глинка Н. Л. Общая химия : Учеб. пособие для вузов. — М. : Интеграл-ПРЕСС, 2008. — 728 с. (также предыдущие издания)
3. Дробашева Т. И. Общая химия : Учеб. для втузов. — Ростов н/Д : Феникс, 2007. — 448 с.
4. Глинка Н. Л. Задачи и упражнения по общей химии : Учеб. пособие для нехим. специальностей вузов. — М. : Интеграл-ПРЕСС, 2006. — 240 с. (также предыдущие издания)
5. Лидин Р. А. Задачи по неорганической химии : Учебн. пособие для хим.-технол. вузов / Р. А. Лидин, В.А. Молочко, Л. Л. Андреева ; под ред. Р. А. Лидина. — М. : Высш. шк., 1990. — 319 с.
Дополнительная
6. Ахметов Н. С. Общая и неорганическая химия : Учеб. для вузов — М. : Высш. шк., Изд. центр «Академия», 2001. — 743 с. (также предыдущие издания)
7. Хомченко И. Г. Общая химия : Учеб. для нехим. вузов — М. : Новая Волна; ОНИКС, 2001. — 463 с.
Учебное издание
Химия : лабораторный практикум
Подписано в печать ХХ.ХХ.ХХ. Формат 60х84/16.
Бумага офсетная. Печать трафаретная. Гарнитура Таймс.
Уч.-изд. л.4,04. Усл. печ. л. 5,41. Тираж 300 экз. Заказ № _____
Государственное образовательное учреждение высшего профессионального образования
«Волгоградский государственный архитектурно-строительный университет»
Сектор оперативной печати ЦИТ
