
- •Введение
- •I.2. Выбор кардиостимулятора
- •I.3. Моноэлектродные системы VDD
- •I.5. Электроды для стимулирующих систем
- •I.6. Наблюдение пациентов с кардиостимуляторами
- •I.7. Кардиостимуляция при приобретенной атриовентрикулярной блокаде у взрослых
- •I.9. Кардиостимуляция при инфаркте миокарда
- •I.11. Предотвращение и прекращение тахиаритмий методом электрокардиостимуляции
- •I.12. Кардиостимуляция при рефлекторных синкопальных состояниях (также см. главу 2)
- •I.13. Кардиостимуляция у детей, подростков и пациентов с врожденными пороками сердца
- •I.14. Кардиостимуляция при специфических состояниях
- •Список литературы
- •II.2. Эпидемиология и факторы риска ВСС
- •II.3. Концепция профилактики внезапной сердечной смерти.
- •II.4. Эффективность ИКД-терапии по результатам клинических исследований
- •II.5. Последние достижения в ИКД-терапии
- •II.6. Использование антитахикардийной стимуляции (АТС) в ИКД
- •II.7. Применение ИКД у детей: особенности и показания.
- •Список литературы
- •III.1. Введение
- •III.2. Понятие о сердечной диссинхронии. Механизмы сердечной ресинхронизации
- •III.3. Технические аспекты сердечной ресинхронизации
- •III.4. Обоснование применения СРТ при ХСН с точки зрения доказательной медицины
- •III.5. Об эффективности сердечной ресинхронизации у больных с фибрилляцией предсердий
- •III.6. Сердечная диссинхрония и СРТ у больных с имплантированными кардиостимуляторами
- •III.7. О комбинации сердечной ресинхронизации и имплантируемых кардиовертеров-дефибрилляторов
- •III.8. Показания для СРТ
- •III.9. Применение эхокардиографии при СРТ
- •III.10. Некоторые дискуссионные и малоизученные вопросы, связанные с СРТ
- •III.11. Экономические аспекты сердечной ресинхронизации и кардиоверсии-дефибрилляции
- •Список литературы
- •IV.1. Описание устройств.
- •IV.2. Применение имплантируемых кардиомониторов у пациентов с обмороками неясного генеза.
- •IV.3. Имплантируемые кардиомониторы у пациентов с недиагностированными симптомными тахикардиями.
- •IV.4. Применение имплантируемых кардиомониторов у пациентов с фибрилляцией предсердий.
- •IV.5. Перспективы
- •Список литературы
- •Введение
- •I.2. Классификация и патофизиология
- •I.3. Эпидемиология
- •I.4. Прогноз
- •I.5. Влияние на качество жизни
- •I.6. Экономические аспекты
- •II.1. Первичное обследование
- •II.2. Методы диагностики
- •III.1. Лечение рефлекторного обморока и ортостатической гипотонии
- •III.2. Аритмогенные обмороки
- •III.3. Обмороки при органических заболеваниях сердца и сердечно-сосудистых заболеваниях
- •III.4. Обмороки неясного генеза у пациентов с высоким риском внезапной сердечной смерти
- •IV.1. Обмороки у пожилых людей
- •IV.2. Обмороки у детей
- •IV.3. Вождение автомобиля и обмороки
- •V.3. Отделения для пациентов с обмороками (преходящей потерей сознания)
- •Список литературы
- •(комментарии к обновленной версии рекомендаций ESC по диагностике и лечению обмороков)
- •Список литературы
- •V.1. Дифференциальная диагностика тахикардий с узкими комплексами QRS
- •V.2. Неотложная терапия тахикардии с узкими комплексами QRS
- •V.3. Специфические тахикардии с узкими комплексами QRS
- •VIII.1. Фармакологическое лечение больных с синдромом WPW
- •VIII.2. Катетерная абляция больных с синдромом WPW.
- •XIII.1. Желудочковые аритмии
- •XIII.2. Наджелудочковые аритмии.
- •XV.1. Радиочастотная катетерная абляция или модификация атриовентрикулярного соединения для контроля частоты сокращений желудочков при предсердных тахиаритмиях.
- •XV.2. Радиочастотная катетерная абляция при aтриовентрикулярной узловой реципрокной (re-entry) тахикардии (АВУРТ)
- •XV.3. Радиочастотная катетерная абляция при предсердной тахикардии, трепетании и фибрилляции предсердий.
- •XV.4. Радиочастотная катетерная абляция дополнительных путей.
- •XV.5. Радиочастотная катетерная абляция при желудочковой тахикардии.
- •XV.6. Радиочастотная катетерная абляция тахиаритмий у детей в возрасте до 5 лет.
- •XVI.3. Тахикардии у детей.
- •XVI.4. Полная атриовентрикулярная блокада.
- •Список литературы
- •II.1. Эпидемиология
- •II.2. Механизмы фибрилляции предсердий
- •III.2. Выявление фибрилляции предсердий
- •III.3. Естественное течение фибрилляции предсердий
- •III.4. ЭКГ методы диагностики и мониторирования фибрилляции предсердий
- •III.5. Типы фибрилляции предсердий и другие определения
- •III.6. Первоначальное ведение больных
- •III.7. Наблюдение
- •IV.1. Антитромботическая терапия
- •IV.2. Контроль частоты сердечных сокращений и ритма сердца.
- •IV.3. Длительная терапия
- •IV.4. Дополнительная терапия
- •V.1. Сердечная недостаточность
- •V.2. Спортсмены
- •V.3. Пороки клапанов сердца
- •V.4. Острый коронарный синдром
- •V.5. Сахарный диабет
- •V.6. Пожилые
- •V.7. Беременность
- •V.8. Послеоперационная фибрилляция предсердий
- •V.9. Гипертиреоз
- •V.10. Синдром Вольфа-Паркинсона-Уайта
- •V.11. Гипертрофическая кардиомиопатия
- •V.12. Заболевание легких
- •Список литературы

ГЛАВА 1 РАЗДЕЛ III
брилляции (СРТ-ИКД) составляет 6-9 лет, после чего обычно требуется замена прибора.
III.4. Обоснование применения СРТ при ХСН с точки зрения доказательной медицины
Многочисленные многоцентровые рандомизированные исследования с участием около 15000 больных доказали эффект СРТ в отношении улучшения сердечных функций и эффективности работы сердца, улучшения качества жизни, увеличения продолжительности жизни, снижения частоты госпитализаций по поводу ХСН, смертности от ХСН и общей смертности [29, 30, 31, 32, 33, 34, 35, 36].
Данные девятнадцати рандомизированных контролируемых исследований (4510 пациентов с ХСН III или IV класса по классификации NYHA) были обобщены в мета-анализе, опубликованном в 2011 г. Al-Majed N.S. и соавт. [37]. Все больные были со сниженной ФВ левого желудочка (<40%) и удлиненным QRS. СРТ привела к достоверному увеличению ФВ левого желудочка, улучшению качества жизни, оцениваемого по Миннесотскому опроснику для больных с сердечной недостаточностью. Количество госпитализаций по поводу ХСН уменьшилось на 35%. Общая смертность уменьшилась на 22%, причем в основном за счет уменьшения смертности от прогрессирования ХСН.
Авторы сделали вывод о том, что СРТ улучшает функциональный и гемодинамический статус, уменьшает количество госпитализаций по поводу ХСН и смертность от всех причин.
Мета-анализ, проведенный по очень жестким критериям, включивший 5 рандомизированных многоцентровых исследований, 2292 больных, подтвердил достоверное влияние СРТ на общую смертность (уменьшение на 29%), на смертность вследствие сердечной недостаточности (уменьшение на 38%), на количество госпитализаций по поводу сердечной недостаточности (уменьшение на 54%) [38].
Справедливости ради следует отметить, что корректность дизайна некоторых многоцентровых исследований была не бесспорна. Не всегда планировались четкие и надежные конечные точки исследований. Проведенные многоцентровые исследования, конечно, оценивали эффект СРТ в особо отобранных группах больных, которые отличались от реальной популяции больных с ХСН. Особенно это касается потенциальной возможности возникновения осложнений СРТ. Безусловно, плацебо-эффект бивентрикулярной стимуляции существует, и его нужно учитывать в оценке реальной эффективности метода. Недостаточно
100

КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ, ИМПЛАНТИРУЕМЫХ КАРДИОВЕРТЕРОВДЕФИБРИЛЛЯТОРОВ, УСТРОЙСТВ ДЛЯ СЕРДЕЧНОЙ РЕСИНРОНИЗИРУЮЩЕЙ ТЕРАПИИ И ИМПЛАНТИРУЕМЫХ КАРДИОМОНИТОРОВ
проработаны вопросы безопасности вмешательств, например, возможность удаления левожелудочкового электрода в случае инфицирования.
Приводим описание одного из крупных исследований, во многом определившего современные показания для СРТ.
Исследование CARE-HF.
Исследование проспективное, параллельное, рандомизированное многоцентровое международное.
Цель.
•Оценить эффект добавления СРТ к оптимальной фармакологической терапии на проявления заболевания и смертность у пациентов с умеренной и выраженной сердечной недостаточностью вследствие систолической дисфункции левого желудочка, осложненной сердечной диссинхронией.
•Изучить механизмы, лежащие в основе наблюдаемых эффектов для выявления маркеров прогноза успеха или неудачи СРТ.
•Оценить отдаленные результаты и экономические последствия.
Дизайнисследования.
• Выборка: 813 пациентов (январь 2001 — март 2003);
––82 центра в 12 странах: Австрия, Бельгия, Дания, Финляндия, Франция, Германия, Италия, Нидерланды, Испания, Швеция, Швейцария и Великобритания.
•Успешная имплантация была осуществлена в 96% случаев.
•Среднее время госпитализации при имплантации – 4 дня.
•Длительность изучения от момента рандомизации в среднем составила 29,4 месяца.
Конечныеточки.
•Первичной конечной точкой исследования являлась комбинация «смерть от всех причин или госпитализация вследствие основных сердечно-сосудистых событий», анализируемая по времени от рандомизации до наступления первого события. Вторичной конечной точкой была смертность от всех причин. Дополнительными вторичными конечными точками были: дина-
101

ГЛАВА 1 РАЗДЕЛ III
мика класса ХСН по классификации NYHA; качество жизни через 90 дней; сердечная функция; нейроэндокринные параметры.
Основныекритериивключенияиисключенияизисследования.
•ХСН, требующая назначение в течение 6 последних недель петлевых диуретиков для купирования симптомов;
•ХСН класс III/IV (NYHA);
•оптимально скоррегированная лекарственная терапия «высокого стандарта», включавшая ингибиторы АПФ или блокаторы рецепторов к ангиотензину и антагонисты альдостерона;
•систолическая дисфункция левого желудочка и дилатация левого желудочка:
––ФВ ≤ 35%; конечный диастолический диаметр > 30 мм/рост; ––QRS ≥ 120 мс;
––диссинхрония, подтвержденная данными эхокардиографии при длительности QRS от 120 до 149 мс:
––задержка предызгнания из аорты > 140 мс;
––межжелудочковая механическая задержка > 40 мс;
––задержка активации задне-боковой стенки левого желудочка. Пациенты с фибрилляцией предсердий, стимулятор-зависимые
пациенты исключались.
Результаты.
Присоединение СРТ к оптимальной лекарственной терапии привело к уменьшению комбинированного показателя смертность+госпитализация по поводу сердечно-сосудистых болезней (уменьшение риска на 34%, p<0,001) вне зависимости от влияния разновидности лекарственного воздействия и других параметров. Уровень общей смертности в группе с лекарственной терапией оказался ниже ожидаемого (на 25% через два года наблюдения), вероятно, за счет оптимального подбора лекарств. Но, несмотря на это, к концу наблюдения в группе СРТ относительное снижение риска смертности достигло 36%, (p<0,002), риск смерти или госпитализации по поводу сердечной недостаточности были меньше в СРТ-группе на 46% (p<0,001).
При оценке симптоматики через 90 дней было показано, что в группе СРТ средний ФК сердечной недостаточности достоверно улучшился, и тяжесть ХСН была достоверно ниже, чем в группе с лекарственной терапией (p<0,0001), а качество жизни, оцениваемое по
102
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ, ИМПЛАНТИРУЕМЫХ КАРДИОВЕРТЕРОВДЕФИБРИЛЛЯТОРОВ, УСТРОЙСТВ ДЛЯ СЕРДЕЧНОЙ РЕСИНРОНИЗИРУЮЩЕЙ ТЕРАПИИ И ИМПЛАНТИРУЕМЫХ КАРДИОМОНИТОРОВ
стандартным опросникам, в группе СРТ было выше (p<0,0001). Через 18 месяцев пациенты из группы СРТ в сравнении с пациен-
тами контрольной группы имели:
•меньшую межжелудочковую механическую задержку
(p<0,0001);
•увеличение ФВ левого желудочка (на 7%, p<0,0001);
•снижение выраженности митральной регургитации (p=0,003);
•уменьшение объема желудочков (p<0,0001);
•увеличениесистолическогоартериальногодавления(p<0,0001);
•снижение уровня NT-pro-BNP (p=0,0016).
Итак, исследование CARE-HF продемонстрировало достоверные результаты по следующим позициям:
•улучшение сердечных функций и эффективности работы сердца;
•улучшение качества жизни;
•увеличение продолжительности жизни;
•снижение частоты госпитализаций по поводу ХСН, смертности от
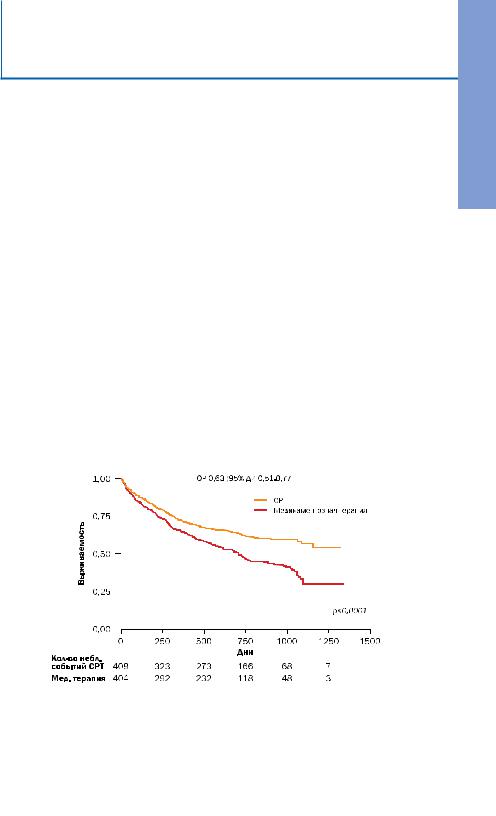
ХСН и общей смертности (рис. 1-2).
Все это позволило сделать вывод о том, что у больных с ХСН и сердечной диссинхронией сердечная ресинхронизация улучшает симптоматику, качество жизни, уменьшает осложнения и риск смерти. СРТ необходимо рассматривать как часть обычной терапии у пациентов
Рисунок 1. CARE-HF. Первичные конечные точки (Смерть вследствие всех причин или не планируемая госпитализация вследствие сердечно-сосудистых причин): ДИ – доверительный интервал.
103
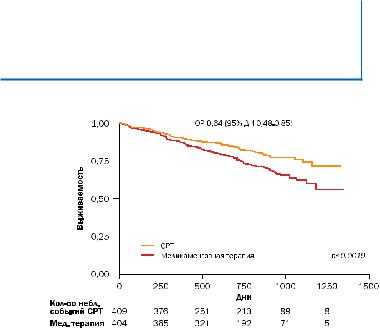
ГЛАВА 1 РАЗДЕЛ III
Рисунок 2. CARE-HF. Смертность вследствие всех причин.
с умеренной и выраженной ХСН и диссинхронией левого желудочка, подтвержденной данными эхокардиографии, как дополнение к медикаментозному лечению [34, 39].
Еще до окончания основной фазы исследования CARE-HF, не зная его результатов, комитет, управляющий исследованием, предположил, что за основной период исследования не удастся получить значимые результаты в отношении показателя общей смертности, и принял решение продлить исследование еще примерно на 8 месяцев. И хотя значимые результаты были получены уже после основной фазы исследования, это дало возможность дополнительно изучить эффекты СРТ.
Основной целью продленной фазы было оценить отдаленные эффекты СРТ на смертность и ее причины.
Средний срок наблюдения больных после имплантации составил 37,4 месяца.
Применение СРТ ассоциировалось с уменьшением риска смертности от всех причин на 40%, с уменьшением риска смертности от сердечной недостаточности на 45% и с уменьшением риска внезапной смерти на 46%.
Таким образом, было показано, что положительный эффект СРТ, наблюдаемый в основном исследовании, сохранялся или усиливался при увеличении времени наблюдения. Уменьшение смертности происходило как за счет уменьшения смертности от сердечной декомпен-
104

КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ, ИМПЛАНТИРУЕМЫХ КАРДИОВЕРТЕРОВДЕФИБРИЛЛЯТОРОВ, УСТРОЙСТВ ДЛЯ СЕРДЕЧНОЙ РЕСИНРОНИЗИРУЮЩЕЙ ТЕРАПИИ И ИМПЛАНТИРУЕМЫХ КАРДИОМОНИТОРОВ
сации, так и за счет уменьшения частоты внезапной смерти.
Эти данные характеризуют стойкость обратимости ремоделирования левого желудочка, характерной для СРТ, в течение длительного времени наблюдения, причем как у пациентов с ишемической, так и неишемической этиологией поражения миокарда [40, 41].
Были получены убедительные результаты СРТ в подгруппе больных с сахарным диабетом [42].
Последние опубликованные данные об отдаленных эффектах исследования CARE-HF (свыше 8 лет наблюдения) свидетельствуют о стойком положительном влиянии СРТ на отдаленную смертность у больных с ХСН. Общая смертность в группе СРТ была на 27% ниже, чем в группе контроля (p=0,007) [43].
Обобщая данные многочисленных публикаций, отражающих как опыт отдельных клиник, так и обширный пласт многоцентровых исследований, сегодня можно говорить о высоком уровне доказательств эффекта СРТ при лечении ХСН. Этот эффект реализовывается не только уменьшением симптомов ХСН, но и улучшением прогноза, то есть увеличением продолжительности жизни и уменьшением смертности.
Однако следует помнить о том, что, как показали результаты регистра PANORAMA в России, популяция пациентов с ХСН и имплантированными устройствами для СРТ-ЭКС и СРТ-ИКД в России существенно отличается по многим демографическим и клиническим характеристикам от популяции пациентов, вошедших в основные многоцентровые исследования и регистры за рубежом. Для российских больных с ХСН характерен более молодой возраст, более выраженная тяжесть ХСН, большая доля больных с фибрилляцией предсердий и др. Следует с осторожностью трактовать зарубежные данные, касающихся СРТ, при переносе их на российскую почву. Однако краткосрочная и долгосрочная эффективность СРТ у российских больных ХСН также была подтверждена многими отечественными исследованиями [44-48].
По результатам проведенных исследований были сформулированы основные критерии отбора больных для СРТ, с небольшой коррекцией использовавшиеся в течение последних десяти лет (больные с ХСН III-IV функционального класса по классификации NYHA, ФВ левого желудочка менее или равной 35%, несмотря на оптимальную медикаментозную терапию, при наличии синусового ритма и величине комплекса QRS равной или более 120 мс). Однако, данные, полученные в результате последних многоцентровых исследований, привели к суще-
105

ГЛАВА 1 РАЗДЕЛ III
ственному пересмотру критериев отбора больных.
Недавно были опубликованы данные нескольких рандомизированных многоцентровых исследований, рассматривающие возможность применения сердечной ресинхронизации у больных с умеренной
идаже незначительной клинической выраженностью ХСН.
Висследование по влиянию ресинхронизации на обратное ремоделирование при нарушении систолической функции левого желудоч-
ка (Resynchronization Reverses Remodeling in Systolic Left Ventricular Dysfunction(REVERSE)быловключено610пациентовсХСНIIФКпоклассификации NYHA и пациентов I ФК с симптомами ХСН в анамнезе, QRS≥120 мс и ФВ левого желудочка ≤40% [49]. Первичной конечной точкой был смешанный клинический ответ, согласно которому пациенты были разделены на пациентов с улучшением, отсутствием изменений или ухудшением в течение относительно короткого периода наблюдения в 12 месяцев. Первичная конечная точка указала на 16%-ное ухудшение в группе CRT-ON (активной СРТ) по сравнению с 21% в группе CRT-OFF (группе контроля) (p=0,10). При вторичном анализе время до первой госпитализации по поводу ХСН в течение 12-месячного периода наблюдения в группе CRT-ON было гораздо больше (отношение рисков (ОР): 0,47; p=0,03).
Европейские исследователи этого трайла наблюдали 262 пациентов в течение 24 месяцев, и обнаружили, что доля больных с ухудшением была значительно меньше в группе CRT-ON в сравнении с группой CRT-OFF (19% и 34%, соответственно, p=0,01) [50]. В Европейской когорте время до первой госпитализации по поводу ХСН или смерти было значительно больше у пациентов с СРТ (ОР: 0,38; p=0,003).
Многоцентровое исследованиепо имплантации автоматических дефибрилляторов – сердечной ресинхронизирующей терапии (Multicenter Automatic Defibrillator Implantation Trial-Cardiac Resynchronization Therapy (MADIT-CRT) было первым большим рандомизированным исследованием, в котором была поставлена цель сравнить эффективность комбинации СРТ+ИКД с эффективностью изолированного применения ИКД в снижении риска клинической конечной точки (событие, связанное с ХСН, или смерть) у больных с легкой или средней выраженностью ХСН [51]. Событие, связанное с ХСН определялось как госпитализация по поводу ХСН (87% всех событий ХСН) или амбулаторное лечение ХСН (оставшиеся 13%). В исследование было включено 1820 пациентов с ишемической (ХСН I-II ФК по NYHA) и неишемической (ХСН II ФК по NYHA) кардиомиопатией с ФВ левого желудочка ≤30% и QRS≥130 мс. Первичная конечная точка была достигнута у 17,2% пациентов в группе
106

КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРИМЕНЕНИЮ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОВ, ИМПЛАНТИРУЕМЫХ КАРДИОВЕРТЕРОВДЕФИБРИЛЛЯТОРОВ, УСТРОЙСТВ ДЛЯ СЕРДЕЧНОЙ РЕСИНРОНИЗИРУЮЩЕЙ ТЕРАПИИ И ИМПЛАНТИРУЕМЫХ КАРДИОМОНИТОРОВ
СРТ+ИКД по сравнению с 25,3% в группе ИКД: снижение на 34% риска развития события, связанного с ХСН, или смерти (ОР в группе СРТ+ИКД: 0,66; p=0,001). Комбинация СРТ+ИКД привела к значительному снижению (на 41%) риска развития событий, в то время как не было отмечено значительной разницы в смертности между группами.
Бóльшая эффективность СРТ+ИКД отмечена у пациентов с широким QRS (≥150 мс) и у женщин, чем у мужчин и пациентов с QRS<150 мс. Дальнейший анализ выявил, что пациенты с блокадой левой ножки пучка Гиса (БЛНПГ), составляющие до 70% из включенных в исследование, показали значительное улучшение от лечения СРТ+ИКД, в то время как пациенты с широким комплексом QRS и блокадой правой ножки пучка Гиса (БПНПГ) или нарушением внутрижелудочковой проводимости (НВП) (независимо от ширины QRS) не продемонстрировали снижения частоты первичных событий [52, 53].
Значение БЛПГ и удлинения QRS≥150 мс для предсказания обратимости ремоделирования левого желудочка было доказано также с помощью мультивариантного анализа [54].
Эти же параметры оказались среди шести, предсказывавших «суперответ» (увеличение ФВ≥14.5%) на СРТ [55]. БЛНПГ была основным параметром, предсказывающим уменьшение общей смертности в этой группе больных [56].
В исследование RAFT (Resynchronization/Defibrillation for Ambulatory Heart Failure Trial) [36] было рандомизировано 1798 пациентов с ХСН II-III
ФК по NYHA, с ФВ левого желудочка ≤30% и продолжительностью базового комплекса QRS≥120 мс или стимулированного QRS≥200 мс в соотношении 1:1 на имплантацию только ИКД или ИКД+СРТ. Аналогично с исследованием MADIT-CRT первичной конечной точкой была определена ХСН, потребовавшая госпитализации, или смерть. Риск первичной конечной точки был значительно снижен — на 25% (ОР: 0,75; p<0,001), с 40,3% в группе ИКД до 33,2% в группе ИКД+СРТ (рис.2). В то же самое время смертность также снизилась до 25% (ОР: 0,75; p=0,003) с 26,1% в группе ИКД до 20,8% у пациентов группы ИКД+СРТ. Поскольку в исследование RAFT были включены 80% пациентов с ФК II по NYHA и 20% с ФК III, авторы провели дополнительный анализ в этих двух подгруппах, который показал, что когда анализ ограничивался только пациентами ФК II по NYHA, снижение сердечных событий было все равно значительным: на 27% снизилась частота первичных конечных точек, на 29% — смертности. Дополнительный анализ подгрупп продемонстрировал бóльшую эффективность ИКД+СРТ у пациентов с длительностью комплекса QRS≥150 мс, чем при
107

ГЛАВА 1 РАЗДЕЛ III
QRS<150 мс и у пациентов с БЛНПГ в сравнении с пациентами с БПНПГ, НВП и со стимулированным QRS. Женщины также показали бóльшую эффективность по сравнению с мужчинами.
Таким образом, результаты проведенных многоцентровых исследований продемонстрировали эффективность СРТ у больных с незначительной и умеренной клинической выраженностью ХСН, сниженной ФВ левого желудочка и удлинением комплекса QRS. Это нашло свое отражение в новой редакции показаний к СРТ, рекомендованных европейскими и американскими экспертами.
В мета-анализе, построенном на пяти рандомизированных много-
центровых исследованиях (COMPANION, CARE-HF, MADIT-SRT, REVERSE, RAFT – 5813 больных), где оценивалось взаимосвязь длительности комплекса QRS с эффектами СРТ, было продемонстрировано достоверное снижение количества комплексных клинических точек (смерть или госпитализация по поводу ХСН и др.) только в группе пациентов с широким (более 150 мс) QRS – на 40% (p<0,001). При умеренном увеличении длительности QRS достоверного влияния СРТ на клинические события продемонстрировано не было [57].
Эти данные нашли свое подтверждение в другом мета-анализе [58]. Для оценки влияния морфологии QRS на эффекты СРТ были использованы данные четырех рандомизированных многоцентровых исследова-
ний (COMPANION, CARE-HF, MADIT-SRT B RAFT) с участием 5356 боль-
ных. Было показано, что только пациенты с БЛПГ продемонстрировали снижение частоты достижения комплексной клинической точки (смерть или госпитализация по поводу ХСН и др.) неблагоприятных клинических событий (на 36%, p=0,00001). Ни у пациентов с блокадой правой ножки пучка Гиса, ни у пациентов с другими нарушениями межжелудочковой проводимости такого эффекта не было отмечено [59].
Мета-анализ 5 многоцентровых исследований, включающий 4317 пациентов с NYHA ФК I/II продемонстрировал более низкую общую смертность у больных с СРТ по сравнению с больными с имплантированными ИКД (на 29%, p=0,04), меньшую частоту госпитализаций по поводу ХСН (на 32%, p<0,001), достоверно большее увеличение ФВ и уменьшение объема левого желудочка. У пациентов II ФК СРТ ассоциировалась с достоверно более низким значением комплексного показателя «смертность-госпитализация» (на 27%, p<0,001), бессимптомные пациенты с I ФК продемонстрировали сниженный риск госпитализации (на 43%, p=0,04) без отличия в уровнях смертности. Был сделан вывод о том, что у пациентов с NYHA ФК I/II СРТ уменьшает общую смертность,
108
