
- •ОРГАНИЧЕСКАЯ
- •Рекомендуемая литература
- •Перечень пособий, методических указаний к проведению учебных занятий и самостоятельной работы студентов
- •Дополнительная литература
- •СТРУКТУРА КУРСА
- •Цель курса
- •ОРГАНИЧЕСКАЯ ХИМИЯ
- •Органическая химия – это химия соединений углерода
- •Основные этапы развития химии
- •ОСНОВЫ ТЕОРИИ СТРОЕНИЯ
- •Бутлеров Александр Михайлович (1828-1886)
- •Структурная теория А.М.Бутлерова
- •Структурная теория А.М.Бутлерова
- •Основные положения теории строения органических соединений (1861)
- •Структурные формулы
- •Объемные модели молекул
- •Объемные модели молекул
- •Функциональная группа
- •Формулы для описания органических веществ
- •Изомерия
- •Изомерия
- •Изомерия
- •Изомерия
- •Изомерия
- •Изомерия
- •Изомерия
- •Изомерия
- •Пространственная изомерия
- •Изомерия
- •Геометрическая изомерия
- •Изомерия
- •Изомерия
- •Изомерия
- •Изомерия
- •Оптическая изомерия
- •Оптическая изомерия
- •Оптическая изомерия
- •Гомология
- •Классификация органических соединений
- •Классификация органических соединений
- •По расположению атомов углерода в молекуле органические соединения делятся на:
- •Классификация органических соединений
- •Классификация органических соединений
- •Классификация органических соединений
- •Классификация органических соединений
- •Классификация органических соединений
- •Классификация органических соединений
- •Классификация органических соединений
- •Классификация органических соединений
- •Основы номенклатуры
- •Основы номенклатуры
- •Основы номенклатуры
- •Основы номенклатуры органических соединений
- •Основы номенклатуры органических
- •ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- •Электронная структура атома углерода в органических соединениях
- •Электронная структура атома углерода в органических соединениях
- •Гибридизация атомных орбиталей
- •Гибридизация
- •Гибридизация
- •Типы связей
- •Ковалентная связь
- •Ковалентная связь
- •Ковалентная связь
- •Ковалентная связь может образовываться двумя способами: 1. каждая частица, участвующая в образовании связи,
- •Типы химической связи
- •Различные виды перекрывания орбиталей
- •Различные виды перекрывания орбиталей
- •Различные виды перекрывания орбиталей
- •Различные виды перекрывания орбиталей
- •Различные виды перекрывания орбиталей
- •Различные виды перекрывания орбиталей
- •Различные виды перекрывания орбиталей
- •Свойства ковалентных связей
- •Энергия связи – средняя энергия, которая необходима для гомолитического разрыва связи (энергия диссоциации).
- •Длина связи и энергия
- •Направленность ковалентной связи
- •Полярность
- •Полярность
- •Поляризуемость
- •Реакционная способность органических соединений
- •Реакционная способность органических соединений
- •Реакционная способность органических соединений
- •Реакционная способность органических соединений
- •Реакционная способность органических соединений
- •Реакционная способность органических соединений
- •Реакционная способность органических соединений
- •Реакционная способность органических соединений
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Классификация органических реакций
- •Реагирующие органические частицы
- •Реагирующие органические частицы
- •Реагирующие органические частицы
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле
- •Взаимное влияние атомов в молекуле

Основы номенклатуры
органических соединений
Тривиальная номенклатура
O O
HN NH
O
Барбитуровая кислота |
31.10.1835 – 20.08.1917 |
Иоганн Фридрих Вильгельм Адольф фон Байер
51

Основы номенклатуры
органических соединений
Рациональная номенклатура
H3C C C CH3 |
H3C CH CH CH3 |
||
диметилацетилен |
симм-диметилэтилен |
||
OH |
CH3 |
O |
|
CH3 CH2 C CH2 CH2 CH3 |
H3C C C |
||
OH |
|||
CH |
CH3 |
||
|
|||
H3C CH3 |
|
||
|
|
||
этилпропилизопропилкарбинол |
триметилуксусная кислота |
||
52

Основы номенклатуры органических соединений
Систематическая номенклатура ИЮПАК
ИЮПАК [от английского названия Международного союза чистой и прикладной химии — International Union of Pure and Applied Chemistry (IUPAC)]
Систематические названия составлены из слов, специально созданных или выбранных для
описания структурных особенностей соединения.
соединения. 

53

Основы номенклатуры органических
соединений
Систематическая номенклатура ИЮПАК
Характеристическая |
Префикс |
Суффикс |
группа |
|
|
—(C)OOH
—COOH —SO3H —(C)H=O
—CH=O
 C
C O
O
—OH
—SH —NH2 —NO2 —OR
—F, —Cl, —Br, —I (Hal)
— |
-овая кислота |
|
карбокси- |
-карбоновая кислота |
|
сульфо- |
-сульфокислота |
|
оксо- |
-аль |
|
формил- |
-карбальдегид |
|
оксо- |
-он |
|
гидрокси-2 |
-ол |
|
меркапто- |
-тиол |
|
амино- |
-амин |
|
ннтро- |
— |
|
алкокси- |
— |
|
фтор-, хлор-, бром-, иод- |
— |
54 |
(галоген-) |
|
|

ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
55

Электронная структура атома углерода в органических соединениях
56

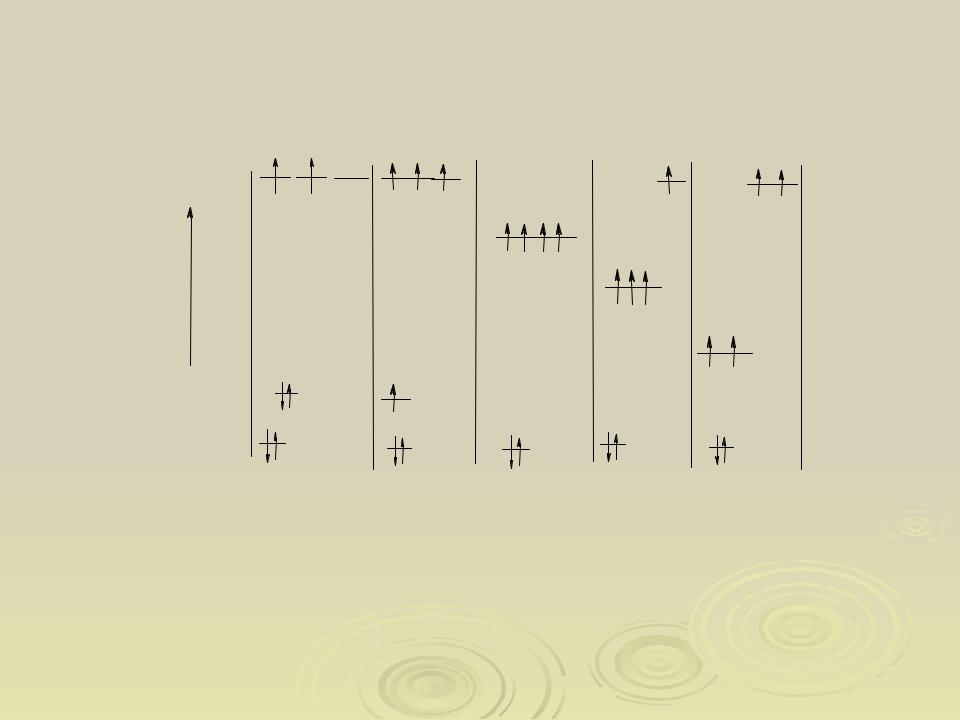
Электронная структура атома углерода в органических соединениях
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 p x 1 |
2 p y 1 |
2 p |
z 0 |
|
|
|
|
|
|
2 p x 1 |
2 p y 1 |
2 p z 1 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
2 s 2 |
|
|
|
|
2 s 1 |
||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
1 s 2 |
|
|
|
|
|
|
|
1 s 2 |
|
|
|
|
|
|
|
|||||||||
основное состояние |
|
возбужденное состояние |
||||||||||||||||||||||
57
Гибридизация атомных орбиталей
2p |
|
|
|
|
2sp3 |
|
|
|
|
Увeличeниe 2sp2 |
|
|
|
|
энeргии |
|
|
|
|
2sp |
|
|
|
|
2s |
|
|
|
|
1s |
|
|
|
|
C |
C* |
sp3 |
sp2 |
sp |
Из четырех неэквивалентных атомных орбиталей (одной S и трех Р) «образуется» ЧЕТЫРЕ эквивалентные «гибридизованные» - SP3 –
гибридные орбитали.
58

Гибридизация
Атомная орбиталь — это часть пространства, в которой вероятность нахождения электрона максимальна.
59

Гибридизация
Гибридные орбитали и характер углеродных атомов
Состояние
углеродного
атома
Возбужденное,
исходное
состояние
Алканы
Алкены
Алкы
|
|
|
|
Валентно |
|
|
|
|
е |
|
Орбитали |
|
состояни |
|
|
|
|
|
е атома |
|
|
|
|
углерода |
2s |
2px |
2py |
2pz |
– |
2sp3 |
2sp3 |
2sp3 |
2sp3 |
I |
2sp2 |
2sp2 |
2sp2 |
2p |
II |
2sp |
2sp |
2p |
2p |
III |
Тип гибридизации и строение молекулы
–
(sp3)  Тетраэдрическое
Тетраэдрическое
(sp2) Тригональное (плоскостное) 
(sp) Дигональное (линейное) 
60
