- •Кіровоградський машинобудівний коледж
- •Лабораторна робота № 1
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 2
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 3
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 4
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 5
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 6
- •Порядок виконання роботи
- •Властивості гідроксильної групи
- •1.Взаємодія з розчином лугу.
- •2. Взаємодія з розчином ферум (ііі) хлориду – якісна реакція на фенол.
- •Властивості бензольного кільця.
- •3. Взаємодія з розчином бромної води – якісна реакція на фенол.
- •Контрольні запитання
- •Лабораторна робота № 7
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота № 8
- •Порядок виконання роботи
- •Контрольні запитання
- •Лабораторна робота №9
- •Порядок виконання роботи
- •Взаємодія з бромною водою – заміщення в бензольному ядрі
- •Окиснення аніліну хромовою сумішшю.
- •Окиснення аніліну розчином хлорного вапна
- •Властивості білків.
- •Ксантопротеїнова реакція
- •Біуретова реакція
- •Контрольні запитання
- •Лабораторна робота №10
- •Порядок виконання роботи
Контрольні запитання
Які речовини можна використати для лабораторного способу добування карбон (IV) оксиду?
Які властивості карбон (IV) оксиду доводить його взаємодія з водою? Які речовина утворюється?
Які сполуки утворюються при взаємодії карбон (IV)оксиду з лугами?
Який іон є якісним іоном на карбонат-іон?
Які сполуки утворюються при розкладанні солей карбонатної кислоти? Які умови реакції?
Лабораторна робота № 4
Тема: Виявлення Карбону, Гідрогену та Хлору в органічних речовинах. Добування та хімічні властивості метану.
Мета: на практиці навчитися виявляти основні складові елементи органічних сполук за допомогою розробленої методики; добути метан в лабораторії та вивчити його властивості.
Обладнання та матеріали: парафін – 0,5г, порошок купруму (ІІ) оксиду – 1-2г, вапняна вода – 2-3мл, безводний купруму (ІІ) сульфат – 2г, калій ацетат або натрій ацетат (безводний, плавлений), натронне вапно свіжопрожарене (1:2); калій перманганат (1% - ний розчин), бромна вода (насичений розчин), пробірки з пробками і газовідвідними трубками, пробірка для вапняної води, штатив, хлоровмісна органічна сполука (хлороформ, дихлоретан – 1мл), мідний дріт товщиною 1-2мм, штатив, фарфорова чашка, кристалізатор, спиртівка або газовий пальник.
Порядок виконання роботи
Дослід 1. Визначення Карбону та Гідрогену.
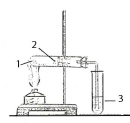
Збирання приладів. Дослід можна проводити у приладі для збирання газів (мал1). Суміш досліджуваної речовини з купрум (ІІ) оксидом помістіть у суху пробірку і закріпіть її у штативі у горизонтальному положенні. Обережно внесіть безводний купрум (ІІ) сульфат і закрийте пробірку пробкою з газовідвідною трубкою, кінець якої опустіть в пробірку з вапняною водою. Обережно нагрівайте пробірку з досліджуваною речовиною. Спостерігайте зміни, що відбуваються з купруму (ІІ) оксидом, купруму (ІІ) сульфатом, вапняною водою, після цього дослід припиніть.
Спостереження __________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
Напишіть рівняння реакцій, що відбуваються_________________________________________
________________________________________________________________________________
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Висновки. Яку роль відіграє у даному досліді купрум (ІІ) оксид? З якою метою використовується вапняна вода та купрум (ІІ) сульфат?________________________________
________________________________________________________________________________
________________________________________________________________________________________________________________________________________________________________
|
|
Мал.1 Виявлення Карбону та Гідрогену в органічній сполуці. 1 – Суміш речовини, що досліджується з оксидом купруму (ІІ); 2 – безводний сульфат купруму (ІІ); 3 – вапняна вода |
Дослід 2. Виявлення хлору.
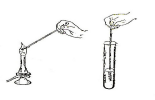
Кінець мідного дроту зігніть петелькою або у вигляді спіралі діаметром 1-2мм. Прожарюйте дротину у полум’ї до тих пір, поки полум’я не перестане забарвлюватись, охолодіть її. Внесіть дротину в речовину, що досліджується, і знову в полум’я (мал2).
Спостереження___________________________________________________________________
Висновки_______________________________________________________________________________________________________________________________________________________
|
|
Мал 2. Виявлення галогену в органічній сполуці (проба Бейльштейна)
|
Дослід 3. Добування метану і вивчення його властивостей.
У суху пробірку помістіть суміш натрій ацетату і натронного вапна (суміш натрій гідроксиду з кальцій гідроксидом). Пробірку заповніть на 1/5 її вмісту і закрийте пробкою з газовідвідною трубкою, закріпіть на штативі з невеликим нахилом у бік пробки. Суміш у пробірці обережно нагрійте.
Спостереження___________________________________________________________________
________________________________________________________________________________
Рівняння реакції _________________________________________________________________
Пропустіть по черзі метан, що виділяється з газовідвідної трубки, крізь розчин бромної води та калій перманганату.
Що спостерігаєте?___________________________________________________________
Рівняння реакцій____________________________________________________________
Після цього звужений кінець газовідвідної трубки, з якої виділяється метан, розмістіть вертикально. Метан, який виділяється з трубки, підпаліть. У полум'я запаленого метану внесіть фарфоровий шпатель, переконавшись, що на його поверхні не утворюється кіптяви.
Який колір має полум’я?___________________________________________________________
Рівняння реакції__________________________________________________________________
Зробіть висновок про хімічні властивості метану______________________________________
________________________________________________________________________________
________________________________________________________________________________________________________________________________________________________________
Підпис студента______________________
Підпис викладача______________________