
- •1. Терминология,
- •2. Энергетика процессов
- •3. Критерии направленности процессов и равновесия
- •4. Химическое равновесие
- •1. Терминология, основные понятия и определения
- •1.1. Термодинамическая система
- •1.2. Термодинамические параметры
- •1.3. Термодинамический процесс и термодинамическое равновесие
- •1.4. Функции пути осуществления процесса и функции состояния
- •1.5. Химический процесс и химическая переменная
- •1.6. Модели идеальных систем в химической термодинамике. Реальные системы
- •2. Энергетика процессов
- •2.1. Первое начало термодинамики (постулат о существовании внутренней энергии)
- •2.2. Термодинамическая работа
- •2.3. Внутренняя энергия и теплота
- •2.4. Энтальпия
- •2.5. Взаимосвязь работы и теплоты с изменениями внутренней энергии и энтальпии в изопроцессах с участием идеального газа
- •2.6. Теплоёмкость
- •2.7. Фазовые переходы I рода
- •2.8. Зависимость теплоёмкости от температуры
- •Простых веществ
- •2.9. Зависимость внутренней энергии и энтальпии от температуры
- •2.10. Зависимость внутренней энергии, энтальпии и теплоемкости от давления
- •2.11. Изменение внутренней энергии и энтальпии в химических реакциях
- •2.12. Экспериментальные методы определения тепловых эффектов химических реакций
- •2.13. Стандартные тепловые эффекты
- •2.14. Зависимость теплового эффекта от температуры. Уравнение Кирхгофа
- •Температуры:
- •2.15. Интегрирование уравнения Кирхгофа
- •2.16. Зависимость энтальпии реакции от давления
- •3. Критерии направленности процессов и равновесия в системах постоянного и переменного составов
- •3.1. Второе начало термодинамики (постулат о существовании энтропии)
- •3 .1.1.С в о и ств а энтропии. Энтропия как критерий направленности самопроизвольных процессов и равновесия в изолированных системах
- •3.1.2. Связь энтропии с параметрами
- •3.1.4. Изменение энтропии при обратимых фазовых переходах I рода
- •3.1.5. Статистическое толкование энтропии. Уравнение б ольцма иа -Пл анка
- •3.1.7. Расчет абсолютных значений энтропии
- •Абсолютной энтропии
- •3.1.8. Изменение энтропии в химических
- •3.2. Критерии направленности процессов и равновесия в неизолированных системах
- •3.2.1. Объединенное уравнение первого и второго начал термодинамики
- •3.2.4. Зависимости энергии Гиббса и энергии Гельмгольца от основных параметров состояния
- •Веществ
- •Веществ
- •Веществ
- •Веществ
- •При наличии фазовых превращений
- •3.2.7. Уравнения г и б б с а-г е л ь м г о л ь ц а
- •3.2.8. Вывод уравнений для зависимостей термодинамических функций от давления и объема
- •3.2.9. О "сложности" преобразований при выводе уравнений химической термодинамики
- •Функций по параметрам состояния
- •3.3. Критерии направленности процессов и равновесия в системах переменного состава
- •3.3.1. Химический потенциал
- •3.3.2. Свойства химического потенциала
- •3.3.3. Химический потенциал моля идеального газа
- •3.3.4. Химический потенциал компонента смеси идеальных газов
- •4. Химическое равновесие
- •4.1. Химическое равновесие в смеси идеальных
- •4.2. Расчет стандартного химического сродства
- •4.3. Стандартное химическое сродство и термодинамическая константа равновесия как характеристики равновесного состояния
- •4.4. Химическое сродство как критерий направленности процесса
- •4.5. Зависимость константы равновесия от температуры
- •4.5.1. Дифференциальная форма уравнений изобары и изохоры химической реакции
- •4.6. Расчет термодинамической константы равновесия
- •4.6.1. Общая характеристика фонда справочных данных
- •4.6.2. Способы расчета термодинамической константы равновесия
- •4 . 7 . 1.Реа к ц и и в смесях газов.
- •Связь термодинамической константы равновесия с
- •Эмпирическими (концентрационными) константами
- •Равновесия:Кр', кх,кп,кс
- •4.7.2.Реакции в гомогенной конденсированной фазе (реакции в растворах)
- •4.7.3. Реакции в гетерогенных системах
- •4.8. Расчет состава равновесной смеси по величине термодинамической константы равновесия
- •4.8.1.Химическое превращение представлено единственным уравнением
- •4.8.2.Химическое превращение представлено двумя уравнениями
- •4.8.3. Множественные реакции
- •4.9. Влияние различных факторов на состав
3.2. Критерии направленности процессов и равновесия в неизолированных системах
при p,t = const и v,t = const
3.2.1. Объединенное уравнение первого и второго начал термодинамики
Это уравнение является одним из самых важных в химической термодинамике. На первый взгляд очень простое пребразование привело к качественно новому этапу в развитии химической термодинамики. Благодаря ему стало возможным перейти к установлению фундаментальных соотношений между термодинамическими функциями и параметрами состояния.
Запишем выражение первого начала термодинамики для простых систем, в которых происходят обратимые изменения:
![]()
Примем во внимание, что
![]()
и после объединения уравнений приходим к выражению:
![]()
Убедимся теперь в том, что записанное уравнение позволяет при определенных ограничениях установить взаимосвязь термодинамических функций с параметрами состояния.
т.е. производная внутренней энергии по энтропии есть температура. При постоянстве энтропии
84
При постоянстве объема
![]()
![]()
[p# 86]
Если теперь учесть выведенное ранее выражение для dU, то:
производная внутренней энергии по объему равна давлению с обратным знаком. Для установления связи параметров состояния с энтальпией запишем уравнение для полного дифференциала данной термодинамической функции:
![]()
![]()
Отсюда следует, что в изобарических условиях
'
Л
'![]()
т.е. производная энтальпии по энтропии равна температуре, а при фиксированной энтропии
![]()
- производная энтальпии по давлению равна объему системы.
В общем случае объединенное уравнение первого и второго начал термодинамики записывается для обратимых процессов в виде:
![]()
где последнее слагаемое представляет работу против всех внешних сил кроме сил внешнего давления, т.е. так называемую максимально полезную работу. Записанное уравнение принято называть фундаментальным уравнением Гиббса. Оно составляет основу математического аппарата термодинамики при рассмотрении самых различные процессов и явлений. Ниже будет показано, как с его помощью были установлены критерии направленности процессов и равновесия в закрытых системах постоянного и переменного составов.
3, Критерии (G и Н) 85
[p# 87]
3.2.2. Энергия Гиббса и энергия Гельмгольца
Второе начало термодинамики устанавливает критерий направленности процессов и равновесия в изолированных системах. Оно утверждает, что любые самопроизвольные процессы в изолированных системах должны сопровождаться возрастанием энтропии. Однако использование этого критерия оказывается неудобным, поскольку для нахождения знака AS требуется вначале найти изменение энтропии рабочей части системы, а затем учесть изменение энтропии, связанное с состоянием теплового резервуара, окружающего рабочую часть системы.
Другой подход к решению данной проблемы был разработан выдающимся американским ученым Джозайей Уиллардом Гиббсом (1839-1903). Он предложил отказаться от рассмотрения изолированных систем и перейти к анализу поведения закрытых систем, которые, как и изолированные, не могут обмениваться с окружением массой, но в отличие от последних свободно обмениваются энергией. Иными словами Гиббс предложил вообще не учитывать изменения, происходящие в состоянии теплового резервуара, и ограничиться рассмотрением процессов, имеющих место в' рабочей части системы. На основании этой идеи, были сформулированы новые критерии направленности процессов и равновесия, которые оказались значительно удобнее для практического применения, чем энтропия.
Чтобы установить эти критерии, запишем объединенное уравнение первого и второго начал термодинамики для системы, которая может совершать разичные виды работы, одним из которых является работа против сил внешнего давления:
![]()
![]()
Знак ">" в этом выражении относится к необратимым процессам, знак "=" - к обратимым.
Рассмотрим, как будет выглядеть это уравнение в условиях, когда V,T^const и p,T=const.
86
Для простых систем, в случае которых 5W = 0, можно записать:
![]()
[p# 88]
Если V, T=const, то

что равноценно выражению:
Так как dU и dS являются полными дифференциалами, то выражение, стоящее в скобках, будет полным дифференциалом функции, включающей внутреннюю энергию и энтропию, а именно:
д =т т — тч
/•V = U 1 О ,
Эта функция была названа энергией Гельмгольца. Для нее можно записать:
dA<0, и, следовательно,
любой самопроизвольный процесс, происходящий в закрытой системе при постоянстве объема и температуры, сопровождается убылью энергии Гельмгольца и завершается достижением равновесия, при котором dA = О и ДА = 0.
Иллюстрацией этого является рис.13.
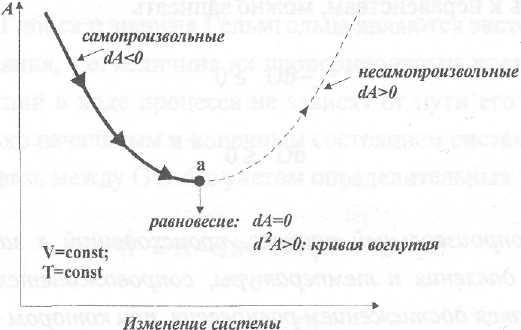
Рис. 13. Изменения энергии Гельмгольца в закрытых системах
3. Критерии (G иН)
87
[p# 89]
Если при постоянных V и Т система совершает работу не только против сил внешнего давления, но и против других сил, то в обратимом процессе убыль энергии Гельмгольца равна максимально полезной работе;
![]()
Энергию Гельмгольца иногда называют свободной внутренней энергией или свободной энергией при постоянных V и Т, подчеркивая тем самым наличие так называемой связанной энергии TS , которая не может быть превращена в работу *).
В практическом отношении более важный случай соответствует условию p,T=const. В случае простых систем:
TdS-dU-pdV>0 В терминах энтальпии будем иметь:
Л 1/ '^
![]()
В левой части мы вновь имеем комбинацию, которую можно рассматривать как полный дифференциал новой функции:
![]() s
s
получившей название энергии Гиббса (синонимы - свободная энергия Гиббса, свободная энтальпия).
Возвращаясь к неравенствам, можно записать
.
![]()
или
![]()
и, следовательно,
любой самопроизвольный процесс, происходящий в закрытой системе при постоянстве давления и температуры, сопровождается убылью энергии Гиббса и завершается достижением равновесия, при котором dG = 0 и AG - 0.
*) Термин свободная энергия впервые предложил Герман Л. Гельмольц (1821-1894), хотя за 13 лет до него эту функцию ввел Франсуа Массье (1832-1896), а за 1 лет до Гельмгольца использовал в своих работах Гиббс.
[p# 90]
88
[p# 91]
Схематическое представление этого положения дано на рис.14 .

Рис. 14 Изменения энергии Гиббса в закрытых системах
Если система совершает работу не только против сил внешнего давления, но и против других сил, то
![]() 5
5
т.е. в условиях обратимости полезная работа равна убыли энергии Гиббса. 3.2.3. Свойства функций G и А
Перечень основных свойств рассматриваемых функций можно сформулировать в довольно сжатой форме.
Энергия Гиббса и энергия Гельмгольца являются экстенсивными функциями состояния, т.е. величина их пропорциональна количеству вещества, а изменение функций в ходе процесса не зависят от пути его осуществления и определяется только начальным и конечным состоянием системы.
Взаимосвязь между G и А с учетом определительных уравнений:
G -H-TS-U + pV-TS
и
A =U-TS
выражается для одного моля уравнением:
[p# 92]
3. Критерии (G и Н)
89
[p# 93]
A =U-TS
выражается для одного моля уравнением:
G-A = pV,
которое для моля идеального газа может быть представлено в виде:
G-A =RT
В случае конденсированных фаз вследствие малости их мольного объема в сравнении с газами произведение pV«RT поэтому для жидкостей и твердых тел
G*A
Поскольку уравнения, определяющие рассматриваемые функции включают внутреннюю энергию, то по абсолютному значению энергия Гиббса и энергия Гельмгольца определены быть не могут.
Энергию Гиббса и энергию Гельмгольца (а также внутреннюю энергию и энтальпию) называют характеристическими функциями. Эти функции обладают двумя важными свойствами. Первое свойство состоит в том, что характеристические функции обращаются в нуль при постоянстве относящихся к ним так называемых "естественных переменных". Для энергии Гиббса естественными переменными являются, как было показано в предыдущем разделе, р и Т , тогда как для энергии Гельмгольца - V и Т. Второе свойство характеристических функций заключается в том, через их производные по естественным переменным можно в явной форме установить связь термодинамических свойств систем с основными термодинамическими параметрами (что будет показано в следующем разделе).
Энергия Гиббса и энергия Гельмгольца являются термодинамическими потенциалами, т.е. функциями, убыль которых при постоянстве естественных переменных равна в условиях обратимости максимально полезной работе.
3. Критерии (Си Н) 90
[p# 94]
