
- •1. Терминология,
- •2. Энергетика процессов
- •3. Критерии направленности процессов и равновесия
- •4. Химическое равновесие
- •1. Терминология, основные понятия и определения
- •1.1. Термодинамическая система
- •1.2. Термодинамические параметры
- •1.3. Термодинамический процесс и термодинамическое равновесие
- •1.4. Функции пути осуществления процесса и функции состояния
- •1.5. Химический процесс и химическая переменная
- •1.6. Модели идеальных систем в химической термодинамике. Реальные системы
- •2. Энергетика процессов
- •2.1. Первое начало термодинамики (постулат о существовании внутренней энергии)
- •2.2. Термодинамическая работа
- •2.3. Внутренняя энергия и теплота
- •2.4. Энтальпия
- •2.5. Взаимосвязь работы и теплоты с изменениями внутренней энергии и энтальпии в изопроцессах с участием идеального газа
- •2.6. Теплоёмкость
- •2.7. Фазовые переходы I рода
- •2.8. Зависимость теплоёмкости от температуры
- •Простых веществ
- •2.9. Зависимость внутренней энергии и энтальпии от температуры
- •2.10. Зависимость внутренней энергии, энтальпии и теплоемкости от давления
- •2.11. Изменение внутренней энергии и энтальпии в химических реакциях
- •2.12. Экспериментальные методы определения тепловых эффектов химических реакций
- •2.13. Стандартные тепловые эффекты
- •2.14. Зависимость теплового эффекта от температуры. Уравнение Кирхгофа
- •Температуры:
- •2.15. Интегрирование уравнения Кирхгофа
- •2.16. Зависимость энтальпии реакции от давления
- •3. Критерии направленности процессов и равновесия в системах постоянного и переменного составов
- •3.1. Второе начало термодинамики (постулат о существовании энтропии)
- •3 .1.1.С в о и ств а энтропии. Энтропия как критерий направленности самопроизвольных процессов и равновесия в изолированных системах
- •3.1.2. Связь энтропии с параметрами
- •3.1.4. Изменение энтропии при обратимых фазовых переходах I рода
- •3.1.5. Статистическое толкование энтропии. Уравнение б ольцма иа -Пл анка
- •3.1.7. Расчет абсолютных значений энтропии
- •Абсолютной энтропии
- •3.1.8. Изменение энтропии в химических
- •3.2. Критерии направленности процессов и равновесия в неизолированных системах
- •3.2.1. Объединенное уравнение первого и второго начал термодинамики
- •3.2.4. Зависимости энергии Гиббса и энергии Гельмгольца от основных параметров состояния
- •Веществ
- •Веществ
- •Веществ
- •Веществ
- •При наличии фазовых превращений
- •3.2.7. Уравнения г и б б с а-г е л ь м г о л ь ц а
- •3.2.8. Вывод уравнений для зависимостей термодинамических функций от давления и объема
- •3.2.9. О "сложности" преобразований при выводе уравнений химической термодинамики
- •Функций по параметрам состояния
- •3.3. Критерии направленности процессов и равновесия в системах переменного состава
- •3.3.1. Химический потенциал
- •3.3.2. Свойства химического потенциала
- •3.3.3. Химический потенциал моля идеального газа
- •3.3.4. Химический потенциал компонента смеси идеальных газов
- •4. Химическое равновесие
- •4.1. Химическое равновесие в смеси идеальных
- •4.2. Расчет стандартного химического сродства
- •4.3. Стандартное химическое сродство и термодинамическая константа равновесия как характеристики равновесного состояния
- •4.4. Химическое сродство как критерий направленности процесса
- •4.5. Зависимость константы равновесия от температуры
- •4.5.1. Дифференциальная форма уравнений изобары и изохоры химической реакции
- •4.6. Расчет термодинамической константы равновесия
- •4.6.1. Общая характеристика фонда справочных данных
- •4.6.2. Способы расчета термодинамической константы равновесия
- •4 . 7 . 1.Реа к ц и и в смесях газов.
- •Связь термодинамической константы равновесия с
- •Эмпирическими (концентрационными) константами
- •Равновесия:Кр', кх,кп,кс
- •4.7.2.Реакции в гомогенной конденсированной фазе (реакции в растворах)
- •4.7.3. Реакции в гетерогенных системах
- •4.8. Расчет состава равновесной смеси по величине термодинамической константы равновесия
- •4.8.1.Химическое превращение представлено единственным уравнением
- •4.8.2.Химическое превращение представлено двумя уравнениями
- •4.8.3. Множественные реакции
- •4.9. Влияние различных факторов на состав
3.3.2. Свойства химического потенциала

Это связано с тем, что в случае других характеристических функций:
Большинство процессов в химии и химической технологии происходят в условиях, когда p,T=const, поэтому из четырех возможных форм выражения для химического потенциала предпочтение отдается уравнению

невозможно обеспечить постоянство естественных переменных при изменении состава системы. Например, трудно представить, что добавление моля компонента оставят неизменными объем или энтропию системы.
Производную энергии Гиббса по числу молей одного из компонентов системы называют также парциальной молярной энергией Гиббса и обозначают G;. Эта характеристика позволяет определить вклад данного компонента в общую энергию Гиббса системы, основываясь на уравнении:
![]()
Очевидно, что химический потенциал чистого вещества равен мольной энергии Гиббса (Gj^r. Поэтому все уравнения, выведенные ранее для энергии
Гиббса, справедливы и для химического потенциала при условии замены всех мольных величин на парциальные мольные. Например:
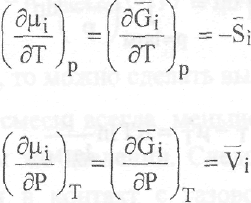
и т.д.
3, Критерии (ц)
[p# 121]
Следует подчеркнуть, что химический потенциал является величиной интенсивной, не зависящей от числа молей (отношение двух экстенсивных величин - всегда величина интенсивная: например, объем и масса - экстенсивные величины, их отношение - плотность - интенсивная).
Особое значение химического потенциала в химии связано с тем, что разность Д^ является количественной характеристикой способности данного компонента самопроизвольно перемещаться из области с высоким значением ц; в
область с низким значением ^. Градиент химического потенциала ~^- при этом
ну;
является движущей силой процесса переноса массы вдоль координаты её перемещения (у).
3.3.3. Химический потенциал моля идеального газа
Химический потенциал моля идеального газа совпадает с мольной энергией Гиббса, Поскольку абсолютная величина энергии Гиббса неизвестна, то, естественно, неизвестно и абсолютное значение химического потенциала. В связи с этим приходится договариваться о стандарте состояния, относительно которого будет производиться отсчёт. Вспомним, что для газов в качестве стандартного принимается их состояние при любой температуре и давлении 1 атм.
Так как для моля чистого вещества при Т - const
1![]() _
>
_
>
то:
![]()
-Интегрируя это уравнение, получаем:

![]()
или
![]()
[p# 122]
П6
[p# 123]
Ит называют стандартным химическим потенциалом газа. Величина его зависит только от температуры и природы газа.
Стоит запомнить, что под логарифмом располагается "безразмерное давление", т.е. давление, выраженное в долях от стандартного. Удобство использования "атм" заключается в том, что применение этой единицы как бы автоматически осуществляет нормировку.
3.3.4. Химический потенциал компонента смеси идеальных газов
Выражение для химического потенциала в данном случае имеет по внешним признакам вид, аналогичный предыдущему уравнению:
![]()
с той разницей, что />/ представляет собой парциальное давление компонента
газовой смеси. Так как
![]() ?
?
где х/ - мольная доля газа и р - общее давление газовой смеси, то
![]()
Два первых члена в правой части этого уравнения равны химическому потенциалу чистого газа при давлении р и, следовательно, уравнение может быть преобразовано к виду:
![]()
, Так как щ <1 и 1пх, < 0, то можно сделать вывод, что химический потенциал любого компонента газовой смеси всегда меньше, чем химический потенциал индивидуального газа при том же давлении. Следовательно, если при некотором цавлении газ будет приведен в контакт с газовой смесью или другим газом, имеющим то же давление, то он будет самопроизвольно распределяться в другом
3. Критерии (ц) П 7
[p# 124]
газе или в газовой смеси. Это, кстати, объясняет тот факт, что любые индивидуальные вещества при взаимном контакте должны распределяться друг в друге с образованием термодинамически более устойчивых систем. Заканчивая данный раздел, отметим, что выражение
![]()
можно рассматривать как определительное для понятия идеальной смеси или идеального раствора в любом агрегатном состоянии (твердом, жидком, газообразном). В этом случае Ц] (Т, р) является химическим потенциалом чистого вещества в том же самом агрегатном состоянии, что и смесь. Например, в жидком растворе \i\ (Т, р) есть химический потенциал или мольная энергия Гиббса чистого жидкого компонента i при температуре Т и давлении р.
118
[p# 125]
