
- •1. Терминология,
- •2. Энергетика процессов
- •3. Критерии направленности процессов и равновесия
- •4. Химическое равновесие
- •1. Терминология, основные понятия и определения
- •1.1. Термодинамическая система
- •1.2. Термодинамические параметры
- •1.3. Термодинамический процесс и термодинамическое равновесие
- •1.4. Функции пути осуществления процесса и функции состояния
- •1.5. Химический процесс и химическая переменная
- •1.6. Модели идеальных систем в химической термодинамике. Реальные системы
- •2. Энергетика процессов
- •2.1. Первое начало термодинамики (постулат о существовании внутренней энергии)
- •2.2. Термодинамическая работа
- •2.3. Внутренняя энергия и теплота
- •2.4. Энтальпия
- •2.5. Взаимосвязь работы и теплоты с изменениями внутренней энергии и энтальпии в изопроцессах с участием идеального газа
- •2.6. Теплоёмкость
- •2.7. Фазовые переходы I рода
- •2.8. Зависимость теплоёмкости от температуры
- •Простых веществ
- •2.9. Зависимость внутренней энергии и энтальпии от температуры
- •2.10. Зависимость внутренней энергии, энтальпии и теплоемкости от давления
- •2.11. Изменение внутренней энергии и энтальпии в химических реакциях
- •2.12. Экспериментальные методы определения тепловых эффектов химических реакций
- •2.13. Стандартные тепловые эффекты
- •2.14. Зависимость теплового эффекта от температуры. Уравнение Кирхгофа
- •Температуры:
- •2.15. Интегрирование уравнения Кирхгофа
- •2.16. Зависимость энтальпии реакции от давления
- •3. Критерии направленности процессов и равновесия в системах постоянного и переменного составов
- •3.1. Второе начало термодинамики (постулат о существовании энтропии)
- •3 .1.1.С в о и ств а энтропии. Энтропия как критерий направленности самопроизвольных процессов и равновесия в изолированных системах
- •3.1.2. Связь энтропии с параметрами
- •3.1.4. Изменение энтропии при обратимых фазовых переходах I рода
- •3.1.5. Статистическое толкование энтропии. Уравнение б ольцма иа -Пл анка
- •3.1.7. Расчет абсолютных значений энтропии
- •Абсолютной энтропии
- •3.1.8. Изменение энтропии в химических
- •3.2. Критерии направленности процессов и равновесия в неизолированных системах
- •3.2.1. Объединенное уравнение первого и второго начал термодинамики
- •3.2.4. Зависимости энергии Гиббса и энергии Гельмгольца от основных параметров состояния
- •Веществ
- •Веществ
- •Веществ
- •Веществ
- •При наличии фазовых превращений
- •3.2.7. Уравнения г и б б с а-г е л ь м г о л ь ц а
- •3.2.8. Вывод уравнений для зависимостей термодинамических функций от давления и объема
- •3.2.9. О "сложности" преобразований при выводе уравнений химической термодинамики
- •Функций по параметрам состояния
- •3.3. Критерии направленности процессов и равновесия в системах переменного состава
- •3.3.1. Химический потенциал
- •3.3.2. Свойства химического потенциала
- •3.3.3. Химический потенциал моля идеального газа
- •3.3.4. Химический потенциал компонента смеси идеальных газов
- •4. Химическое равновесие
- •4.1. Химическое равновесие в смеси идеальных
- •4.2. Расчет стандартного химического сродства
- •4.3. Стандартное химическое сродство и термодинамическая константа равновесия как характеристики равновесного состояния
- •4.4. Химическое сродство как критерий направленности процесса
- •4.5. Зависимость константы равновесия от температуры
- •4.5.1. Дифференциальная форма уравнений изобары и изохоры химической реакции
- •4.6. Расчет термодинамической константы равновесия
- •4.6.1. Общая характеристика фонда справочных данных
- •4.6.2. Способы расчета термодинамической константы равновесия
- •4 . 7 . 1.Реа к ц и и в смесях газов.
- •Связь термодинамической константы равновесия с
- •Эмпирическими (концентрационными) константами
- •Равновесия:Кр', кх,кп,кс
- •4.7.2.Реакции в гомогенной конденсированной фазе (реакции в растворах)
- •4.7.3. Реакции в гетерогенных системах
- •4.8. Расчет состава равновесной смеси по величине термодинамической константы равновесия
- •4.8.1.Химическое превращение представлено единственным уравнением
- •4.8.2.Химическое превращение представлено двумя уравнениями
- •4.8.3. Множественные реакции
- •4.9. Влияние различных факторов на состав
4.8.2.Химическое превращение представлено двумя уравнениями
Пусть, например, в газовой фазе одновременно протекают реакции:
A+B-C+D
-
С + 2В-Е
Допустим, что в начальный момент времени продукты в исходной смеси отсутствуют, а количества А и В составляют, соответственно, 1 и 2 моля.
Вполне очевидно, что каждая из записанных реакций должна быть охарактеризована своей степенью протекания. Обозначим их, соответственно, £i и ^2 и тогда равновесные количества всех присутствующих в смеси веществ
составят:
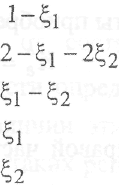
Общее число молей будет равно: 3-
Изменение числа молей в первой реакции составляет A v, - 0 и во второй Av2 = -2. С учетом этого выражения для термодинамических констант равновесия при идеальности газовой фазы следует записать в виде:

![]()
![]()
В результате получается система двух нелинейных уравнений относительно двух неизвестных величин: ^ и ^2- Уравнения могут быть
150
[p# 154]
решены графически. С этой целью строят две зависимости ^2 = f(4i)? °Дна из которых соответствует уравнению для Kls вторая - уравнению для К3.
Пересечение линий дает решение системы уравнений. При использовании компьютера решение может быть найдено и без процедуры графических построений.
;'
4.8.3. Множественные реакции
Из примера, разобранного в предыдущем разделе, становится очевидным, что в случае множественных реакций будет необходимо решать систему из нескольких нелинейных уравнений, число которых будет совпадать с числом одновременно протекающих реакций. С этой целью могут быть использованы различные вычислительные методы, два из которых, а именно, метод минимизации энергии Гиббса и метод релаксации, считаются предпочтительными.
Метод минимизации энергии Гиббса заключается в поиске минимума энергии Гиббса дл рассматриваемой системы реакций. Этот минимум при постоянстве р и Т достигается, когда состав системы, отвечает равновесному. Если, например, рассматривается равновесие, устанавливающееся в идеальной газовой смеси, то выражение для энергии Гиббса системы будет иметь вид:
![]()
![]()
![]()
Сложность решения задачи заключается в том, что подстановка в записанное уравнение каждого нового значения nj требует решения системы
нелинейных уравнений для всех остальных компонентов. Обычно поиск минимума данной функции осуществляется с помощью метода множителей Лагранжа, который реализован в упоминавшихся компьютерных базах термодинамических данных. Анализ процедуры решения данной задачи выходит за рамки данного курса, поэтому ниже мы остановимся на рассмотрении существа более простого и достаточно наглядного метода,
4. Химическое равновесие 151
[p# 155]
называемого методом релаксации или методом последовательно соединенных реакторов.
В этом случае рассматриваемую совокупность реакций представляют в виде системы последовательно соединенных реакторов, число которых равно числу независимых стехиометрических уравнений. Каждый реактор действует как периодический и обеспечивает достижение равновесия в реакции, номер которой соответствует номеру реактора.
Процесс мысленно начинают с загрузки исходной смеси в первый реактор, где равновесие достигается в первой реакции. Полученные продукты перегружают во второй реактор, в котором равновесия достигает вторая реакция. Затем продукты перегружается в третий реактор и так далее. В каждый реактор поступает равновесная смесь продуктов из предыдущего реактора, и в каждом реакторе протекает только одна реакция.
Первый проход заканчивается после того, как смесь прошла реактор, номер которого соответствует номеру последней реакции. Сказанное поясняет рис.26.

Рецикл равновесного потока
Рис. 26. Схема метода релаксации для определения равновесного состава в случае множественных реакций
Если, например, в рассматриваемой системе происходит три реакции, то после третьего реактора полученную реакционную смесь вновь загружают в первый реактор и цикл повторяют до тех пор, пока степени протекания каждой реакции не станут исчезающе малыми.
Таким образом, в методе последовательно соединенных реакторов приходится решать уравнения с одной неизвестной величиной £, что существенно проще, чем одновременное решение системы нелинейных уравнений. В каждом новом «проходе» системы реакторов степень
152
[p# 156]
превращения постепенно снижается, приближаясь к нулевому значению. Если число реакций сравнительно невелико (равно, например, шести), сходимость достигается менее, чем через десять «проходов» через реакторную систему.
В качестве примера приведем данные *> о термической диссоциации изо-пропанола в газовой фазе при 400 К и общем давлении 1 атм. В упрощенном варианте процесс может быть представлен тремя уравнениями:



где цифры, стоящие под веществами, соответствуют обозначениям в уравнениях для констант равновесия указанных реакций, представленных через степени протекания.
Выражения для термодинамических констант относительно первого цикла вычислений записываются в виде;
![]()


*) Стенли М. Уэйлес. Фазовые равновесия в химической технологии . М.: Мир, [p# 157]
1989. Т. 2, С. 497.
4. Химическое равновесие
153
[p# 158]
где подстрочные индексы 10, 20, 30 и т.д. относятся к числу молей компонентов 1, 2, 3 и т.д. в начальный момент времени для каждого цикла вычислений. Это означает, что:
на входе во второй реактор (n10)2 = OMo)i -£i;
на входе в третий (n,0)3 = (n10)i-§i-^ (П20)з =(п2о)2+42
и так далее для всех компонентов в общем цикле вычислений. Найденные значения концентраций всех компонентов после третьего реактора считаются исходными во втором цикле вычислений.
Результаты расчета для случая, когда в реактор вводится один моль изо-пропанола приведены в табл.6.
Таблица 6
Результаты расчёта методом релаксации состава равновесной смеси при термической диссоциации изо-пропанола
|
Реакция |
Первый цикл расчёта |
Второй цикл расчёта |
Третий цикл расчета | ||||||
|
1 |
2 |
3 |
1 |
2 |
3 |
1 |
2 |
3 | |
|
1. Изопропанол |
1 |
0.9398 |
0.6843 |
0.6837 |
0.6992 |
0.6968 |
0.6968 |
0.6969 |
0.6969 |
|
2. Водород |
0 |
0 |
0.2555 |
0.2561 |
0.2561 |
0.2585 |
0.2585 |
0.2585 |
0.2585 |
|
3 . н-Пропанол |
0 |
0.0602 |
0.0602 |
0.0602 |
0.0447 |
0.0447 |
0.0446 |
0.0446 |
0.0446 |
|
4. Ацетон |
0 |
0 |
0.2555 |
0.2555 |
0.2555 |
0.2579 |
0.2579 |
0.2579 |
0.2579 |
|
5. Пропионовый Альдегид |
0 |
0 |
0 |
0.0006 |
0.0006 |
0.0006 |
0.0006 |
0.0006 |
0.0006 |
|
6. nt |
1.00 |
1.00 |
1.2555 |
1.2561 |
1.2561 |
1.2585 |
1.2585 |
1.2585 |
1.2585 |
|
Tji |
0,0602 |
|
|
-0.0155 |
|
|
-0.0001 |
|
|
|
М2 |
|
0.2555 |
|
|
0.0024 |
|
|
2(10'6) |
|
|
9-^3 |
|
|
0.0006 |
|
|
3(Ю-5) |
|
|
3{КГ5) |
Как видно из табл.6, достаточно всего трех «проходов», чтобы степень превращения снизилась до 1(И.
