
- •1Врач-анестезиолог, отделение общей анестезиологии, Кливлендский клинический фонд, Кливленд, Огайо, сша.
- •Классификация нервных волокон
- •Электромиография и исследование нервно-мышечной проводимости
- •1Вместо лидокаина можно использовать хлоропрокаин.
- •1В состав гидрокодонсодержащих препаратов входит также и ацетаминофен (викодин, др.).
- •1В состав оксикодонсодержащих препаратов может входить ацетаминофен (перкоцет) или аспирин (перкодан).
- •1В состав некоторых пропоксифенсодержащих препаратов входит ацетаминофен (дарвоцет).
- •1В большинстве случаев авторы не рекомендуют проведение постоянной поддерживающей инфузии.
- •Раздел IV
- •1. Частота сердечных сокращений
- •2. Ударный объем
- •1. Функциональные кривые желудочка
- •2. Оценка систолической функции
- •Фракция выброса
- •3. Оценка диастол ической функции
- •Эндотелиальные факторы
- •Анатомия и физиология коронарного кровообращения
- •1. Анатомия
- •2. Факторы, определяющие величину коронарного кровотока
- •3. Кислородный баланс в миокарде
- •Потребность миокарда в кислороде
- •I. Наджелудочковые аритмии
- •II. Желудочковые аритмии
- •2. Выбор анестетиков и вспомогательных средств:
- •1. Общие принципы
- •2. Премедикация
- •1. Митральный стеноз
- •2. Митральная недостаточность
- •3. Пролапс митрального клапана
- •4. Аортальный стеноз
- •5. Гипертрофическая кардиомиопатия
- •6. Аортальная недостаточность
- •7. Трикуспидальная недостаточность
- •Гипоплазия левых отделов сердца
- •1. Обструктивные поражения
- •2. Простые шунты
- •3. Сложные шунты
- •Внесердечные заболевания
- •Гипогликемия
- •1Частота импульсов автоматически изменяется в зависимости от потребности в сердечном выбросе.— Примеч. Пер.
- •1. Преиндукционный период
- •2. Индукция анестезии
- •3. Предперфузионный период
- •4. Перфузионный период
- •5. Завершение ик
- •6. Постперфузионный период
- •7. Послеоперационный период
- •Анестезия при трансплантации сердца
- •1. Тампонада сердца
- •2. Констриктивныи перикардит
- •Расслаивание аорты
- •1. Аэробный метаболизм
- •2. Анаэробный метаболизм
- •3. Влияние анестезии на клеточный метаболизм
- •1. Грудная клетка и дыхательная мускулатура
- •2. Трахеобронхиальное дерево
- •3. Кровообращение и лимфоток в легких
- •4. Иннервация
- •1.Эластическое сопротивление
- •2. Легочные объемы
- •3. Неэластическое сопротивление
- •4. Работа дыхания
- •5. Влияние анестезии на механику дыхания
- •1. Вентиляция
- •2. Легочный кровоток
- •3. Шунты
- •4. Влияние анестезии на газообмен
- •Напряжение газов в альвеолах, артериальной и венозной крови
- •1.Кислород
- •Высокий альвеолярно-артериальный градиент по кислороду
- •2. Углекислый газ
- •1.Кислород
- •2. Углекислый газ
- •1. Дыхательные центры
- •2. Центральные рецепторы
- •3. Периферические рецепторы
- •4. Влияние анестезии на регуляцию дыхания
- •Состояния, при которых необходима раздельная вентиляция легких
- •Тяжелая гипоксемия при заболевании одного легкого
- •1. Опухоли
- •2. Легочные инфекции
- •3. Бронхоэктазы
- •1. Предоперационный период
- •2. Интраоперационный период
- •3. Послеоперационный период
- •Анестезия при торакоскопических операциях
- •Легочный лимфангиоматоз
- •1. Предоперационный период
- •2. Интраоперационный период
- •3. Послеоперационный период
- •1. Церебральное перфузионное давление
- •2. Ауторегуляция мозгового кровообращения
- •3. Внешние факторы
- •Внутричерепное давление
- •Влияние анестетиков и вспомогательных средств на цнс
- •1. Испаряемые анестетики
- •Мк и внутричерепной объем крови
- •2. Закись азота
- •1.Для индукции анестезии
- •2. Вспомогательные средства
- •3. Вазопрессоры
- •4. Вазодилататоры
- •5. Миорелаксанты
- •Патологическое пристрастие к алкоголю и наркотическим препаратам
- •Как проводят эст?
- •Неосмотическая секреция адг
- •Гиперосмоляльность и гипернатриемия
- •Гипернатриемия при низком содержании натрия в организме
- •Гипоосмоляльность и гипонатриемия
- •Гипонатриемия с повышенной осмоляльностью плазмы
- •Застойная сердечная недостаточность
- •Внепочечные потери
- •Тяжелая физическая нагрузка
- •Изолированное снижение секреции калия в дистальном отделе нефрона
- •Повышенное поступление калия
- •Гиперкальциемия
- •Клинические проявления гиперкальциемии
- •1.Гемолитические реакции
- •2. Негемолитические иммунные реакции
- •Нитропруссид
- •Кислоты и основания
- •Сопряженные пары и буферы
- •Клинические нарушения
- •Компенсаторные механизмы
- •Нервно-мышечные нарушения
- •Травмы и заболевания грудной клетки
- •Болезни плевры
- •Обструкция дыхательных путей
- •Наследственные нарушения обмена веществ
- •Центральная стимуляция дыхания
- •Хлоридчувствительный метаболический алкалоз
- •1. Антагонисты альдостерона
- •2. Неконкурентные калийсберегающие диуретики
- •Сердечно-сосудистая система
- •Предоперационное обследование
- •Миорелаксанты
- •Предоперационный период
Нитропруссид
1Могут быть безопасными при варианте А-.
2Препараты противопоказаны из-за риска возникновения
метгемоглобинемии
Кислотно-основное состояние 30
Практически все химические реакции в организме человека зависят от поддержания концентрации ионов водорода в физиологически допустимых пределах. Концентрация ионов водорода жестко регулируется, поскольку ее изменения могут вызвать дисфункцию многих органов и систем.
Сложную систему регуляции концентрации водородных ионов часто называют кислотно-основным состоянием, знание которого чрезвычайно важно для анестезиолога. Интраоперационные изменения вентиляции и перфузии быстро приводят к изменениям кислотно-основного состояния. Следовательно, чтобы правильно проводить анестезию, необходимо хорошо разбираться в нарушениях кислотно-основного состояния, их влиянии на организм и методах лечения.
В этой главе обсуждается физиология и патофизиология кислотно-основного состояния, а также предлагается системный подход к интерпретации результатов анализа газов крови.
Определения и терминология
Химия кислот и оснований Концентрация ионов водорода и рН
В любом водном растворе молекулы воды обратимо диссоциируют на ионы водорода и гидроксидные ионы:
Н2О ↔ Н+ + ОН-.
Кинетику этого процесса можно описать с помощью константы диссоциации Kw:
KW=[H+] X [OH-] = 10-14.
Концентрацию воды в знаменателе этого уравнения опускают, поскольку она не имеет существенного значения и уже включена в константу. Следовательно, если [Н+] или [ОН~] известна, можно легко рассчитать концентрацию другого иона.
Пример: если [Н+] = 10-8 нмоль/л, тогда [ОН-] = 10-/10-8= 10-6 нмоль/л.
В норме [Н+] артериальной крови составляет 40 нмоль/л (40 X 10-9 моль/л). Проводить расчеты с числами такого порядка крайне неудобно, поэтому концентрацию ионов водорода принято выражать через рН. рН раствора — это отрицательный десятичный логарифм концентрации ионов водорода (рис. 30-1). Следовательно, в норме рН артериальной крови составляет -log (40 X 10-9) = 7,40. Концентрация ионов водорода от 16 до 160 нмоль/л (рН 6,8-7,8) совместима с жизнью.
Как и большинство других констант диссоциации, Kw зависит от температуры. Если температура составляет 25°С, то точка электронейтральности для воды достигается при рН 7,0, если 37 °С — то при рН 6,8. Изменения рН в зависимости от температуры имеют важное значение при гипотермии (гл.21).
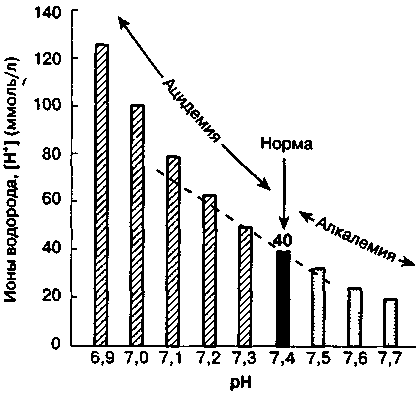
Рис. 30-1. Взаимосвязь между рН и [Н+]. В интервале значений рН от 7,1 до 7,5 зависимость между рН и [Н+] принимает почти линейный характер. (Из: Narms R. G., Emmett M. Simple and Mixed Acid-base Disorders: A Practical Approach. Medicine, 1980; 59:161.)
Кислоты и основания
В соответствии с определением Бренстеда-Лоури, кислотой называют донор протона (Н+), а основанием — акцептор протона. Соответственно, кислотность водного раствора отражает концентрацию FT. Сильной кислотой является вещество, которое легко и почти необратимо отдает Н+ и повышает [Н+] в растворе. Сильное основание, наоборот, активно связывает Н+ и снижает [Н+]. Слабые кислоты обратимо отдают Н+, а слабые основания — обратимо связывают Н+; те и другие оказывают меньшее влияние на [Н+] в растворе, чем сильные кислоты и основания. Большинство биологических соединений являются либо слабыми основаниями, либо слабыми кислотами.
Для растворов, содержащих слабую кислоту НА, где
НА ↔ Н+ + А-,
константу диссоциации К рассчитывают следующим образом:
К = [Н+] х [А-/ [НА], или [Н+] = К х [НА]/ [А-].
Последнее уравнение, представленное в форме отрицательного десятичного логарифма, называют уравнением Гендерсона-Хассельбальха:
pH = pK+log([A-]/[HA]).
Из этого уравнения следует, что рН раствора зависит от величины отношения концентрации аниона к концентрации недиссоциированной кислоты.
