
- •Содержание
- •Общие методические указания
- •Энергетика химических процессов (термохимические расчеты)
- •1. Химическое сродство
- •Контрольные задания
- •2. Химическая кинетика
- •Контрольные задания
- •3. Химическое равновесие
- •Контрольные задания
- •4. Свойства растворов. Гидролиз солеи. Жесткость воды и методы ее устранения
- •Контрольные задания
- •5. Окислительно-восстановительные реакции
- •Контрольные задания
- •Варианты контрольного задания
- •Список литературы
- •Приложение
- •Стандартные теплоты (энтальпии) образования ∆h°298 некоторых веществ
- •Стандартные абсолютные энтропии s°298 некоторых веществ
- •Радиусы атомов (å)
- •Энергия (потенциал) ионизация и электроотрицательность атомов элементов
- •Энергия связи при 298 к (250с)
- •Дипольные моменты μ некоторых молекул
- •Константы диссоциации (Кд) некоторых электролитов в водных растворах при 18-250с
- •Основные классы неорганических веществ
- •Взаимосвязь простых веществ, оксидов, оснований и кислот (реакции солеобразования)
- •Некоторые термодинамические функции при 298 к (250с), 100 кПа
- •Некоторые характеристики веществ при 298 к
- •Произведения растворимости некоторых малорастворимых электролитов при 250с
- •Составитель Заглядимова н.В.
2. Химическая кинетика
Кинетика — учение о скорости различных процессов, в том числе химических реакций. Критерием принципиальной осуществимости реакций является неравенство ∆Gр.т.<0. Но это неравенство не является еще полной гарантией фактического течения процесса в данных условиях, не является достаточным для оценки кинетических возможностей реакции. Так,∆G°298, Н2О (г) = - 228,59 кДж/моль, a∆G°298, АlI3(к) = - 313,8 кДж/моль и, следовательно, при Т = 298 К ир= 1,013-105Па возможны реакции, идущие по уравнениям:
Н2(г) + 1/2О2(г)=Н2О(г); (1)
2А1(к)+3I2(к)=2 АlI3(к). (2)
Однако эти реакции при стандартных условиях идут только в присутствии катализатора (платины для первой и воды для второй). Катализатор как бы снижает кинетический «тормоз», и тогда проявляется термодинамическая природа вещества. Скорость химических реакций зависит от многих факторов, основные из которых — концентрация и давление реагентов, температура и действие катализатора. Эти же факторы определяют и достижение равновесия в реагирующей системе.
ПРИМЕР 1.Во сколько раз изменится скорость прямой и обратной реакции в системе
2SО2(r)+О2(r)↔2SО3(r),
13
если объем газовой смеси уменьшить в три раза? В какую сторону сместится равновесие системы?
Решение
Обозначим концентрации реагирующих веществ: [SО2]=a, [O2]=b, [SO3] =с. Согласно закону действия масс скорости прямой и обратной реакции до изменения объема
![]()
![]()
После уменьшения объема гомогенной системы в 3 раза концентрация каждого из реагирующих веществ увеличится в 3 раза: [SО2]=3a, [О2]=3b, [SО3]=3c. При новых концентрациях скорости и прямой и обратной реакции:
![]()
![]()
Отсюда
![]()
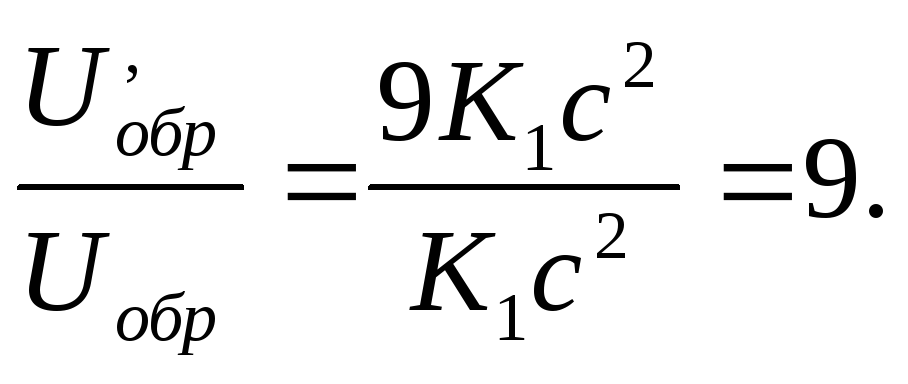
Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной - только в 9 раз. Равновесие системы сместилось в сторону образования SО3.
ПРИМЕР 2.Вычислите, во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 70°С, если температурный коэффициент равен 2.
Решение
Зависимость скорости химической реакции от температуры определяется
эмпирическим правилом Вант-Гоффа по формуле
![]()
![]()
Следовательно, скорость реакции Uт, при температуре 70°С больше скорости реакцииUт1, при температуре 30°С в 16 раз.
ПРИМЕР 3.Константа равновесия гомогенной системы
СО(г)+Н2О(г) ↔ СО2(г)+Н2(г)
при 850°С равна 1. Вычислите концентрации всех веществ при равновесии, если исходные концентрации:
[СО]исх=3 моль/л, [Н2О]исх=2 моль/л
14
Решение
При равновесии скорости прямой и обратной реакции равны, а отношение констант этих скоростей постоянно и называется константой равновесия данной системы:
Uпр=К1[СО][Н2О];Uобр= К2[СО2][Н2];
![]()
В условии задачи даны исходные концентрации, тогда как в выражении Крвходят только равновесные концентрации всех веществ системы. Предположим, что к моменту равновесия концентрация [СО2]2= х моль/л. Согласно уравнению системы число молей образовавшегося водорода при этом будет также х моль/л. По столько же молей (х моль/л) СО и Н2Oрасходуются для образования х молей СO2и Н2. Следовательно, равновесные концентрации всех четырех веществ
[СО2]р= [Н2]р=х моль/л; [CO]p= (3—х) моль/л;
[Н2О]р= (2—х) моль/л.
Зная константу равновесия, находим значение х, а затем исходные концентрации всех веществ:
![]()
х2= 6—2х—Зх+х2; 5х = 6, л: =1,2 моль/л.
Таким образом, искомые равновесные концентрации:
[СO2]Р=1,2 моль/л; [Н2]р=1,2 моль/л;
[CO]p=3 - 1,2= 1,8 моль/л; [Н2О]Р=2 - 1,2=0,8 моль/л.
ПРИМЕР 4. Эндотермическая реакция разложения пентахлорида фосфора протекает по уравнению
РС15(г)↔РС13(г)+С12(г); ∆Н= +92,59 кДж.
Как надо изменить: а) температуру; б) давление; в) концентрацию, чтобы сместить равновесие в сторону прямой реакции — разложения PCl5?
Решение
Смещением или сдвигом химического равновесия называют изменение равновесных концентраций реагирующих веществ в результате изменения
одного из условий реакции. Направление, в котором сместилось равновесие, определяется по принципу Ле-Шателье: а) так как реакция разложения РС15эндотермическая (∆Н>0), то для смещения равновесия в сторону прямой реакции нужно повысить температуру; б) так как в данной системе
15
разложение PCl5ведет к увеличению объема (из одной молекулы газа образуются две газообразные молекулы), то для смещения равновесия в сторону прямой реакции надо уменьшить давление; в) смещения равновесия в указанном направлении можно достигнуть как увеличением концентрации PCl5, так и уменьшением концентрации РСl3или С12.
