
35.07 Процеси і апарати. Адсорбція
.pdfМІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ ХАРЧОВИХ ТЕХНОЛОГІЙ
ЗАТВЕРДЖУЮ
Ректор _____________ С.В.Іванов
(Підпис)
«____» ______________ 20__ р.
ПРОЦЕСИ І АПАРАТИ ХАРЧОВИХ ВИРОБНИЦТВ
МЕТОДИЧНІ РЕКОМЕНДАЦІЇ до вивчення розділу «Абсорбція»
для студентів напрямів підготовки 6.051701 «Харчові технології та інженерія», 6.050502 “Інженерна механіка”, 6.050503 “Машинобудування”
денної та заочної форм навчання
Всі цитати, цифровий та фактичний матеріал, |
СХВАЛЕНО |
бібліографічні відомості перевірені. |
на засіданні кафедри |
Написання одиниць відповідає стандартам |
процесів і апаратів |
|
харчових виробництв |
Підписи укладачів |
Протокол № 4 |
______________________ О.С. Марценюк |
від 21 листопада 2013 р. |
______________________ Л.В. Зоткіна |
|
______________________ Ю.В.Запорожець |
|
______________________ Н.А.Ткачук |
|
«____» ______________ 20__ р. |
|
Реєстраційний номер |
|
електронних методичних |
|
рекомендацій у НМВ |
|
___35.07 – 28.11.2013____ |
|
КИЇВ НУХТ 2013
Процеси і апарати харчових виробництв[Електронний ресурс]: метод. рекомендації до вивч. розділу «Абсорбція» для студентів напрямів підготовки 6.051701 «Харчові технології та інженерія», 6.050502 “Інженерна механіка”, 6.050503 “Машинобудування” ден. та заоч. форм навч. / уклад. О.С. Марценюк, Л.В. Зоткіна, Ю.В. Запорожець, Н.А. Ткачук,– К.: НУХТ, 2013. – 49 с.
Рецензент І.Ф. Малежик, д-р техн. наук, проф.
Укладачі: О.С. Марценюк, д-р техн. наук, проф.
Л.В.Зоткіна, Ю.В.Запорожець,
Н.А.Ткачук, кандидати техн. наук, доценти
Відповідальний за випуск О.Ю.Шевченко, д-р техн. наук, проф.
Подано в авторській редакції
|
|
|
|
|
ВСТУП |
|
|
|
|
|
|
|
|
|
Дисципліна «Процеси і апарати харчових виробництв» завершує загально- |
|
|||||||||||
інженерну підготовку студентів і готує їх до вивчення спеціальних дисциплін |
|
||||||||||||
навчального |
плану. Розділ «Абсорбція» є |
важливим |
при |
вивченні |
дисципліни |
|
|||||||
«Процеси і апарати харчових виробництв». |
|
|
|
|
|
|
|
|
|||||
|
Абсорбція – вибіркове поглинання рідиною певних компонентів із газової |
|
|||||||||||
фази – застосовується, або відбувається спонтанно(самовільно), в усіх галузях |
|
||||||||||||
харчового |
виробництва, і |
найпоширеніша |
|
у |
цукровій |
галузі(сатурація, |
|
||||||
сульфітація), |
спиртовій (уловлювання етилового спирту із газів бродіння, |
|
|||||||||||
виробництво |
|
вуглекислоти), |
виноробстві |
(сульфітація |
|
виноматеріалів), |
|
||||||
олієжировій галузі (дезодорація жирів, відгонка екстрагентів, при виробництві |
|
||||||||||||
пива і газових напоїв |
|
|
|
|
|
|
|
|
|
|
|||
|
Особливістю цього процесу є те, що при розгляді питань фазової рівноваги і |
|
|||||||||||
виконання розрахунків концентрації компонентів |
виражають різними |
способами |
|
||||||||||
(у різних одиницях виміру). Наприклад знадно з законом Генрі рівноважний |
|
||||||||||||
парціальний |
тиск компонентів у газовій фазі(Па) |
визначається |
його |
мольною |
|
||||||||
часткою (кмоль компонента/кмоль суміші – безрозмірна величина). У рідкій фазі, |
|
||||||||||||
при |
складанні |
матеріально |
балансу |
|
на |
основі |
закону |
збереження |
м |
||||
користуються відносними масовими концентраціями(кг компонента/кг інертного |
|
||||||||||||
носія – безрозмірна величина). Користуються також іншими способами вираження |
|
||||||||||||
концентрації: |
процентами |
масовими |
та |
|
об’ємни, масовими |
частками, |
|
||||||
об’ємними масовими і мольними концентраціями.
Укожній окремій розрахунковій формулі концентрації повинні бути виражені
воднакових одиницях виміру, що вимагає навичок застосування формул для
перерахунку концентрацій, виражених різними способами. Недостатнє висвітлення цього питання в основному підручнику з процесів і апаратів[1] компенсується даними методичними рекомендаціями.
Також приводиться не розглянуті в підручнику матеріали про застосування нерегулярних насадок, неізотермічну абсорбцію, графічну побудову та розрахунок
кількості |
одиниць |
перенесення |
.масиРозгляд |
цих |
питань |
ілюструється |
прикладами розв’язання задач. |
|
|
|
|
||
|
|
1. |
|
АБСОРБЦІЯ |
|
|
|
|
|
Процес абсорбції – це вибіркове поглинання об'ємом рідини(розчинення у |
|
||||||
рідині) певних компонентів із газової або парової суміші. Виділення з рідини |
|
|||||||
розчиненого в ній компонента називають десорбцією. |
|
|
|
|
||||
|
Причиною (рушійною силою) переходу компонента з однієї фази в іншу(за |
|
||||||
рівності температур і тисків у |
контактуючих ) |
фазахєрізниця |
хімічних |
|
||||
потенціалів, визначених по газовій або рідкій фазі. Компонент переходить із фази |
|
|||||||
з більшим значенням хімічного потенціалу у фазу з меншим його значенням. У |
|
|||||||
разі |
однакових |
значень |
хімічних |
потенціалів |
компонента |
в |
обох |
фа |
встановлюється фазова рівновага, під |
час якої загальна кількість молекул |
|
||||||
компонента, що |
внаслідок дифузії переходять із газової |
фази в рідку, дорівнює |
|
|||||
такій же кількості молекул, що переходять із рідкої фази у газову.
У технічних розрахунках користуються не хімічними потенціал, ами величинами, що легше визначаються – концентраціями. Але при цьому однаковим значенням хімічного потенціалу компонента А відповідають різні концентрації
цього ж компонента у рідкій і газовій фазах. Концентрації компонентів А і В у |
|
||||
фазах двофазних систем виражають різними способами, найчастіше у величинах, |
|
||||
приведених |
у |
додатках(табл.1). Мольними |
величинами |
користуються |
у |
розрахунках, пов'язаних з фазовою рівновагою і визначенням рушійної ,сили масовими – переважно у розрахунках матеріальних потоків робочих середовищ.
Формули для перерахунку концентраційу рідкій фазі подані у додатках
(табл. 2). Для газової фази справедливі ті ж самі співвідношення, але з заміною позначень x на y, X на Y, Cx на Cy.
У газовій фазі концентрація компонента може бути виражена також через його парціальний тиск. На основі рівнянь Клапейрона і Дальтона мольна(і рівна
їй об'ємна) частка y будь–якого компонента суміші ідеальних газів |
|
|
||||
|
|
y = p / P, |
|
|
|
(1.1) |
де р – парціальний тиск компонента суміші, Па; |
|
|
|
|||
Р – загальний тиск суміші газів (парів), рівний сумі парціальних тисків усіх |
||||||
компонентів Р = pA + pB + pC +..., Па. |
і |
парціальних |
тисків |
рівняння(1.1) |
||
Для |
рівноважних |
концентрацій |
||||
переписується у вигляді |
y* = p*/P. |
|
|
(1.1а) |
||
|
|
|
|
|||
Рівноважний парціальний тиск компонента |
у газовій фазі *р визначається |
|||||
його мольною часткою x у рідкій фазі(рідку фазу приймають за визначальну) і
описується законом Генрі |
|
р* = Ех, |
(1.2) |
де Е – коефіцієнт Генрі, що залежить від природи і температури контактуючих фаз, Па. (Величина х, як відношення кіломолів(кмоль компонента ,Ащо
поглинається/кмоль суміші компонента А і інертного носія) безрозмірніснаВ , тому коефіцієнт Е має розмірність тиску, Па, мм рт. ст.
Значення Е для водних розчинів деяких газів подані в додатках(табл. 3).
Добре розчинні гази(аміак, діоксид сірки) у табл. |
3 відсутні, |
оскільки |
закону |
||||
Генрі не підкоряються. |
|
|
|
|
|
|
|
Підставивши у рівняння (2) значення р*=y·P за рівнянням (1а), маємо: |
|
||||||
|
|
y* = mx, |
|
|
|
|
(1.3) |
де y* – мольна частка компонента у газовій фазі, рівноважна з рідиною; |
|
||||||
m = E/P – |
безрозмірнісний |
коефіцієнт |
(коефіцієнт |
розподілу), що |
|||
характеризує дану |
систему |
газ– рідина |
при t = const і P = const і за графічною |
||||
інтерпретацією m = y*/Δx* |
є тангенсом |
кута нахилу лінії |
фазової |
рівноваги, |
|||
побудованої в координатах x – y. |
|
|
|
|
|
||
Для розчинів ідеальних газів, до яких відносяться переважно малорозчинні |
|||||||
гази, коефіцієнти |
Генрі постійні і лінії |
фазової |
рівноваги |
за рівнянням(1.3) – |
|||
прямі. Реальні гази підпорядковуються закону Генрі у зоні низьких концентрацій
(поблизу |
початку |
координат), де лінія фазової рівноваги має прямолінійний |
відрізок. |
Рівноважні |
концентрації реальних(добре розчинних) газів описують |
складнішими рівняннями або наводять у вигляді таблиць. Зі зростанням тиску коефіцієнт розподілу m зменшується, а з підвищенням температури– збільшується. Відповідно розчинність газів збільшується зі зростанням тиску і
зниженням температури. |
|
|
|
Наявність |
у воді розчинених ,солейособливо |
електролітів, |
знижує |
розчинність газів. Наприклад, розчинність діоксиду |
вуглецюV, у |
л/л, у |
|
безалкогольних напоях, що містять солі. |
|
|
|
|
V = Vче–0,8 с, |
|
(1.4) |
де Vч – розчинність діоксиду вуглецю у чистій воді, л/л; с – концентрація солей, г/л.
Основне рівняння масопередачіM = K cF під час безперервної абсорбції
може бути виражене через рушійну силу у газовій фазі( y = y*– y) або у рідкій фазі ( x = x – x* ):
|
M= Ky Dyc F |
(1.5) |
або |
М= Kx Dxc F , |
(1.6) |
де М – витрата компонента, що переходить з однієї фази в другу, кмоль/с; |
||
F – площа поверхні масопередачі, м2 ; |
|
|
K y – коефіцієнт |
масопередачі, віднесений |
до рушійної сили y,∆ вираженої |
через мольні частки компонента в газовій фазі, кмоль/( м2 ·с);
K x – коефіцієнт масопередачі, віднесений до рушійної сили ∆x, вираженої через мольні частки компонента у рідкій фазі, кмоль/( м2 ·с);
Dyc і Dxc – відповідно середні для всього процесу рушійні сили.
В останніх двох рівняннях замість мольних витрат і концентрацій можуть бути масові, а замість Dyc може бути DYc , DCyc і Dpc ; відповідно, замість Dxc
можуть бути DX c або DCxc .
Якщо допустити, що поверхня поділу фаз не чинить дифузійного опору
перенесенню компонента і на ній існує фазова рівновага, |
рівняння рівноваги |
описуються прямими лініями ( y* = mx або y* = mx + b), то отримаємо залежності |
|
між коефіцієнтами масопередачі K y і K x і фазовими коефіцієнтами масовіддачі by і |
|
bx , кмоль/( м2 ·с):
К y |
= |
|
1 |
|
|
|
|
; |
|
(1.7) |
|
|
1 |
+ |
|
m |
|
|
|||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
bx |
|
|
|
|
||
|
|
|
by |
|
|
|
|
|
|||
К x |
= |
|
1 |
|
|
|
, |
(1.8) |
|||
|
1 |
+ |
|
1 |
|||||||
|
|
|
|
|
|
||||||
|
|
|
mby |
bx |
|
|
|||||
|
|
|
|
|
|
|
|||||
де m– тангенс кута нахилу лінії рівноваги.
Слід звернути увагу на ,тещо рівняння (1.7) і (1.8) справедливі лише в одиницях виміру рушійної сили у рідкій і газовій фазах у кмоль компонента А/кмоль суміші компонентів (А+В), тобто коли Ky ,Kx ,by і bx виражені у
кмоль /(м2 × с) = |
кмоль |
або |
|
кмоль |
. |
|
м2 × с |
кмоль |
|
м2 × с(Dy =1) |
|||
|
|
|
|
|||
|
кмоль |
|
|
|||
|
|
|
|
|
|
|
Знаменники рівнянь (1.7) |
і (1.8) |
являють собою загальні дифузійні опори, |
||||
рівні сумі дифузійних опорів газової і рідкої фаз і відповідають уявленням про механізм перенесення компонента під час абсорбції. За цими уявленнями компонент із газової фази спочатку переноситься до поверхні поділу фаз з коефіцієнтом масовіддачі by (дифузійний опір 1/ by ), проходить крізь поверхню
поділу фаз (яка не чинить дифузійного опору), а потім переноситься в середину потоку рідкої фази з коефіцієнтом масовіддачі bx (дифузійний опір m / bx ). Процес масопередачі гальмується переважно у фазі з більшим дифузійним опором(з
меншим коефіцієнтом масовіддачі). |
|
|
|
||
З рівняння (1.7) |
випливає, що коли основний дифузійний опір зосереджений |
||||
у газовій фазі(добре |
розчинні газі), тобто за умови |
m |
< |
1 |
маємо K y » by . Ця |
bx |
|
||||
|
|
|
by |
||
умова реалізується при малих кутах нахилу лінії рівноваги та великих значеннях коефіцієнта масовіддачі у рідкій фазіbx і означає, що перенесення компонента гальмується опором газової фази. Для зменшення опору газової фази її потрібно

додатково турбулізувати (вибирати контактні пристрої, які |
турбулізують газову |
||||
фазу). |
1 |
|
1 |
|
|
Аналогічний аналіз рівняння (1.8) показує, що при |
< |
маємо Kx » bx , |
|||
mby |
|||||
|
|||||
|
|
bx |
|||
тобто для прискорення міжфазного перенесення малорозчинних газів(основний дифузійний опір зосереджений у рідкій )фазіпотрібно вибирати апарати з турбулізованою рідкою фазою.
Коефіцієнти масовіддачі розраховують за виведеними на основі теорії подібності критеріальними рівняннями, у яких коефіцієнти і показники степенів визначаються експериментально для різних умов процесу і типів контактних пристроїв. Наприклад, для абсорберів з неупорядкованою засипаною в навал насадкою при плівковому режимі течії (10 ≤ Rеp ≤ 10000) маємо:
а) Для газової фази
Nu¢ = 0, 407 |
× Re0,655 |
(Pr¢)0,33 |
, |
(1.9) |
г |
г |
г |
|
|
де Nuг¢ = bг de – дифузійний критерій Нуссельта для газу;
Dг
Reг = 4wrг – модифікований критерій Рейнольдса для газу; smг
Prг¢ = |
mг |
– дифузійний критерій Прандля для газу; |
|
|
|
|
|||||
rг Dг |
|
|
|
|
|||||||
|
|
м |
|
кмоль |
|
кг |
|
||||
bг – коефіцієнт масовіддачі для газу, |
= |
= |
; |
||||||||
|
|
кмоль |
|
кг |
|||||||
|
|
|
c |
м2 × с |
|
м2 × с |
|
||||
|
|
|
м3 |
|
м3 |
|
|||||
|
|
|
|
|
|
|
|
|
|||
Dг – коефіцієнт дифузії компонента в газі, м2 /с ; de – еквівалентний діаметр насадки, de=4Vв/s , м; Vв– вільний об’єм насадки, м3/м3;
s – питома поверхня насадки, м2/м3;
w – швидкість газу, розрахована на повний переріз колони (фіктивна), м/с; rг – густина газу, кг/м3;
mг – динамічний коефіцієнт в’язкості газу, Па·с. б) Для рідкої фази
|
|
bpdпр |
Nu'p=0,0021Rep0,75(Pг'p)0,5, |
(1.10) |
де Nu¢p |
= |
– дифузійний критерій Нуссельта для рідини; |
|
|
|
|
|||
|
|
Dp |
|
|
Rep |
= |
4L |
– модифікований критерій Рейнольдса для рідини; |
|
Ssymp |
||||
|
|
|
Prp¢ = |
|
mp |
|
– дифузійний критерій Прандтля для рідини; |
|
|
|
||||||||||||||
rp Dp |
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
æ |
m2 |
ö1/ 3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
d |
|
= ç |
p |
÷ – приведена товщина плівки рідини; |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
пр |
ç r2 g |
÷ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
è |
p |
ø |
|
|
|
м |
|
кмоль |
|
|
|
кг |
|
||||||
bр – коефіцієнт масовіддачі для рідини, |
= |
|
= |
|
; |
||||||||||||||||
|
|
|
кмоль |
|
|
|
кг |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
c |
м2 ×с |
|
|
м2 |
×с |
|
|||||
D |
– коефіцієнт дифузії компонента у рідині м2/с; |
м3 |
|
|
|
|
м3 |
|
|||||||||||||
|
p |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
L – масова витрата рідини, кг/с; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
rp |
і mp – густина, кг/м3, і динамічний коефіцієнт в’язкості, Па·с, рідини; |
||||||||||||||||||||
g – прискорення вільного падіння, g = 9,81 м/с2. |
|
|
|
|
|
|
|
||||||||||||||
Вираз для критерію Rep отримано наступним чином. |
|
|
|
|
|
|
|||||||||||||||
Зрошуваний рідиною (змочений) периметр перерізу абсорбера, м |
|||||||||||||||||||||
|
|
|
|
|
|
П = F / Hн = Ssy , |
|
|
|
|
|
|
|
||||||||
де F– поверхня контакту фаз, м2; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Нн – висота шару насадки, м; |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
S = p D 2 / 4 |
– площа поперечного перерізу колони діаметром D, м2 |
||||||||||||||||||||
s – питома поверхня сухої насадки, м2/м3; |
|
|
|
|
|
|
|
|
|
||||||||||||
y – безрозмірнісний коефіцієнт змоченості насадки. |
|
|
|
|
|
|
|||||||||||||||
Швидкість течії плівки рідини через насадку: |
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
w |
= |
L |
= |
|
|
L |
, |
|
|
|
|
|
|
||
|
|
|
|
|
|
rp Пd |
rpSsyd |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
пл |
|
|
|
|
|
|
|
|
|
|
|||||
де d – середня товщина плівки, м. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Еквівалентний діаметр плівки рідини: |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
dпл = 4Пd / П = 4d .
Підставивши ці значення у вираз для критерію Re p , отримаємо:
Rep = |
wплdпл rp |
= |
4L |
(1.11) |
|
mp |
Sdymp |
||||
|
|
|
|||
Матеріальний баланс абсорбера складають |
виходячи з того, що рідкий |
||||
поглинач (абсорбент) нелеткий і його маса у процесі залишається незмінною; змінюється лише вміст у ньому поглинутого компонента. Також вважають, що інертний газ не розчиняється в рідині і його маса теж не змінюється. Тому
концентрації |
|
компонента |
у газі |
і |
в рідині виражають у відносних масових |
|||||||||
одиницях. |
Згідно |
з |
.1.рис1 |
із |
рівняння |
матеріального |
балансу |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
LX |
п + GYп = LX к + GYк |
маємо: |
|
|
|
|
||||||||
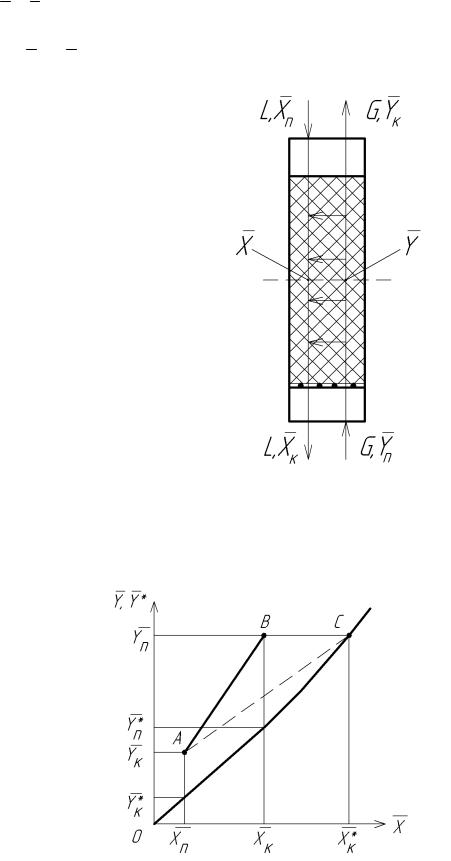
|
|
|
|
|
|
|
|
|
|
M = G(Yп -Yк ) L=( Xк - Xп ), |
(1.12) |
||||||||
де M – витрата компонента, що переходить у суміжну фазу, кг/с, G i L – витрати інертного газу і рідкого поглинача, кг/с;
Yп i Yк – початкова і кінцева відносні масові концентрації компонента у газовій фазі (на вході в апарат і виході з нього), кг компонента/кг інертного газу;
Xп і Xк – початкова і кінцева концентрації компонента у рідкому поглиначі, кг компонента/кг рідкого поглинача.
|
|
У |
Рис.1.1. Матеріальний баланс процесу абсорбції |
|
|
|||||||||
|
|
|
|
|
|
|
робочою лінією процесу |
і |
при |
|||||
координатах X |
- Y рівняння (1.12) є |
|||||||||||||
постійних G i L зображується відрізком прямої, |
|
|
|
|
ù |
і |
||||||||
обмеженої точками B éY |
, X |
|||||||||||||
|
|
|
|
|
|
|
|
|
ë п |
к û |
|
|||
|
|
|
|
ù , показаної на рис.1.2 . |
|
|
|
|
|
|
||||
A éY |
, X |
|
|
|
|
|
|
|||||||
ë к |
п û |
|
|
|
|
|
|
|||||||
Рис.1. 2. Робоча АВ і рівноважна ОС лінії процесу абсорбції

Рівняння цієї прямої – робочої лінії АВ
Y = Y п + L / G( X - Xк )
або
Y = Y к + L / G( X - Xп )
де Y і X – змінні по висоті колони концентрації компонента, що поглинається, в контактуючих нерівноважних потоках газу і рідини в розглядуваному перерізі апарата.
Мінімальну витрату рідкого сорбента Lmin отримаємо за умови рівноважного значення сорбенту на виході з апарата
Lmin = |
|
|
|
M |
, кг/с. |
(1.13) |
|||
|
|
|
к* - X |
п |
|||||
X |
|
|
|
||||||
Дійсна витрата сорбента, кг/с |
|
|
|
|
|
|
|
|
|
L = Lmin ×j , |
|
|
|||||||
де j > 1 – коефіцієнт надлишку рідкого сорбента. |
|
|
|||||||
Питома витрата сорбента |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
l = |
L |
= |
|
Y |
п - Yк |
|
, кг/кг. |
|
|
|
|
|
|
|
|
|
||||
|
|
G X к - X п |
|
|||||||
Рушійною силою абсорбції (за газовою фазою) у будь-якому перерізі апарата |
||||||||||
є різниця |
між концентрацією компонента у газовій фазі |
і рівноважн |
||||||||
концентрацією |
компонента у цій же фазі, яка відповідає існуючій у |
даному |
||||||||
перерізі концентрації компонента у рідкій фазі. Вона може бути виражена у будь- |
||||||||||
яких одиницях виміру додаток (табл. 1), проте при використанні у матеріальному балансі її виражають у тих же одиницях(відносних масових частках), що
використовуються |
|
|
|
|
|
|
|
|
|
|
* . У розрахунках абсорберів |
|
рушійну |
|||||||||
у балансі: DY |
=Y |
-Y |
||||||||||||||||||||
силу часто виражають у одиницях тиску. |
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
Якщо у координатах X |
- Y побудувати лінію рівноваги OС і робочу лінію |
|||||||||||||||||||
АВ, то згідно рис. 2 рушійна сила у точці В (нижній переріз апарата) буде |
|
|
|
|
|
|||||||||||||||||
Y |
-Y * . |
|||||||||||||||||||||
|
|
У загальному рівнянні масопередачі |
|
п п |
||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
M = KY |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
DYcep × F, |
(1.14) |
||||||||||||
де M – витрата компонента, що поглинається, кг/с; KY |
– коефіцієнт масопередачі, |
|||||||||||||||||||||
|
|
кг |
|
; F – поверхня масопередачі, м2, використовується середня |
||||||||||||||||||
|
м2 ×с |
кг |
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
кг інертного газу
рушійна сила DYсер , кг/кг інертного газу.
За умови, що в межах від Xп до Xк лінія рівноваги пряма, середня рушійна
сила
