
- •Львівський національний медичний університет
- •Модуль 2. Загальні закономірності метаболізму Тематичний план практичних занять з модуля 2
- •Завдання для самостійної роботи студентів (срс)
- •Модуль 2. Загальні закономірності метаболізму.
- •Теоретичні питання
- •Наукові напрямки роботи кафедри біохімії
- •Практична робота Визначення оптичної густини забарвлених розчинів у залежності від їх концентрації.
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Дослід 2. Дослідження термолабільності амілази слини.
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •1/16 Мл сечі розщеплює 2 мл 0,1 %-го розчину крохмалю;
- •1Мл сечі розщеплює - х мл 0,1 %-го розчину крохмалю,
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Література Основна:
- •Аналізувати зміни активності індикаторних ферментів плазми крові при патологіях певних органів та тканин. Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •А. Амілази, ліпази, фосфатази
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •А. Ацетил-КоА
- •Література Основна:
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •1. Дослідження дії якого з перерахованих ферментів базується на знебарвленні бензидину при його окисненні?
- •3. За яких умов відбувається забарвлення пірокатехіну при окисненні його молекулярним киснем в присутності фенолоксидази:
- •Приклади тестів “Крок-1”
- •Література Основна:
- •Теоретичні питання
- •Практична робота Дослід 1.Вивчення окисного фосфорилування в мітохондріях та дії роз’єднувача – 2,4-динітрофенолу на цей процес.
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •2. Універсальність хеміоосмотичної теорії для живих систем. Література Основна:
- •Теоретичні питання
- •Приклади тестового контролю знань.
- •А. Аконітатгідратази
- •Приклади тестів та ситуаційних задач по засвоєнню практичних навичок
- •Література Основна:
- •Модуль 3. Метаболізм Вуглеводів, ліпідів, амінокислот та його регуляція
- •Тематичний план практичних занять з модуля 3 Завдання для самостійної роботи студентів (срс)
- •Змістовий модуль 9. Метаболізм вуглеводів та його регуляція
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок -1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів “Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •2. Реакція з феруму хлоридом (III) (проба Герхарда).
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Отримання калібрувальних розчинів
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Тема № 9. Дослідження процесів детоксикації аміаку та біосинтезу сечовини.
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Індивідуальна самостійна робота студентів
- •Література
- •Теоретичні питання
- •Практична робота
- •Контроль виконання лабораторної роботи
- •Приклади тестів „Крок-1”
- •Самостійна індивідуальна робота студентів
- •Література
- •Теоретичні питання
- •Приклади тестового контролю знань „Крок 1”
- •Приклади тестів та ситуаційних задач по засвоєнню практичних навичок
- •Література
Практична робота
Дослід 1. Визначення вмісту сечовини в сечі.
Принцип методу. Метод базується на здатності сечовини, що містить аміногрупи, утворювати з парадиметиламінобензальдегідом в кислому середовищі комплексну сполуку, забарвлену в жовтий колір. Інтенсивність забарвлення прямо пропорційна концентрації сечовини в досліджуваній сечі і визначається фотоколориметрично.
Матеріальне забезпечення: сеча; 2 %-ний розчин парадиметил-амінобензальдегіду (ПДМАБА); стандартний розчин сечовини (2,5 %); ФЕК, піпетки, мікропіпетки, сухі пробірки.
Хід роботи. У пробірку наливають 0,2 мл сечі, додають 1,2 мл розчину ПДМАБА і ретельно перемішують. Через 15 хв пробу фотометрують в сухих кюветах шириною 3 мм (синій світлофільтр, λ = 450-480 нм) проти води. Показник Е для контролю – 0,08. Для визначення вмісту сечовини в сечі користуються готовим калібрувальним графіком (0,5; 1,0; 1,5; 2,0; 2,5 г сечовини в 100 мл) і розраховують кількість сечовини в г/добу. При побудові калібрувального графіку використовують стандартні розчини сечовини (замість сечі беруть 0,2 мл кожного стандарту, обробляють так само, як і сечу, і аналогічно фотометрують). Коефіцієнт перерахунку в одиниці СІ (ммоль/добу) дорівнює 16,65.
Пояснити отримані результати. Зробити висновок.
Дослід 2. Визначення вмісту сечовини в сироватці крові та сечі за реакцією з діацетилмонооксимом.
Принцип методу. Сечовина в кислому середовищі за наявності тіосемикарбазиду і солей феруму утворює з діацетилмонооксимом комплексну сполуку червоного кольору, оптична густина якої при зеленому світлофільтрі (500-560 нм) пропорційна концентрації сечовини.
 діацетилмонооксим
діацетил гідроксиламін
діацетилмонооксим
діацетил гідроксиламін
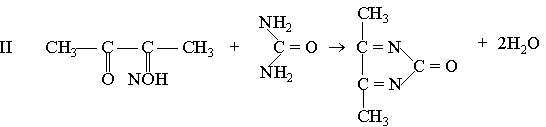
діацетил сечовина діазинове похідне
Матеріальне забезпечення: розчин трихлорацетатної кислоти (ТХАК) (100 г/л), діацетилмонооксим (25 г/л, водний стабільний розчин), тіосемикарбазид (2,5 г/л водний розчин стабільний при зберіганні у темному посуді за кімнатної температури), кислота сульфатна, конц.(96 %), кислота ортофосфорна (85 %), розчин феруму хлориду (основний розчин – 5 г феруму хлориду доводять до 100 мл водою і підкислюють додаванням 1 мл сульфатної кислоти конц.; з основного розчина готують робочий: 1 мл основного розчину феруму хлориду доводять до 100 мл водою, додають 8 мл конц. сульфатної кислоти і 1 мл 85 % ортофосфатної кислоти; зберігають 2 тижні у темному посуді), розчин бензойної кислоти (2 г/л), розчин сечовини (7 ммоль/л – 42г/100 мл), кольоровий реактив (до 30 мл робочого розчину феруму хлориду додають 20 мл води, 1 мл розчину діацетилмонооксиму і 0,25 мл розчину тіосемикарбазиду; кольоровий розчин готують кожен раз перед використанням), спектрофотометр, водяна баня з температурою 100 С, сироватка крові, добова сеча профільтрована, розведена ізотонічним розчином натрію хлориду або дистильованою водою 1:50 або 1:100.
Хід роботи. Визначення з депротеїнуванням. Зразки: сироватка (плазма) крові ліпемічна або гемолізована; цільна кров (плазма).
Хід визначення проводять за наступною схемою:
|
|
Контрольна проба, мл |
Стандартна проба, мл |
Дослідна проба, мл |
|
Н2О |
1,0 |
0,8 |
0,8 |
|
Розчин ТХАК |
1,0 |
1,0 |
1,0 |
|
Досліджуваний зразок |
- |
- |
0,2 |
|
Стандартний розчин сечовини |
- |
0,2 |
- |
|
Перемішати і центрифугувати 10 хвилин при 3000 об/хв. | |||
|
Надосадова рідина |
0,5 |
0,5 |
0,5 |
|
Кольоровий розчин |
5,0 |
5,0 |
5,0 |
Вміст пробірок ретельно перемішують, отвір закривають алюмінієвою фольгою і пробірки ставлять у киплячу водяну баню точно на 20 хв. Потім пробірки швидко охолоджують водою і вимірюють оптичну густину стандартної (Астанд.) та дослідної (Адосл.) проб при зеленому світлофільтрі (500-560 нм) проти контрольної проби в кюветі товщиною 1,0 см. Забарвлення є стійким протягом 15 хв. Звернути увагу на наступне: якщо вміст сечовини в пробі перевищує 17 ммоль/л, пробу необхідно розвести дистильованою водою і аналіз провести повторно. Результат необхідно перемножити на розведення.
Розрахунок вмісту сечовини проводять за формулою:
Адосл.
С =
7 де:
=
7 де:
Астанд.
С – вміст сечовини в дослідній пробі, ммоль/л;
Адосл. – оптична густина дослідної проби;
Астанд. – оптична густина стандартної проби;
7 – вміст сечовини у стандартному розчині, ммоль/л.
Пояснити отриманий результат. Зробити висновок.
Клініко-діагностичне значення. Синтез сечовини відбувається в печінці (цитозоль і мітохондрії) головним чином з аміаку, який утворюється при дезамінуванні амінокислот, розпаді пуринових і піримідинових нуклеотидів. За добу з сечею здорової людини виділяється 20-35 г або 333-583 ммоль сечовини. В нормі вміст сечовини в сироватці крові становить 3,3- 8,3 ммоль/л.
Відхилення від нормального вмісту залежать від інтенсивності процесів синтезу сечовини та її виведення.
Збільшення вмісту сечовини в сироватці крові є однією з головних ознак порушення видільної функції нирок. Крім того, зростання рівня сечовини у сироватці крові може бути нениркового походження – при втраті організмом рідини (блювання, пронос, зневоднення), при посиленому розпаді білків (гостра жирова дистрофія печінки).
Зменшення вмісту сечовини може спостерігатися при захворюваннях печінки (паренхіматозна жовтяниця, цироз печінки) внаслідок порушення синтезу сечовини в печінці.
Підвищений вміст сечовини у сечі спостерігається при дефіциті білка в їжі, при злоякісній анемії, гарячці, інтенсивному розпаді білків в організмі, після прийому саліцилатів, при отруєнні фосфором.
Знижений вміст сечовини спостерігається при цирозі печінки, паренхіматозній жовтяниці, нефриті, ацидозі, уремії.
Дослід 3. Проба Фелінга. Якісна реакція на фенілпіровиноградну кислоту.
Принцип методу. Фенілпіровиноградна кислота утворює з іонами трьохвалентного феруму комплексну сполуку, забарвлену у синьо-зелений колір.
Матеріальне забезпечення: сеча хворого на фенілкетонурію, 10 %-ний розчин феруму хлориду, крапельниці, фільтри, піпетки.
Хід роботи. До 2 мл свіжовідфільтрованої сечі наливають 8-10 крапель 10% розчину FeCl3. За наявності у сечі фенілпіровиноградної кислоти через 30-60 сек з’являється синьо-зелене забарвлення, яке зникає поступово протягом 5-30 хв в залежності від концентрації фенілпіровиноградної кислоти в сечі.
Клініко-діагностичне значення. Вроджена відсутність у дітей в печінці ферменту фенілаланін-4-монооксигенази призводить до блокування окиснення фенілаланіну в тирозин і, відповідно, всіх подальших метаболічних перетворень тирозину. Нагромадження у крові та тканинах фенілаланіну та продуктів його розпаду, в тому числі фенілпіровиноградної кислоти, викликає інтоксикацію організму. Наслідком цього є порушення нормального розвитку мозку і важкі нервові розлади. Діагностичним критерієм цього спадкового захворювання є підвищений вміст фенілаланіну в крові, наявність фенілпіровиноградної кислоти в сечі. В нормі концентрація фенілаланіну в крові дітей в середньому становить: до 1 місяця – 0,133 ммоль/л, від 1 місяця до 1 року – 0,095 ммоль/л, від 1 року до 14 років – 0,115 ммоль/л.
Пробу на фенілпіровиноградну кислоту можна проводити на фільтрувальному папері. Смужку фільтрувального паперу змочують сечею, висушують на повітрі і наносять краплю 10% розчину FeCl3. Позитивна проба дає синьо-зелене забарвлення. Аналогічну пробу можна проводити на сухій або мокрій дитячій пелюшці.
