
- •Биокинетика
- •Глава 1. Введение в биокинетику
- •Предмет изучения биокинетики
- •Химическая кинетика как основа биокинетики
- •1.2.1. Современные представления о механизме химической реакции
- •1.2.2. Скорость химической реакции
- •1.2.3. Константа равновесия
- •1.2.4. Выражения для константы скорости элементарной химической реакции
- •1.2.5. Влияние pH на скорость химической реакции
- •1.2.6. Кинетический эксперимент
- •Глава 2. Ферментативный катализ
- •2.1. Кинетические схемы и механизм ферментативной реакции
- •2.1.1. Схема Михаэлиса-Ментен
- •2.1.2. Определение параметров Wm и Km из экспериментальных данных
- •2.1.3. Метод графов при анализе кинетических схем
- •2.1.4. Определение концентрации активных центров
- •2.2. Типичные зависимости начальной стационарной скорости реакции от концентрации субстрата
- •2.2.1. Ингибирование и активация избытком субстрата
- •2.2.2. Аллостерические эффекты
- •2.3. Многосубстратные реакции
- •2.4.2. Релаксационная кинетика
- •2.5. Влияние температуры и pH на скорость ферментативных реакций
- •2.6. Ингибирование ферментативных реакций
- •2.7. Инактивация ферментов
- •2.8. Полиферментные системы. Сопряженные ферментные реакции
- •2.9. Кинетика действия ферментов в открытых системах
- •3.1.1. Химическое строение рецепторов и лигандов
- •3.1.2. Агонисты и антагонисты
- •3.2.3. Строение и функционирование g-белок сопряженных рецепторов
- •3.2.4. Механизмы внутриклеточного проведения и усиления рецепторного сигнала
- •3.2.5. Инактивация рецепторного сигнала
- •3.3.1. Диффузия рецепторов
- •3.3.2. Связываение нескольких молекул лиганда с одним рецептором
- •1) Координаты Хилла.
- •2) Координаты Бьеррума.
- •3.4. Взаимодействие нескольких лигандов с одним рецептором
- •3.5. Учет функции распределения клеток по количеству рецепторов на мембране
- •3.6. Феномен колебаний рецепторного связывания
- •Глава 4. Клеточный рост
- •4.1. Клеточный цикл
- •4.2. Экспоненциальная фаза роста
- •4.2.1. Многосубстратные процессы
- •4.2.2. Ингибирование и активация клеточного роста
- •4.2.3. Влияние pH
- •4.4.1. Выражение для удельной скорости клеточного роста в экспоненциальной фазе
- •4.4.2. Многостадийность клеточного цикла
- •5.1. Пассивный транспорт
- •5.2. Активный ионный транспорт
- •Глава 6. Эндоцитоз
2.8. Полиферментные системы. Сопряженные ферментные реакции
Реакции в полиферментных системах можно рассматривать как последовательные процессы, в которых каждая стадия катализируется своим ферментом, например:
![]() (2.67)
(2.67)
При этом считается, что скорости ферментативных реакций на первой и второй стадии реакции описываются уравнением Михаэлиса. Предполагая, что в системе гомогенно распределены субстраты и ферменты (т.е. нет образования специфических комплексов между ферментами) и градиенты субстратов и продукта по всему объему равны нулю, для схемы (2.67) можно записать следующие дифференциальные уравнения:
 (2.68)
(2.68)
Пренебрегая изменением S1со временем (при избыткеS1), в уравнении (2.68) можно разделить переменные и проинтегрировать:
 (2.69)
(2.69)
 (2.70)
(2.70)
где
![]() (2.71)
(2.71)
Уравнение (2.70) имеет смысл при условии
![]() (2.72)
(2.72)
что приводит к неравенству
 (2.73)
(2.73)
Рассмотрим наиболее важный частный случай, когда максимальная скорость второй стадии существенно превышает скорость первой (V2m>>W1). Тогда выражение (2.70) сводится к следующему
![]() (2.74)
(2.74)
При V2m>>W1,S2/K2m<<1, и в этих условиях справедливо неравенство
![]() (2.75)
(2.75)
С учетом этого неравенства уравнение (2.74) приводит к следующей зависимости
 (2.76)
(2.76)
Соответственно, концентрация продукта
 (2.76)
(2.76)
Кривая продукт-время имеет период индукции
![]() (2.77)
(2.77)
и асимптотически приближается к прямой с тангенсом угла наклона, равным стационарной скорости процесса.
Рассмотрим общий случай
![]() (2.78)
(2.78)
в условиях бимолекулярного режима (Si <<Kim) и малой степени конверсии субстрата в конечный продукт (P<<S1+S2+…+Sn). Этой схеме соответствует следующая система дифференциальных уравнений:
 (2.79)
(2.79)
где
![]() (2.80)
(2.80)
В стационарном состоянии:
![]() (2.81)
(2.81)
и в условиях бимолекулярного режима (Si <<Kim):
![]() (2.82)
(2.82)
![]() (2.83)
(2.83)
Тогда при малой степени конверсии субстрата в конечный продукт (P<<S1+S2+…+Sn):
![]() (2.84)
(2.84)
 (2.85)
(2.85)
 (2.86)
(2.86)
Выражение (2.86) дает теоретический критерий определения лимитирующей стадии: наибольшее (лимитирующее) влияние на общую скорость процесса оказывают ферменты, имеющие наименьший параметр Vim/Kim.
2.9. Кинетика действия ферментов в открытых системах
Под открытыми системамипонимают системы, в которых происходит обмен компонента с окружающей средой. В принципе, такими системами являются все живые организмы. Кроме того, открытые системы часто используются в технологических процессах в промышленности.
Некоторые типы открытых систем:
открытая по субстрату и продуктам;
открытая по ферменту.
Некоторые типы реакторов:
проточный реактор идеального перемешивания;
проточный реактор идеального вытеснения;
мембранный реактор.
2.9.1. Основные принципы описания кинетики каталитических реакцих в открытых по субстрату системах
Рассмотрим некоторый элементарный объем, в котором протекает реакция. Скорость изменения концентрации субстрата описывается дифференциальным уравнением:
![]() (2.87)
(2.87)
Реакционная часть описывается уравнением Михаэлиса:
![]() (2.88)
(2.88)
Обменная часть описывается в общем случае уравнением непрерывности потока компонента:
![]() (2.89)
(2.89)
Поток J равен
![]() (2.90)
(2.90)
где D– коэффициент диффузии, аv– скорость ламинарного потока.
2.9.2. Реактор идеального вытеснения
Рассмотрим одномерный реактор (длинную трубу) идеального вытеснения в пренебрежении диффузией. В стационаре:
![]() (2.91)
(2.91)
тогда
![]() (2.91)
(2.91)
Решение уравнения (2.91):
![]()
2.9.3. Реактор идеального перемешивания
Для реактора идеального перемешивания диффузией также можно пренебречь. В стационаре:
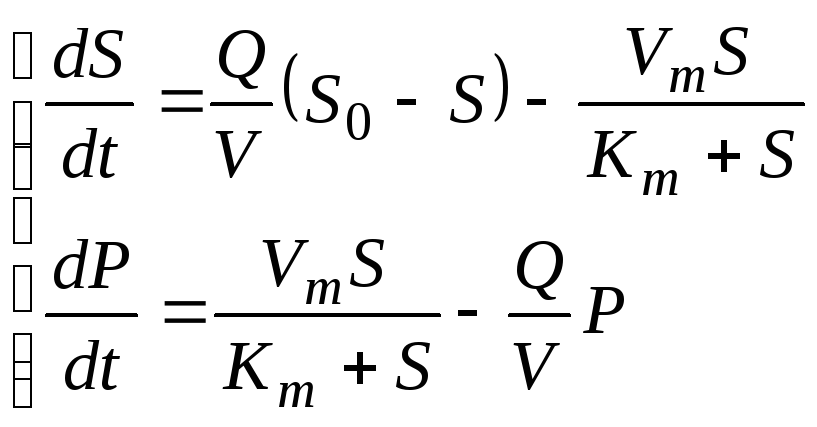 (2.92)
(2.92)
где V– объем реактора,Q– объемный поток в реактор (равный объемному потоку из реактора).
Глава 3. Молекулярная рецепция
3.1. Основные понятия
Рецепторы– особые химические соединения на поверхности или внутри клеток, посредством которых происходит клеточное распознавание веществ (лигандов) и формирование клеточного ответа. Характеристики рецепторов: локализация (на мембране или внутриклеточно), специфичность взаимодействия, трансдукция сигнала (формирование клеточного ответа).
Лиганды– химические вещества, способные реагировать с рецепторами.
Взаимодействие лигандов с рецепторами в простейшем случае представляется следующей схемой:
![]() (3.1)
(3.1)
Изменение концентрации лиганд-рецепторных комплексов, согласно схеме (3.1) описывается дифференциальным уравнением:
![]() (3.2)
(3.2)
Если L >> R:
 (3.3)
(3.3)
Выражение (3.3) называется уравнением сорбции или уравнением (изотермой) Ленгмюра.
Используя (3.3), можно определить концентрацию рецепторов по их аффинности (в равновесии), линеаризуя это уравнение в подходящих координатах:
![]() (3.4)
(3.4)
![]() (уравнение
Скэтчарда) (3.5)
(уравнение
Скэтчарда) (3.5)
Однако, далеко не все зависимости клеточного ответа от концентрации добавленного лиганда удовлетворительно описываются изотермой ленгмюра. Многочисленные исследования в этой области привели к формированию представлений о механизмах внутриклеточного проведения и усиления рецепторного сигнала.
