
- •Сера и ее неорганические соединения
- •1.1.Сера
- •1.2.Полисульфидные анионы
- •1.3. Гидриды серы (сульфаны)
- •1.4. Галогениды серы
- •2. Органические соединения серы
- •2.1. Тиоспирты (меркаптаны, тиолы)
- •2.1.1. Способы синтеза тиолов
- •2.1.2. Физические свойства тиолов
- •2.1.3.Синтезы на основе тиолов
- •2.2. Сульфиды (тиоэфиры)
- •2.3.Сульфоокиси и сульфоны
- •2.4.Сульфокислоты
- •2.5..Сернистые производные угольной кислоты.
- •3. Основные методы извлечения сероорганических
- •3.1. Общая характеристика методов очистки нефтей от сероорганических соединений
- •3.2. Экстракционные методы
- •Метод сернокислотной экстракции.
- •Метод щелочной экстракции.
- •Экстракция органическими растворителями (сольвентная экстракция).
- •3.3. Методы комплексообразования
- •3.4. Методы окисления
- •3.5. Адсорбционно-хроматографические методы
- •Адсорбция на силикагелях.
- •Адсорбция на оксиде алюминия.
- •Адсорбция на цеолитах.
- •Вопросы для самопроверки
- •Список использованной литературы
2.5..Сернистые производные угольной кислоты.
Сероуглерод CS2 – (дисульфид углерода) – аналог угольного ангидрида СО2.
Бесцветная жидкость с приятным запахом, под действием света разлагается, продукты разложения придают сероуглероду желтый цвет и отвратительный запах.
Молекула CS2 линейна. Выше 300 С в инертной атмосфере сероуглерод разлагается на углерод и серу. Сероуглерод крайне огнеопасен и вспыхивает на воздухе уже от прикосновения нагретой стеклянной палочкой.
Сероуглерод – прекрасный растворитель жиров, масел, смол, каучуков, растворяет S, P, J2. Сероуглерод токсичен, поражает нервную и сердечно-сосудистую системы. Его получают прямым взаимодействием угля и серы при высокой температуре (750 –1000С).
В промышленности сероуглерод получают реакцией метана или природного газа с парами серы в присутствии силикагеля при 500 –700 С в камере из хромоникелевой стали.
В присутствии катализаторов сероуглерод хлорируется до четыреххлористого углерода:
![]()
![]()
Сера легко обменивается на кислород при нагревании с оксидами металлов.
С сульфидом натрия сероуглерод образует тритиокарбонат натрия NaCS3 – аналог соды. Со щелочью реагирует подобно диоксиду углерода и образует соль дитиоугольной кислоты:

С алкоголятами металлов сероуглерод образует соли ксантогеновых кислот:
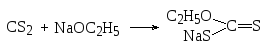
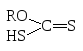
Сами ксантогеновые кислоты неустойчивы и, образуясь, при подкислении их
солей, тотчас разлагается с образованием исходного спирта и сероуглерода.
![]()
Алкилированием солей ксантогеновой кислоты получают полные эфиры дитиоугольной кислоты:
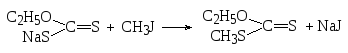
При нагревании эти эфиры гладко разлагаются с образованием олефина и отщеплением меркаптана и сероокиси углерода:

Это реакция носит название реакция Чугаева. Она используется при исследовании спиртов сложной структуры.
3. Основные методы извлечения сероорганических
соединений из нефтей и нефтяных фракций
3.1. Общая характеристика методов очистки нефтей от сероорганических соединений
Разработка новых методов выделения и концентрирования сернистых соединений нефти представляет собой часть исследования их состава, строения и свойств. Поэтому важной проблемой является создание эффективной комплексной схемы определения и выделения сероорганических соединений из нефтей и любых ее фракций, что позволит перейти к детальному их исследованию.
В настоящее время известны разнообразные методы концентрирования и извлечения сероорганических соединений из углеводородного сырья. Разработаны промышленные схемы получения концентратов сульфидов, сульфоксидов и сульфонов из нефтей и нефтяных дистиллятов, которые также сыграли положительную роль в исследовании нефтяных сернистых соединений и позволяют уже сейчас определять реальные пути их квалифицированного использования. В частности, они могут применяться в гидрометаллургии при обогащении руд и экстракции многих металлов, в том числе и благородных, для решения экологических проблем, для лечения животных и повышения
урожайности сельскохозяйственных культур, являются исходным сырьем в различных реакциях органического и нефтехимического синтеза. Масштабное же применение нефтяных сернистых соединений сдерживается ввиду отсутствия промышленно приемлемых способов их извлечения из нефтей и нефтепродуктов. Поэтому возможности их широкого использования обусловливают необходимость разработки простых и перспективных для промышленной реализации способов выделения сульфидов, меркаптанов и тиофенов, а также поиск промышленно приемлемых способов их превращения в би- и полифункциональные производные с еще более интересными свойствами, чем исходные продукты. Наиболее надежные и доступные способы выделения сероорганических соединений – окисление различными окислителями, адсорбция на силикагеле и оксиде алюминия, сернокислотная и щелочная экстракции. В каждом данном способе возможно много вариантов, различающихся природой используемого окислителя, экстрагента, катализатора окисления, растворителя, объемом
технологических выбросов и т. д. Из всех перечисленных методов, по-видимому, более перспективны способы, основанные на экстракционном принципе, которые привлекают простотой технологического воплощения и хорошо отработаны в промышленности. Поэтому не прекращаются работы по подбору различных растворителей для выделения и концентрирования сернистых соединений нефти. Общими недостатками различных растворителей являются низкая селективность и достаточно высокая растворяющая способность в отношении парафинонафтеновых углеводородов. В связи с этим в процессах селективной очистки нефтепродуктов подбираются различные добавки к растворителям (спирты, вода), регулирующие селективность.
