
- •Видавництво Львівської комерційної академії
- •Розділ 1. Матеріалознавство непродовольчих товарів
- •Тема 1. Основні матеріалознавчі поняття. Структура матеріалів План
- •1. Класифікація матеріалів
- •2. Зв’язок властивостей матеріалів з будовою атомів і молекул,
- •Ковалентні зв’язки - утворюються, коли атоми поєднують валентні електрони, добудовуючи свою електронну оболонку.
- •Принципи будови кристалічних та аморфних матеріалів
- •Аморфні структури матеріалів
- •Вивчення макро- , мікро- та молекулярних структур матеріалів
- •Тема 2. Властивості матеріалів План
- •1. Фізичні властивості матеріалів
- •1.1. Структурно-фізичні властивості
- •1.3. Гідрофізичні властивості
- •1.4. Термічні властивості матеріалів
- •1.5. Оптичні властивості
- •1.6. Акустичні властивості
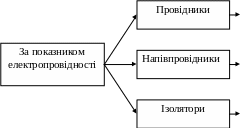
- •1.7. Електричні і магнітні властивості
- •2 . Хімічні властивості
- •Біостійкість - здатність матеріалу чинити опір руйнуванню під впливом бактерій, пліснявих грибів, моху, рослин паразитів, комах.
- •Тема 3. Класифікація, характеристика металів та їхніх сплавів
- •1. Класифікація металів
- •2. Типи сплавів
- •3. Діаграми стану двокомпонентних сплавів (типи діаграм)
- •Типи діаграм
- •4. Діаграма стану сплаву “залізо-вуглець”
- •5. Класифікація і характеристика чавуну та сталі
- •6. Металокераміка
- •Тема 4. Характеристика структури і властивостей деревини План
- •2. Структура деревини
- •2.1. Макроструктура деревини
- •2.2. Мікроструктура деревини
- •3. Класифікація та характеристика основних порід деревини
- •Листяні розсіяно-судинні Ядрові – горіх грецький, червоне дерево, платан, тополя, верба.
- •4.1.4. Термічні властивості
- •4.1.5. Оптичні властивості
- •Дуже сильний блиск у червоного, лимонного і сатинового дерев; підвищений блиск у дуба, бука, клена, платана, ільма.
- •4.1.6. Акустичні властивості
- •4.1.7. Електричні властивості
- •4.2. Хімічні властивості
- •Тема 5. Пластичні маси План
- •1.1. Полімери: класифікація, хімічний склад, структура
- •1.2. Інші компоненти, які можуть входити у склад пластмас
- •2. Класифікація пластмас
- •3.1.5. Оптичні властивості
- •3.1.6. Електричні властивості
- •3.2. Хімічні властивості
- •Тема 6. Скляні матеріали План
- •1. Структура скла
- •2. Сировинні матеріали, що використовуються для
- •Вводять з метою пониження температури варіння скломаси;
- •2.2. Допоміжні матеріали.
- •3. Класифікація та види стекол
- •Кришталеве скло – скло, яке містить в значних кількостях оксид
- •4.1.3. Гідрофізичні властивості
- •4.1.4. Термічні властивості
- •4.1.5. Оптичні властивості
- •4.1.6. Електричні властивості
- •4.2. Хімічні властивості
- •Тема 7. Керамічні матеріали План
- •Сировинні матеріали, що використовуються для виготовлення керамічних виробів
- •Структура кераміки
- •Основні елементи структури:
- •3.1.2. Механічні властивості
- •3.1.3. Гідрофізичні властивості
- •3.1.4. Термічні властивості
- •3.1.5. Оптичні властивості
- •3.2. Хімічні властивості
- •Тема 8. Природні кам’яні матеріали План
- •1. Головні породоутворювальні мінерали
- •Розділ 2. Основи технології виробництва товарів народного споживання
- •Тема 1. Технологія виготовлення виробів з металів та їх
- •1. Способи виготовлення металевих виробів
- •2. Термічна обробка деталей та заготовок з вуглецевих сталей
- •3. Хіміко – термічна обробка
- •Ціанування Поверхневе насичення сталевих виробів одночасно
- •Поверхневе насичення бором для підвищення
- •4. Обробка поверхні металевих виробів, з’єднання деталей та
- •Крацовання Обробка поверхні металевими щітками з сталевого
- •Галтовання Обробка виробів в барабанах, які обертаються. В
- •Тема 2.Технологія виготовлення виробів з пластичних мас
- •Тема 3. Технологія виготовлення виробів зі скла План
- •1. Підготування сировинних матеріалів
- •2. Варіння скломаси
- •3. Способи формування скляних виробів
- •4. Способи формування листового скла
- •Тема 4. Технологія виготовлення виробів з кераміки План
- •1. Підготування сировинних матеріалів
- •2. Формування виробів
- •Технологія проведення відпалів
- •Література
- •Додаткова література
Укоопспілка
Львівська комерційна академія
Матеріалознавство і основи технології виробництва
товарів народного споживання
Опорний конспект лекцій
для студентів спеціальностей 6.050301; 6.050302; 6.050303
Львів
Видавництво Львівської комерційної академії
2005
Укладачі: Полікарпов І.С.,
Уська А.М.,
Шумський О.В.,
Кирильчук Р.В.
Рецензенти: доц. Беднарчук М.С.,
доц. Пелик Л.В.
Відплвідальний за випуск: проф.Полікарпов І.С.
Опорний конспект лекцій рекомендований до друку Вченою радою ТКФ №9 від 29 червня 2005 р.
Полікарпов І.С.,
Уська А.М.,
Шумський О.В.,
Кирильчук Р.В.
2005
Розділ 1. Матеріалознавство непродовольчих товарів
Тема 1. Основні матеріалознавчі поняття. Структура матеріалів План
Основні матеріалознавчі терміни. Класифікація матеріалів.
Зв’язок властивостей матеріалів з будовою атомів і молекул, з міжатомними і міжмолекулярними зв’язками.
Принципи будови кристалічних та аморфних матеріалів.
Вивчення макро -, мікро - та молекулярних структур матеріалів.

Література: 4, 5, 8.
1. Класифікація матеріалів

За будовою
Кристалічні
Аморфні



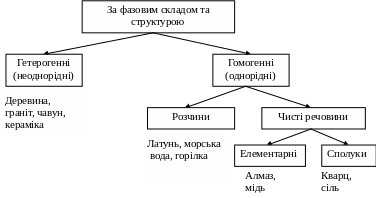
Метали, мінерали
Пластмаси, скляні матеріали
Срібло, мідь, алюміній,
сталь
Si, Se, C, оксиди, сульфіди
Гума, скло, кераміка, пластмаса
2. Зв’язок властивостей матеріалів з будовою атомів і молекул,
з міжатомними і міжмолекулярними зв’язками
 Будова
атомів
Будова
атомів
Індивідуальні властивості атомів залежать від:
маси і заряду ядра;
загальної кількості електронів;
кількості валентних електронів;
наявності вільних енергетичних рівнів і підрівнів.
І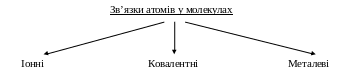 онні
зв’язки - утворюються
між аніонами і катіонами під впливом
кулонівських
онні
зв’язки - утворюються
між аніонами і катіонами під впливом
кулонівських
сил.
Об’єднання іоннів у твердій речовині відбувається за принципом
максимально щільної упаковки твердих куль у просторі.
Ковалентні зв’язки - утворюються, коли атоми поєднують валентні електрони, добудовуючи свою електронну оболонку.
Структури з ковалентними зв’язками мають сталий кут зв’язків,
чого не могло бути в іонних структурах.
Металеві зв’язки - в атомах металів валентні електрони мають здатність
“вільно” переходити в межах структури. Тому метали і мають
високі електро- й теплопровідність, блиск.
Металічні структури утворюються за принципом щільної
упаковки твердих куль.
Міжмолекулярні (вандерваальсові) зв’язки - існують між нейтральними
молекулами. Дія їх слабка, тому молекулярні з’єднання мають, як
правило, низьку температуру плавлення.
