
- •Лекций по курсу «методы получения биологически активных соединений» Электронный вариант на основе учебника: в.С. Мокрушин, г.А. Вавилов
- •Предисловие
- •Введение
- •Глава 1
- •Классификация лекарственных средств
- •Действие лекарственных средств на метаболизм живых организмов
- •1.2. Методы поиска новых препаратов
- •1.2.1. Основные этапы создания лекарственных препаратов, подходы к получению и отбору лекарственных средств
- •1.2.2. Разработка плана синтеза
- •1.3. Сырьевая база химико-фармацевтической промышленности
- •1.3.1. Продукты переработки твердого топлива и коксохимического производства
- •1.3.2. Продукты нефтеоргсинтеза
- •1.3.3. Лесохимическое сырье
- •1.3.4. Некоторые продукты многотоннажных производств
- •1.4. Теоретические аспекты выбора метода синтеза
- •1.4.1. Энергетические факторы
- •1.4.2. Классификация реакций
- •1.4.3. Механизм и кинетика реакций
- •1.4.4. Уравнения Гаммета, Тафта
- •1.4.5. Квантово-химические расчеты
- •1.4.6. Выбор растворителя
- •Характеристики растворителей
- •1.5. Разработка технологической схемы производства
- •1.5.1. Категории и типы технологических схем
- •1.5.2. Правила составления и основные требования к технологическим схемам
- •1.5.3. Оформление чертежей технологических схем
- •1.5.4. Типовое оснащение и привязка химического реактора к конкретному производству
- •Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
- •2.1. Реакции электрофильного замещения
- •2.1.1. Нитрование
- •2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
- •2.1.1.2. Химические особенности реакций нитрования, реагенты, механизм
- •2.1.1.3. Нитрование арил и гетариламинов
- •2.1.1.4. Нитрование азотной кислотой
- •2.1.1.5. Технологические аспекты нитрования
- •2.1.1.6. Использование реакции нитрования для получения полупродуктов и лекарственных средств
- •2.1.1.7. Получение нитроэфиров и n-нитросоединений Так же как и при нитровании ароматических соединений, при получении нитроэфиров используют смесь азотной и серной кислот:
- •2.1.2. Нитрозирование
- •2.1.2.1. Механизм нитрозирования, реагенты
- •2.1.2.2. Особенности проведения реакции
- •2.1.2.3. Особенности структуры и свойств нитрозосоединений
- •2.1.2.4. Практика проведения реакции нитрозирования
- •2.1.2.5. Техника безопасности, экология
- •2.1.3. Сульфирование
- •2.1.3.2. Реагенты, использующиеся при проведении реакции сульфирования, механизм реакции
- •2.1.3.3. Особенности сульфирования, побочные реакции
- •2.1.3.4. Влияние температуры
- •2.1.3.5. Сульфирование бензола и его производных
- •2.1.3.6. Сульфирование анилина и его производных
- •2.1.3.8. Сульфирование хлорсульфоновой кислотой
- •2.1.3.9. Техника безопасности, экология
- •2.1.4. Сульфохлорирование
- •2.1.4.1. Химические особенности реакции
- •2.1.4.2. Технологические аспекты сульфохлорирования
- •2.1.4.3. Синтез сульфаниламидных препаратов
- •2.1.4.4. Техника безопасности, экология
- •2.1.5. Введение углеродных остатков в Ароматическое и гетероциклическое ядро
- •2.1.5.1. Реакции с-алкилирования
- •Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
- •Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
- •2.1.5.2. Реакции гидроксиалкилирования
- •2.1.5.3. Реакции хлоралкилирования
- •2.1.5.4. Реакции аминоалкилирования
- •2.1.5.5. Реакции с-ацилирования
- •2.1.5.6. Реакции с-формилирования
- •2.1.5.7. Реакция карбоксилирования
- •2.1.5.8. Карбоксилирование алифатических соединений
- •2.1.5.9. Техника безопасности, экология
- •2.1.6. Галогенирование
- •2.1.6.1. Препараты, содержащие в молекуле атомы галогенов
- •2.1.6.2. Реагенты, механизм реакций галогенирования
- •2.1.6.3. Хлорирование ароматических соединений
- •2.1.6.4. Бромирование, иодирование
- •2.1.6.5. Технологические аспекты галогенирования
- •2.1.6.7. Галогенирование альдегидов, кетонов и кислот
- •2.1.6.8. Свободнорадикальное галогенирование
- •Энергия стадий процесса
- •2.1.6.10. Получение галогенамидов
- •2.1.6.11. Окислительное хлорирование
- •2.1.6.12. Меры предосторожности при проведении реакций галогенирования
- •2.1.6.13. Экология
- •2.2. Реакции нуклеофильного замещения
- •Реакции нуклеофильного замещения у насыщенного атома углерода
- •2.2.1.1. Типы реакций
- •Реагенты для проведения реакций алкилирования
- •Механизмы реакций
- •Алкилирование аминов
- •Селективные методы синтеза первичных аминов
- •Селективные методы синтеза вторичных аминов
- •Алкилирование спиртов и фенолов
- •Алкилирование сн кислот
- •Алкилирование гетероциклических соединений
- •Техника безопасности, экология
- •2.2.2. Реакции нуклеофилов с соединениями,
- •2.2.2.1. Обзор реакций, их кинетика и механизм
- •2.2.2.2. Реакции ацилирования
- •2.2.2.3. Реакции нитрилов с нуклеофилами
- •2.2.2.4. Реакции этерификации, получение амидов и гидразидов кислот
- •2.2.2.5. Получение азометинов и гидразонов
- •2.2.2.6. Методы получения первичных аминов с помощью перегруппировок
- •2.2.2.7. Использование реакций в основном органическом синтезе
- •2.2.2.8. Технология, техника безопасности, экология
- •2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
- •2.2.3.1. Нуклеофильное замещение по типу sn1
- •2.2.3.2. Ариновое замещение
- •2.2.3.3. Реакции нуклеофилов с ипсо-замещением нуклеофугных групп
- •Получение полупродуктов и лекарственных препаратов. В отсутствие электроноакцепторных заместителей замещение атома хлора происходит при высокой температуре и в присутствии катализатора:
- •2.2.3.4. Нуклеофильное замещение водорода
- •Еще в начале хх в. Было найдено, что реакция хинолина (изохинолина, фенантридина) с хлорангидридами кислот и цианидом натрия дает устойчивые соединения Райсерта (реакция Райсерта):
- •2.2.3.5. Замещение гидроксигрупп
- •2.2.3.6. Замещение по механизму anrorc
- •2.2.3.7. Технологические аспекты проведения реакций, техника безопасности, экология
2.1.5.1. Реакции с-алкилирования
Еще в конце XIX в. были разработаны методы введения алкильных остатков в ароматическое ядро. К ним относятся: реакция Фриделя-Крафтса и ее модификации – взаимодействие ароматических соединений с алкилгалогенидами в присутствии кислот Льюиса, реакция алкилирования олефинами и спиртами в присутствии кислых катализаторов.
Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
R-Hal, R-CH=CH2, (R)3C-OH
Реакционная способность алкилгалогенидов уменьшается в следующем ряду:
RF> RCl > RBr > RI
Обычно не используют алкилиодиды, т. к. они дороги и малореакционноспособны. При наличии в молекуле алкилгалогенида двух различных атомов галогена замещается наиболее активный. Так, например, при алкилировании бензола 1-фтор-3-хлорпропаном с использованием BF3 в качестве катализатора образуется в основном 3-хлорпропилбензол. Независимо от метода генерирования карбокатионов их активность увеличивается от первичных к вторичным и третичным алкилам. Наибольшей реакционной способностью обладают бензильные производные. Без катализатора реакция, за редким исключением, не идет. Каталитическая активность кислот Льюиса уменьшается в следующем ряду:
AlBr3 > AlCl3 > GaBr3 > GaCl3 > FeCl3 > BF3 > ZnCl2 > SbCl5
При алкилировании олефинами используют кислотные катализаторы. Их активность уменьшается в ряду:
HF > H2SO4 > HCl > P2O5 > H3PO4
Наряду с гомогенными катализаторами в настоящее время используют и гетерогенные. Их применение дает существенные преимущества: они легко отделяются от реакционной массы и могут быть использованы многократно. В качестве таких катализаторов нашли применение сульфированный сополимер стирола и дивинилбензола (смола КУ-2), фосфорная кислота на твердом носителе (глина, силикагель), цеолиты (алюмосиликаты со строго регулярной структурой).
Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
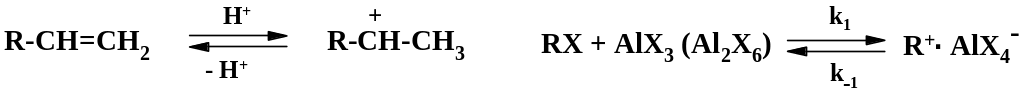
Механизм реакций алкилирования является типичным для процессов электрофильного замещения (в схеме образование -комплексов опущено):
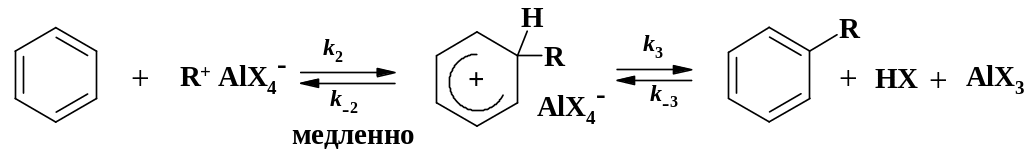
Лимитирующей стадией процесса является образование -аддукта. Это подтверждается тем, что отсутствует кинетический изотопный эффект, соотношение kН/kD близко к единице. Реакция обратима, кинетическое уравнение можно представить в следующем виде:
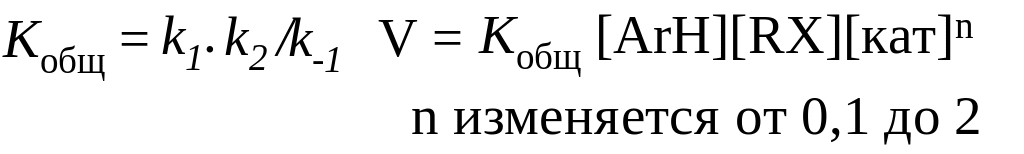
Катализатор, в зависимости от условий, может быть и реагентом. Его концентрация колеблется от 0,1 до 2 молей.
В отличие от нитрования и сульфирования, реакции С-алкилирования имеют особенности, связанные со структурой карбокатиона и электронодонорными свойствами алкильных групп.
Особенности реакции:
1. Следует обратить внимание на возможность изомеризации карбокатиона, т. к. вторичные катионы более стабильны.
![]()
Соотношение продуктов алкилирования н- к изо- зависит от реакционной способности арена. Это хорошо видно при сравнении алкилирования бензола и толуола:
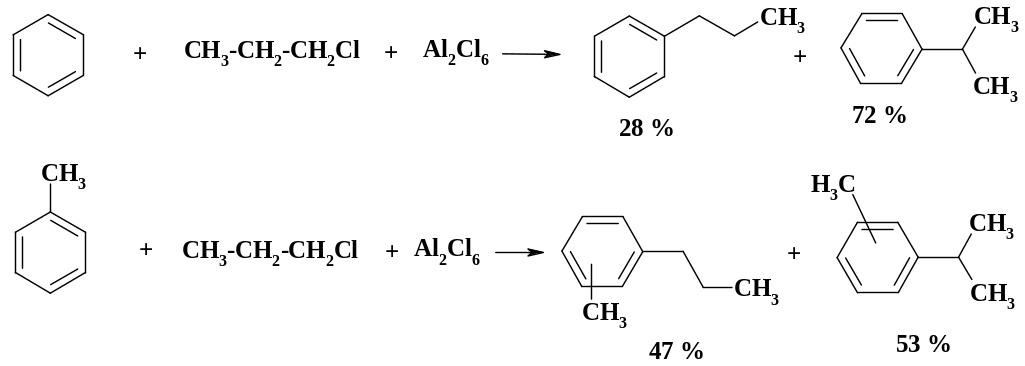
Низкая реакционная способность арена ведет к высокому содержанию вторичных арилалкилов, высокая реакционная способность ArH обусловливает в основном образование продуктов нормального строения.
2. Как уже отмечалось, реакция обратима. Это приводит к изомеризации продукта реакции за счет отщепления алкильной группы и повторному алкилированию. Кроме того, в -аддукте может происходить и 1,2-сдвиг. Так при обработке о-ксилола хлоридом алюминия и сухим хлористым водородом образуется сложная смесь продуктов:
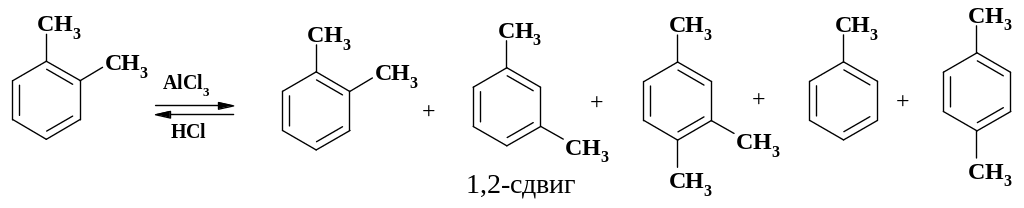
3. Анализ данных кинетических исследований по уравнению Гаммета показывает, что константа реакционной серии = -2 … -5. Однако, в отличие от нитрования, +Alk < 0. Это значит, что образующийся продукт легче вступает в реакцию, чем исходный. Всегда образуется смесь продуктов.
Итак, С-алкилирование – реакция с очень низкой региоселективностью, и ее применение в ХФП ограниченно. Но в основном органическом синтезе реакции С-алкилирования широко используются.
Алкилирование углеводородов, технология. Наиболее крупнотоннажными продуктами являются: этилбензол (около 20 млн т) – сырье для производства стирола; кумол (около 5 млн т) – сырье для получения фенола и ацетона; высшие алкилбензолы (производство более 2 млн. тонн) – используют при получение алкиларилсульфонатов (см. раздел 2.1.3).
Рассмотрим подробнее получение этилбензола. В связи с большой мощностью производства рентабельно осуществлять получение этилбензола непрерывным способом. Используют тщательно осушенный бензол и этилен высокой чистоты. В большинстве производств пока в качестве катализатора применяют хлорид алюминия. Катализаторный комплекс готовят в отдельном аппарате смешением AlCl3, полиэтилбензолов, бензола с добавкой хлористого этила, который при реакции с бензолом дает необходимое количество HCl для активации катализатора. Процесс представлен на схеме:
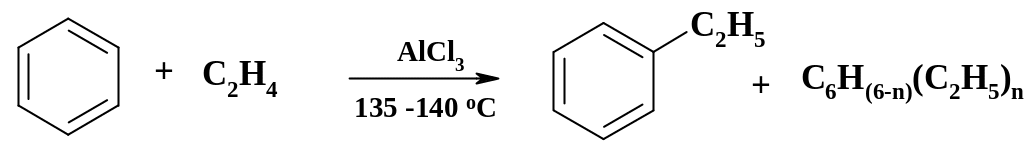
Количество бензола должно быть намного больше, чем этилена. Обычное соотношение этих реагентов в молях 3 : 1, благодаря чему количество продуктов ди-, три- и тетраалкилирования снижается. Для утилизации малоиспользуемых этилбензолов (n = 2 – 4) их направляют в реакцию в качестве реагентов для переэтилирования. Суммарное уравнение этого процесса для диэтилбензолов:
C6H6 + C6H4(Et)2 → 2 C6H5Et
В качестве примера можно рассмотреть параметры материального потока в одном из производств. Загрузка:
C6H6 – 54657 кг/ч (700 моль/ч); С2H4 – 6540 кг/ч (233 моль/ч);
С6H4(Et)n – 4828 кг/ч, n = 2 – 4; AlCl3 – 190 кг/ч
Состав алкилата представлен в табл. 2.8:
Таблица 2.8
Алкилат |
кг/ч |
% |
Алкилат |
кг/ч |
% |
PhH |
36 823 |
67,6 |
Ph(Et)3 |
1 387 |
1,2 |
PhEt |
19 312 |
24,7 |
Ph(Et)4 |
294 |
0,2 |
Ph(Et)2 |
5 978 |
6,1 |
AlCl3 |
190 |
0,2 |
Процесс ведут в стальной футерованной кислотостойкой плиткой колонне. Через штуцеры в днище колонны подается этилен и бензол, а также катализаторный комплекс. Тепло, выделяющееся в результате реакции, отводится за счет испарения бензола. Пары бензола и этилбензолов конденсируют и направляют на ректификацию. Жидкий алкилат непрерывно уходит из бокового штуцера и далее на отстаивание, где отделяется катализаторный комплекс, который вновь направляют в реакцию. Верхний слой промывают водой и передают на ректификацию. Фракцию, содержащую диэтилбензолы, частично возвращают в это производство. Часть направляют на получение дивинилбензола. Лучшие результаты получены при использовании BF3, степень конверсии 32,8 %.
Экономически более эффективным методом является парофазное алкилирование на цеолитах при температуре 400 оС. При получении кумола в качестве катализатора используют серную кислоту либо смолу КУ-2.
В ХФП ограниченно применяют стабилизатор окисления ионол. Его получают алкилированием фенола бутиленом, либо трет-бутиловым спиртом. В данном случае из-за большого объема третбутильного остатка реакция региоселективна.
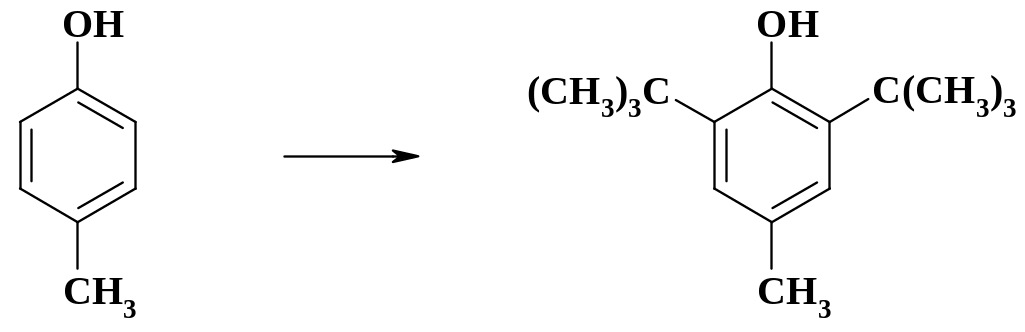
Одним из методов синтеза бензофенона, из которого получают бензгидрол – сырье для производства димедрола (дибензгидрамина), является взаимодействие бензола с хлористым метиленом или четыреххлористым углеродом:
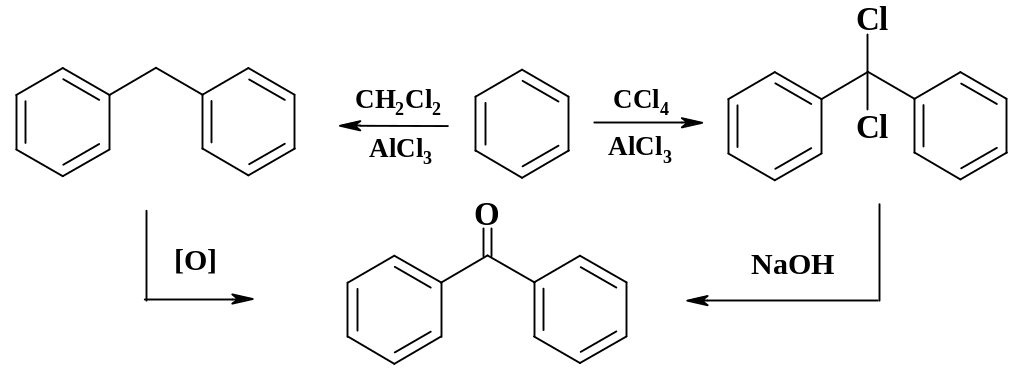
Бензофенон получают окислением дифенилметана или щелочным гидролизом дифенилдихлометана (см. разделы 2.3.1 и 2.6). Действие димедрола и его синтез приведены в разделах 1.1 и 2.2.1.
