
- •Лекций по курсу «методы получения биологически активных соединений» Электронный вариант на основе учебника: в.С. Мокрушин, г.А. Вавилов
- •Предисловие
- •Введение
- •Глава 1
- •Классификация лекарственных средств
- •Действие лекарственных средств на метаболизм живых организмов
- •1.2. Методы поиска новых препаратов
- •1.2.1. Основные этапы создания лекарственных препаратов, подходы к получению и отбору лекарственных средств
- •1.2.2. Разработка плана синтеза
- •1.3. Сырьевая база химико-фармацевтической промышленности
- •1.3.1. Продукты переработки твердого топлива и коксохимического производства
- •1.3.2. Продукты нефтеоргсинтеза
- •1.3.3. Лесохимическое сырье
- •1.3.4. Некоторые продукты многотоннажных производств
- •1.4. Теоретические аспекты выбора метода синтеза
- •1.4.1. Энергетические факторы
- •1.4.2. Классификация реакций
- •1.4.3. Механизм и кинетика реакций
- •1.4.4. Уравнения Гаммета, Тафта
- •1.4.5. Квантово-химические расчеты
- •1.4.6. Выбор растворителя
- •Характеристики растворителей
- •1.5. Разработка технологической схемы производства
- •1.5.1. Категории и типы технологических схем
- •1.5.2. Правила составления и основные требования к технологическим схемам
- •1.5.3. Оформление чертежей технологических схем
- •1.5.4. Типовое оснащение и привязка химического реактора к конкретному производству
- •Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
- •2.1. Реакции электрофильного замещения
- •2.1.1. Нитрование
- •2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
- •2.1.1.2. Химические особенности реакций нитрования, реагенты, механизм
- •2.1.1.3. Нитрование арил и гетариламинов
- •2.1.1.4. Нитрование азотной кислотой
- •2.1.1.5. Технологические аспекты нитрования
- •2.1.1.6. Использование реакции нитрования для получения полупродуктов и лекарственных средств
- •2.1.1.7. Получение нитроэфиров и n-нитросоединений Так же как и при нитровании ароматических соединений, при получении нитроэфиров используют смесь азотной и серной кислот:
- •2.1.2. Нитрозирование
- •2.1.2.1. Механизм нитрозирования, реагенты
- •2.1.2.2. Особенности проведения реакции
- •2.1.2.3. Особенности структуры и свойств нитрозосоединений
- •2.1.2.4. Практика проведения реакции нитрозирования
- •2.1.2.5. Техника безопасности, экология
- •2.1.3. Сульфирование
- •2.1.3.2. Реагенты, использующиеся при проведении реакции сульфирования, механизм реакции
- •2.1.3.3. Особенности сульфирования, побочные реакции
- •2.1.3.4. Влияние температуры
- •2.1.3.5. Сульфирование бензола и его производных
- •2.1.3.6. Сульфирование анилина и его производных
- •2.1.3.8. Сульфирование хлорсульфоновой кислотой
- •2.1.3.9. Техника безопасности, экология
- •2.1.4. Сульфохлорирование
- •2.1.4.1. Химические особенности реакции
- •2.1.4.2. Технологические аспекты сульфохлорирования
- •2.1.4.3. Синтез сульфаниламидных препаратов
- •2.1.4.4. Техника безопасности, экология
- •2.1.5. Введение углеродных остатков в Ароматическое и гетероциклическое ядро
- •2.1.5.1. Реакции с-алкилирования
- •Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
- •Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
- •2.1.5.2. Реакции гидроксиалкилирования
- •2.1.5.3. Реакции хлоралкилирования
- •2.1.5.4. Реакции аминоалкилирования
- •2.1.5.5. Реакции с-ацилирования
- •2.1.5.6. Реакции с-формилирования
- •2.1.5.7. Реакция карбоксилирования
- •2.1.5.8. Карбоксилирование алифатических соединений
- •2.1.5.9. Техника безопасности, экология
- •2.1.6. Галогенирование
- •2.1.6.1. Препараты, содержащие в молекуле атомы галогенов
- •2.1.6.2. Реагенты, механизм реакций галогенирования
- •2.1.6.3. Хлорирование ароматических соединений
- •2.1.6.4. Бромирование, иодирование
- •2.1.6.5. Технологические аспекты галогенирования
- •2.1.6.7. Галогенирование альдегидов, кетонов и кислот
- •2.1.6.8. Свободнорадикальное галогенирование
- •Энергия стадий процесса
- •2.1.6.10. Получение галогенамидов
- •2.1.6.11. Окислительное хлорирование
- •2.1.6.12. Меры предосторожности при проведении реакций галогенирования
- •2.1.6.13. Экология
- •2.2. Реакции нуклеофильного замещения
- •Реакции нуклеофильного замещения у насыщенного атома углерода
- •2.2.1.1. Типы реакций
- •Реагенты для проведения реакций алкилирования
- •Механизмы реакций
- •Алкилирование аминов
- •Селективные методы синтеза первичных аминов
- •Селективные методы синтеза вторичных аминов
- •Алкилирование спиртов и фенолов
- •Алкилирование сн кислот
- •Алкилирование гетероциклических соединений
- •Техника безопасности, экология
- •2.2.2. Реакции нуклеофилов с соединениями,
- •2.2.2.1. Обзор реакций, их кинетика и механизм
- •2.2.2.2. Реакции ацилирования
- •2.2.2.3. Реакции нитрилов с нуклеофилами
- •2.2.2.4. Реакции этерификации, получение амидов и гидразидов кислот
- •2.2.2.5. Получение азометинов и гидразонов
- •2.2.2.6. Методы получения первичных аминов с помощью перегруппировок
- •2.2.2.7. Использование реакций в основном органическом синтезе
- •2.2.2.8. Технология, техника безопасности, экология
- •2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
- •2.2.3.1. Нуклеофильное замещение по типу sn1
- •2.2.3.2. Ариновое замещение
- •2.2.3.3. Реакции нуклеофилов с ипсо-замещением нуклеофугных групп
- •Получение полупродуктов и лекарственных препаратов. В отсутствие электроноакцепторных заместителей замещение атома хлора происходит при высокой температуре и в присутствии катализатора:
- •2.2.3.4. Нуклеофильное замещение водорода
- •Еще в начале хх в. Было найдено, что реакция хинолина (изохинолина, фенантридина) с хлорангидридами кислот и цианидом натрия дает устойчивые соединения Райсерта (реакция Райсерта):
- •2.2.3.5. Замещение гидроксигрупп
- •2.2.3.6. Замещение по механизму anrorc
- •2.2.3.7. Технологические аспекты проведения реакций, техника безопасности, экология
2.2.2.7. Использование реакций в основном органическом синтезе
Применение рассматриваемых в данном разделе реакций очень обширно, поэтому приведены лишь некоторые примеры без описания технологии и условий проведения процесса. Производство мыла (натриевые соли жирных кислот) из жиров является многотоннажным и осуществляется за счет реакции гидролиза (омыления) технических сортов жира:
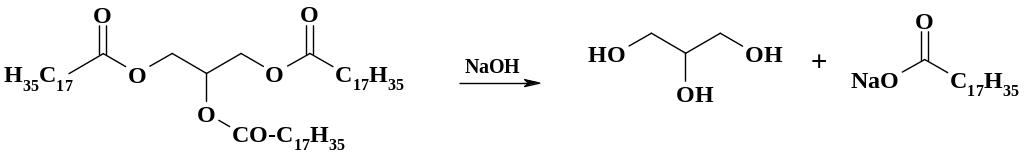
При получении лавсана используют реакцию этерификации терефталевой кислоты этиленгликолем, образующуюся в процессе воду отгоняют вместе с этиленгликолем, который берут в большом избытке:
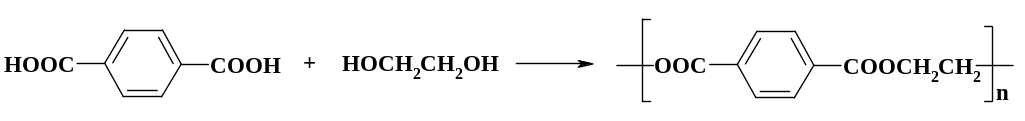
Присоединение синильной кислоты к карбонильной группе используют в производстве метилметакрилата – мономера в синтезе полиметилметакрилата (оргстекла). При взаимодействии ацетона с циановодородом образуется ацетонциангидрин, последующая дегидратация и превращение нитрильной группы в сложноэфирную приводит к получению целевого продукта:
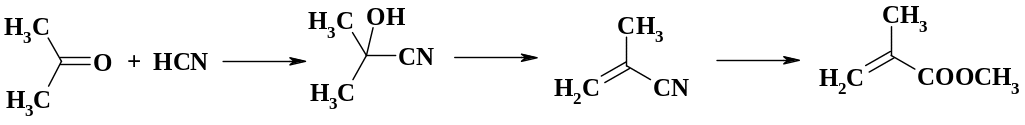

В производстве акриламида из акрилонитрила нитрильную группу превращают в амидную в присутствии кислотного катализатора. Выход составляет около 60 %. Проведение процесса биотехнологическим способом (специальный вид бактерий) позволило повысить выход практически до количественного.
Реакции ацилирования применяют при получении триацетата целлюлозы и многих других продуктов.
Гидратацией олефинов получают спирты. Так синтезируют этанол из этилена.
![]()
Катализатором служит фосфорная кислота, одновременно образуются диэтиловый эфир, ацетальдегид и низкомолекулярный полиэтилен. Примеси отделяют ректификацией. Качество спирта ниже, чем получаемого брожением углеводов. Из-за высокого давления и температуры технологическая схема этого простого химического процесса весьма сложна.
2.2.2.8. Технология, техника безопасности, экология
При синтезе лекарственных средств используют периодические процессы и обычную емкостную аппаратуру. В случае проведения синтеза с хлорангидридами аппаратура должна быть эмалированная. Выбор типа мешалки диктуется конкретными условиями.
При работе с хлорангидридами кислот следует исключить их разлив. При попадании их на кожу проводят обработку раствором соды. Работа с фосгеном требует особых предосторожностей. В помещении должны быть установлены автоматические датчики, сигнализирующие о превышении ПДК фосгена в воздухе. Одновременно должна включаться аварийная вентиляция. Как правило, выход продуктов реакции высок, отходов немного. Растворители подлежат регенерации.
2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
Значение реакций для органического синтеза и получения лекарственных средств. Виды реакций по механизму: типа SN1, ариновое замещение, присоединение–отщепление – SNAr, нуклеофильное замещение водорода (SNH), ANRORC. Кинетика, закономерности. Использование реакций нуклеофильного замещения в органическом синтезе и при получении хинозола, парацетамола, мефенаминовой кислоты, сульфаниламидных препаратов. Нуклеофильное замещение водорода в синтезе диазепиновых транквилизаторов. Реакция Бухерера, синтез препарата митоксантрон.
В промышленном органическом синтезе широко используются реакции нуклеофильного замещения при получении нитрофенолов и нитроанилинов (см. раздел 2.1.1), в медицинской промышленности – в синтезе препаратов хинозол, парацетамол, мефенаминовая кислота, сульфаниламиды и многих других. Биологическое действие ряда лекарственных средств уже было рассмотрено в предыдущих разделах, а для некоторых приведено в данном разделе при описании их синтеза.
Реакции нуклеофильного замещения могут протекать по различным механизмам:
типа SN1;
аринный;
присоединение-отщепление (SNAr);
нуклеофильное замещение водорода (SNH);
ANRORC.
