
- •Лекций по курсу «методы получения биологически активных соединений» Электронный вариант на основе учебника: в.С. Мокрушин, г.А. Вавилов
- •Предисловие
- •Введение
- •Глава 1
- •Классификация лекарственных средств
- •Действие лекарственных средств на метаболизм живых организмов
- •1.2. Методы поиска новых препаратов
- •1.2.1. Основные этапы создания лекарственных препаратов, подходы к получению и отбору лекарственных средств
- •1.2.2. Разработка плана синтеза
- •1.3. Сырьевая база химико-фармацевтической промышленности
- •1.3.1. Продукты переработки твердого топлива и коксохимического производства
- •1.3.2. Продукты нефтеоргсинтеза
- •1.3.3. Лесохимическое сырье
- •1.3.4. Некоторые продукты многотоннажных производств
- •1.4. Теоретические аспекты выбора метода синтеза
- •1.4.1. Энергетические факторы
- •1.4.2. Классификация реакций
- •1.4.3. Механизм и кинетика реакций
- •1.4.4. Уравнения Гаммета, Тафта
- •1.4.5. Квантово-химические расчеты
- •1.4.6. Выбор растворителя
- •Характеристики растворителей
- •1.5. Разработка технологической схемы производства
- •1.5.1. Категории и типы технологических схем
- •1.5.2. Правила составления и основные требования к технологическим схемам
- •1.5.3. Оформление чертежей технологических схем
- •1.5.4. Типовое оснащение и привязка химического реактора к конкретному производству
- •Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
- •2.1. Реакции электрофильного замещения
- •2.1.1. Нитрование
- •2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
- •2.1.1.2. Химические особенности реакций нитрования, реагенты, механизм
- •2.1.1.3. Нитрование арил и гетариламинов
- •2.1.1.4. Нитрование азотной кислотой
- •2.1.1.5. Технологические аспекты нитрования
- •2.1.1.6. Использование реакции нитрования для получения полупродуктов и лекарственных средств
- •2.1.1.7. Получение нитроэфиров и n-нитросоединений Так же как и при нитровании ароматических соединений, при получении нитроэфиров используют смесь азотной и серной кислот:
- •2.1.2. Нитрозирование
- •2.1.2.1. Механизм нитрозирования, реагенты
- •2.1.2.2. Особенности проведения реакции
- •2.1.2.3. Особенности структуры и свойств нитрозосоединений
- •2.1.2.4. Практика проведения реакции нитрозирования
- •2.1.2.5. Техника безопасности, экология
- •2.1.3. Сульфирование
- •2.1.3.2. Реагенты, использующиеся при проведении реакции сульфирования, механизм реакции
- •2.1.3.3. Особенности сульфирования, побочные реакции
- •2.1.3.4. Влияние температуры
- •2.1.3.5. Сульфирование бензола и его производных
- •2.1.3.6. Сульфирование анилина и его производных
- •2.1.3.8. Сульфирование хлорсульфоновой кислотой
- •2.1.3.9. Техника безопасности, экология
- •2.1.4. Сульфохлорирование
- •2.1.4.1. Химические особенности реакции
- •2.1.4.2. Технологические аспекты сульфохлорирования
- •2.1.4.3. Синтез сульфаниламидных препаратов
- •2.1.4.4. Техника безопасности, экология
- •2.1.5. Введение углеродных остатков в Ароматическое и гетероциклическое ядро
- •2.1.5.1. Реакции с-алкилирования
- •Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
- •Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
- •2.1.5.2. Реакции гидроксиалкилирования
- •2.1.5.3. Реакции хлоралкилирования
- •2.1.5.4. Реакции аминоалкилирования
- •2.1.5.5. Реакции с-ацилирования
- •2.1.5.6. Реакции с-формилирования
- •2.1.5.7. Реакция карбоксилирования
- •2.1.5.8. Карбоксилирование алифатических соединений
- •2.1.5.9. Техника безопасности, экология
- •2.1.6. Галогенирование
- •2.1.6.1. Препараты, содержащие в молекуле атомы галогенов
- •2.1.6.2. Реагенты, механизм реакций галогенирования
- •2.1.6.3. Хлорирование ароматических соединений
- •2.1.6.4. Бромирование, иодирование
- •2.1.6.5. Технологические аспекты галогенирования
- •2.1.6.7. Галогенирование альдегидов, кетонов и кислот
- •2.1.6.8. Свободнорадикальное галогенирование
- •Энергия стадий процесса
- •2.1.6.10. Получение галогенамидов
- •2.1.6.11. Окислительное хлорирование
- •2.1.6.12. Меры предосторожности при проведении реакций галогенирования
- •2.1.6.13. Экология
- •2.2. Реакции нуклеофильного замещения
- •Реакции нуклеофильного замещения у насыщенного атома углерода
- •2.2.1.1. Типы реакций
- •Реагенты для проведения реакций алкилирования
- •Механизмы реакций
- •Алкилирование аминов
- •Селективные методы синтеза первичных аминов
- •Селективные методы синтеза вторичных аминов
- •Алкилирование спиртов и фенолов
- •Алкилирование сн кислот
- •Алкилирование гетероциклических соединений
- •Техника безопасности, экология
- •2.2.2. Реакции нуклеофилов с соединениями,
- •2.2.2.1. Обзор реакций, их кинетика и механизм
- •2.2.2.2. Реакции ацилирования
- •2.2.2.3. Реакции нитрилов с нуклеофилами
- •2.2.2.4. Реакции этерификации, получение амидов и гидразидов кислот
- •2.2.2.5. Получение азометинов и гидразонов
- •2.2.2.6. Методы получения первичных аминов с помощью перегруппировок
- •2.2.2.7. Использование реакций в основном органическом синтезе
- •2.2.2.8. Технология, техника безопасности, экология
- •2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
- •2.2.3.1. Нуклеофильное замещение по типу sn1
- •2.2.3.2. Ариновое замещение
- •2.2.3.3. Реакции нуклеофилов с ипсо-замещением нуклеофугных групп
- •Получение полупродуктов и лекарственных препаратов. В отсутствие электроноакцепторных заместителей замещение атома хлора происходит при высокой температуре и в присутствии катализатора:
- •2.2.3.4. Нуклеофильное замещение водорода
- •Еще в начале хх в. Было найдено, что реакция хинолина (изохинолина, фенантридина) с хлорангидридами кислот и цианидом натрия дает устойчивые соединения Райсерта (реакция Райсерта):
- •2.2.3.5. Замещение гидроксигрупп
- •2.2.3.6. Замещение по механизму anrorc
- •2.2.3.7. Технологические аспекты проведения реакций, техника безопасности, экология
2.2.2.2. Реакции ацилирования
Реакции ацилирования широко используются в медицинской промышленности для введения ацильных групп в амино- и гидроксигруппу.
Реагенты для проведения реакций ацилирования. Для ацилирования аминов и фенолов используют следующие реагенты: ClCOCl, AlkOCOCl, RCOF, RCOCl, (RCO)2O, CH2=C=O, RCOOH + (CH3CO)2O, RCOOAr, RCOOAlk, RCOOH. Условия проведения реакций приведены в табл. 2.11:
Таблица 2.11
Условия проведения реакций ацилирования
Ацилирующий агент |
Выделяющийся продукт |
Условия реакции |
RCOCl |
HCl |
Инертный растворитель, кислотосвязывающее средство |
(RCO)2O |
RCOOH |
Нагревание в инертном растворителе |
RCOOH |
H2O |
Избыток кислоты, высокая температура, использование катализаторов – HCl, H2SO4 |
RCOOR1 |
R1OH |
Нагревание в инертном растворителе, отгонка спирта |
CH2=C=O |
нет |
Инертный растворитель |
При выборе ацилирующего агента следует руководствоваться экономическими показателями. Введение ацильной защитной группировки предполагает в дальнейшем ее безвозвратную потерю. Наиболее дешевыми агентами являются эфиры хлоругольной кислоты. В частности, для ацилирования анилина используют метиловый эфир хлоругольной кислоты (ClCOOCH3) с получением фенилуретилана, который является исходным продуктом в синтезе сульфаниламидных препаратов. При выборе между кислотой и хлорангидридом необходимо учитывать реакционную способность субстрата ацилирования. Если субстрат малореакционноспособен, то используют хлорангидрид как более реакционноспособный агент. Если кислота имеет высокую стоимость, целесообразно ее перевести в хлорангидрид. Следует помнить, что при использовании хлорангидрида необходимо применять кислотосвязывающие средства. Ими могут быть ацилируемые амины. При их высокой стоимости для связывания кислоты применяют пиридин или триэтиламин.
Амид или эфир кислоты может быть получен из ее хлорангидрида по реакции Шоттен – Баумана. Метод заключается в медленном добавлении хлорангидрида к щелочному раствору субстрата ацилирования. Реакцию ведут при пониженной температуре. Хороший выход и полное использование реагентов достигается при проведении реакции на поверхности раздела фаз. Это возможно в случаях, когда продукт реакции не растворим в воде.
В техническом органическом синтезе по этой реакции получают производные мочевины. В водный раствор амина, содержащий карбонат натрия, барботируют фосген и отфильтровывают полученный осадок.

При ацилировании кислотой в результате реакции выделяется вода, а т. к. реакция обратима, воду необходимо удалять из сферы реакции или связывать. В синтезе пептидов в качестве водосвязывающего и активирующего агента используют дициклогексилкарбодиимид, который превращается в дициклогексилмочевину и удаляется из сферы реакции:
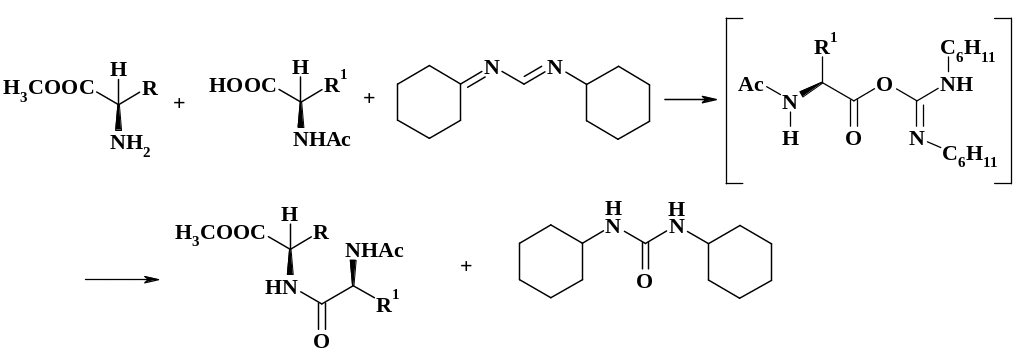
Достоинством является то, что реакция стереоселективна и не наблюдается изменения оптической активности. Способ относительно дорог, но высокий выход и стереоселективность реакции компенсируют этот недостаток. Метод подробно рассмотрен в разделе 3.1.
Хорошим ацетилирующим средством является кетен (CH2=C=O), который получают пиролизом ацетона или уксусной кислоты при 750 оС.

Реакция ацетилирования с кетеном идет практически с количественным выходом в воде. Дикетен – жидкость с Ткип 130 оС, в промышленности его получают димеризацией кетена. С аминами дикетен дает амиды ацетоуксусной кислоты:

Дикетен в последнее время находит весьма широкое применение в промышленном органическом синтезе в качестве ацетилирующего реагента и полноценного заменителя ацетоуксусного эфира в реакциях конденсации с образованием ряда гетероциклических продуктов (пиримидины, 1,4-диазепины, пиразолы и др.). Этот вид сырья при его крупномасштабном производстве является более дешевым, чем ацетоуксусный эфир, а реакции конденсации с участием дикетена проходят в более мягких условиях и зачастую с почти количественным выходом целевого продукта.
Синтез лекарственных средств. Многотоннажным препаратом, широко использующимся в медицинской практике, является ацетилсалициловая кислота (аспирин), которая применяется в качестве противовоспалительного, жаропонижающего и болеутоляющего средства. Имеются сведения о противотромбозном действии препарата. Более подробно механизм действия рассмотрен в разделе 2.1.5. Следует отметить, что в США аспирин является основным болеутоляющим средством, тогда как в Европе в качестве основного компонента болеутоляющих препаратов применяют анальгин.
Аспирин получают ацетилированием салициловой кислоты уксусным ангидридом в апротонном растворителе: Получение жаропонижающих и болеутоляющих средств парацетамол и фенацетин уже рассматривалось в различных разделах. На последней стадии используют ацетилирование уксусным ангидридом.
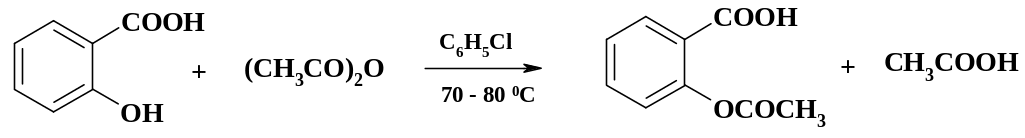

При ацилировании фталевым ангидридом сульфаниламидных препаратов норсульфазола и сульфапиридазина получают препараты фталазол и фтазин, применяемые при кишечных инфекциях.
В отличие от реакции с сульфаниламидами, фталевый и малеиновый ангидриды при взаимодействии с гидразином дают гетероциклы:
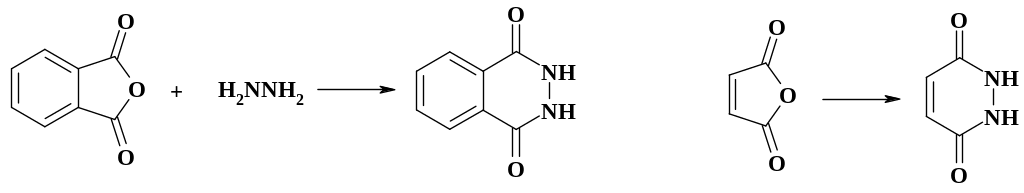
Таким образом, ацилирование гидразина приводит к образованию амидной связи по обеим карбонильным группам с образованием пиридазинового цикла (см. также раздел 2.7).
Фталогидразин и пиридазиндион являются промежуточными продуктами в синтезе гипотензивного средства дегидролазин и сульфаниламидного препарата сульфапиридазин (раздел 2.2.3). Фталильную защиту аминогруппы в аминокислотах и пептидах снимают с помощью гидразингидрата, при этом образуется также фталогидразин (раздел 3.1).
Для проведения реакции ацилирования кислотой используют смесь кислоты с уксусным ангидридом. Так на первой стадии синтеза пуриновых алкалоидов, в частности теофиллина (R = CH3), проводят ацилирование диметилмочевины циануксусной кислотой в присутствии уксусного ангидрида. Следует отметить, что реакционная способность NH-группы в диметилмочевине низка. Уксусный ангидрид и циануксусная кислота образуют смешанный ангидрид уксусной и циануксусной кислоты, обладающий уже высокой реакционной способностью. В результате его взаимодействия с мочевиной происходит реакция ацилирования в довольно мягких условиях.
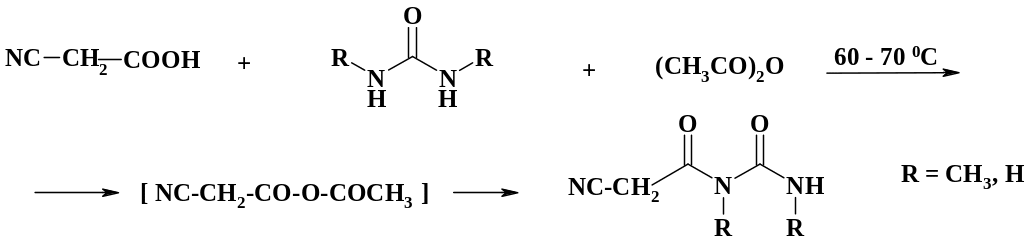
Следующей стадией является реакция циклизации – нуклеофильная атака NH-группы мочевинного фрагмента молекулы на углерод нитрильной группы, условия реакции рассмотрены в разделе 2.7. Полученные цианоацетилмочевины применяются в синтезе производных 4-аминоурацила и урацила.
Примером использования в качестве ацилирующего средства кислоты может служить метод получения нафазолина (нафтизин, санорин). Препарат возбуждает 1- и 2-адренорецепторы, суживает сосуды и зрачок, повышает артериальное давление. При ринитах облегчает носовое дыхание. Применяют его для лечения острых ринитов, аллергических конъюнктивитов и для остановки носовых кровотечений. Как видно из схемы, процесс ацилирования идет в довольно жестких условиях:

Вторая стадия – гетероциклизация – требует применения очень высокой температуры.
