
- •Лекций по курсу «методы получения биологически активных соединений» Электронный вариант на основе учебника: в.С. Мокрушин, г.А. Вавилов
- •Предисловие
- •Введение
- •Глава 1
- •Классификация лекарственных средств
- •Действие лекарственных средств на метаболизм живых организмов
- •1.2. Методы поиска новых препаратов
- •1.2.1. Основные этапы создания лекарственных препаратов, подходы к получению и отбору лекарственных средств
- •1.2.2. Разработка плана синтеза
- •1.3. Сырьевая база химико-фармацевтической промышленности
- •1.3.1. Продукты переработки твердого топлива и коксохимического производства
- •1.3.2. Продукты нефтеоргсинтеза
- •1.3.3. Лесохимическое сырье
- •1.3.4. Некоторые продукты многотоннажных производств
- •1.4. Теоретические аспекты выбора метода синтеза
- •1.4.1. Энергетические факторы
- •1.4.2. Классификация реакций
- •1.4.3. Механизм и кинетика реакций
- •1.4.4. Уравнения Гаммета, Тафта
- •1.4.5. Квантово-химические расчеты
- •1.4.6. Выбор растворителя
- •Характеристики растворителей
- •1.5. Разработка технологической схемы производства
- •1.5.1. Категории и типы технологических схем
- •1.5.2. Правила составления и основные требования к технологическим схемам
- •1.5.3. Оформление чертежей технологических схем
- •1.5.4. Типовое оснащение и привязка химического реактора к конкретному производству
- •Глава 2 методы получения промежуточных продуктов и синтетических лекарственных препаратов
- •2.1. Реакции электрофильного замещения
- •2.1.1. Нитрование
- •2.1.1.1. Реакции нитрования в синтезе некоторых лекарственных препаратов
- •2.1.1.2. Химические особенности реакций нитрования, реагенты, механизм
- •2.1.1.3. Нитрование арил и гетариламинов
- •2.1.1.4. Нитрование азотной кислотой
- •2.1.1.5. Технологические аспекты нитрования
- •2.1.1.6. Использование реакции нитрования для получения полупродуктов и лекарственных средств
- •2.1.1.7. Получение нитроэфиров и n-нитросоединений Так же как и при нитровании ароматических соединений, при получении нитроэфиров используют смесь азотной и серной кислот:
- •2.1.2. Нитрозирование
- •2.1.2.1. Механизм нитрозирования, реагенты
- •2.1.2.2. Особенности проведения реакции
- •2.1.2.3. Особенности структуры и свойств нитрозосоединений
- •2.1.2.4. Практика проведения реакции нитрозирования
- •2.1.2.5. Техника безопасности, экология
- •2.1.3. Сульфирование
- •2.1.3.2. Реагенты, использующиеся при проведении реакции сульфирования, механизм реакции
- •2.1.3.3. Особенности сульфирования, побочные реакции
- •2.1.3.4. Влияние температуры
- •2.1.3.5. Сульфирование бензола и его производных
- •2.1.3.6. Сульфирование анилина и его производных
- •2.1.3.8. Сульфирование хлорсульфоновой кислотой
- •2.1.3.9. Техника безопасности, экология
- •2.1.4. Сульфохлорирование
- •2.1.4.1. Химические особенности реакции
- •2.1.4.2. Технологические аспекты сульфохлорирования
- •2.1.4.3. Синтез сульфаниламидных препаратов
- •2.1.4.4. Техника безопасности, экология
- •2.1.5. Введение углеродных остатков в Ароматическое и гетероциклическое ядро
- •2.1.5.1. Реакции с-алкилирования
- •Реагенты, катализаторы. Как отмечалось, реагентами могут быть алкилгалогениды, олефины и спирты:
- •Механизм реакции. При взаимодействии реагента и катализатора быстро образуется карбокатион, его присутствие зафиксировано с помощью спектроскопии ямр:
- •2.1.5.2. Реакции гидроксиалкилирования
- •2.1.5.3. Реакции хлоралкилирования
- •2.1.5.4. Реакции аминоалкилирования
- •2.1.5.5. Реакции с-ацилирования
- •2.1.5.6. Реакции с-формилирования
- •2.1.5.7. Реакция карбоксилирования
- •2.1.5.8. Карбоксилирование алифатических соединений
- •2.1.5.9. Техника безопасности, экология
- •2.1.6. Галогенирование
- •2.1.6.1. Препараты, содержащие в молекуле атомы галогенов
- •2.1.6.2. Реагенты, механизм реакций галогенирования
- •2.1.6.3. Хлорирование ароматических соединений
- •2.1.6.4. Бромирование, иодирование
- •2.1.6.5. Технологические аспекты галогенирования
- •2.1.6.7. Галогенирование альдегидов, кетонов и кислот
- •2.1.6.8. Свободнорадикальное галогенирование
- •Энергия стадий процесса
- •2.1.6.10. Получение галогенамидов
- •2.1.6.11. Окислительное хлорирование
- •2.1.6.12. Меры предосторожности при проведении реакций галогенирования
- •2.1.6.13. Экология
- •2.2. Реакции нуклеофильного замещения
- •Реакции нуклеофильного замещения у насыщенного атома углерода
- •2.2.1.1. Типы реакций
- •Реагенты для проведения реакций алкилирования
- •Механизмы реакций
- •Алкилирование аминов
- •Селективные методы синтеза первичных аминов
- •Селективные методы синтеза вторичных аминов
- •Алкилирование спиртов и фенолов
- •Алкилирование сн кислот
- •Алкилирование гетероциклических соединений
- •Техника безопасности, экология
- •2.2.2. Реакции нуклеофилов с соединениями,
- •2.2.2.1. Обзор реакций, их кинетика и механизм
- •2.2.2.2. Реакции ацилирования
- •2.2.2.3. Реакции нитрилов с нуклеофилами
- •2.2.2.4. Реакции этерификации, получение амидов и гидразидов кислот
- •2.2.2.5. Получение азометинов и гидразонов
- •2.2.2.6. Методы получения первичных аминов с помощью перегруппировок
- •2.2.2.7. Использование реакций в основном органическом синтезе
- •2.2.2.8. Технология, техника безопасности, экология
- •2.2.3. Нуклеофильное замещение в ряду ароматическИх и гетероциклических оединений
- •2.2.3.1. Нуклеофильное замещение по типу sn1
- •2.2.3.2. Ариновое замещение
- •2.2.3.3. Реакции нуклеофилов с ипсо-замещением нуклеофугных групп
- •Получение полупродуктов и лекарственных препаратов. В отсутствие электроноакцепторных заместителей замещение атома хлора происходит при высокой температуре и в присутствии катализатора:
- •2.2.3.4. Нуклеофильное замещение водорода
- •Еще в начале хх в. Было найдено, что реакция хинолина (изохинолина, фенантридина) с хлорангидридами кислот и цианидом натрия дает устойчивые соединения Райсерта (реакция Райсерта):
- •2.2.3.5. Замещение гидроксигрупп
- •2.2.3.6. Замещение по механизму anrorc
- •2.2.3.7. Технологические аспекты проведения реакций, техника безопасности, экология
Действие лекарственных средств на метаболизм живых организмов
Препараты воздействуют на различные биологические системы организма. Взаимодействие ЛС с объектами организма может вызвать ингибирование или стимуляцию рецепторов медиаторов на мембране клеток, ингибирование ферментов, гормонов, биосинтеза нуклеиновых кислот и т. д. Из-за того, что многочисленные метаболитические процессы тесно взаимосвязаны, обычно ЛС влияют на метаболизм нескольких продуктов. При этом говорят о механизме действия лекарственного средства. В данном разделе рассмотрен ряд препаратов с различным механизмом действия, биологический эффект других лекарственных средств будет описан при рассмотрении их синтеза.
Одним из нейромедиаторов периферических нервных окончаний и в синапсах ЦНС является норадреналин (НА) – предшественник адреналина. Биосинтез НА происходит в несколько стадий: аминокислота тирозин гидроксилируется, образующийся дигидроксифенилаланин (ДОФА) превращается в дофамин и далее в НА. Структуры мембраны тканей, реагирующие с НА, называют адренорецепторами. Взаимодействие НА с ними на клеточной мембране приводит к усилению выработки ц-АМФ (вторичный медиатор). Адреналин – гормональное вещество, влияющее на обменные процессы, повышает артериальное давление, повышает содержание сахара в крови, улучшает функциональную способность скелетных мышц.
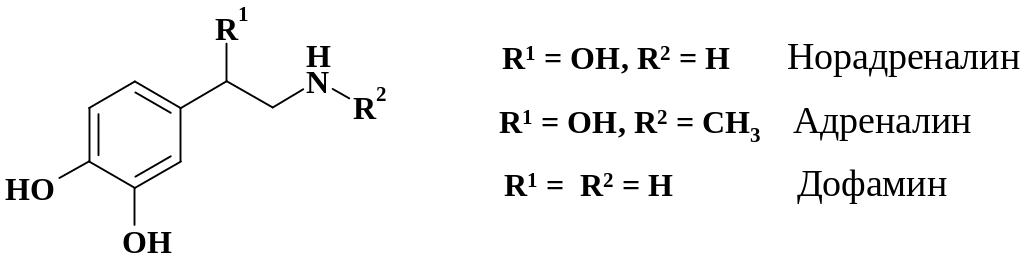
Существуют два вида адренорецепторов – (1 и 2) и (1 и 2). При возбуждении -адренорецепторов наблюдается возбуждение (сужение сосудов, сокращение матки). Возбуждение -адренорецепторов вызывает тормозные эффекты и расширение сосудов, при этом повышается тонус миокарда.
К препаратам, стимулирующим -адренорецепторы (адреномиметики), относится фенилэфрин (мезатон). Препарат применяют для лечения анафилактического и нейрогенного шока, выведения из состояния коллапса, он обладает сосудосуживающим действием.
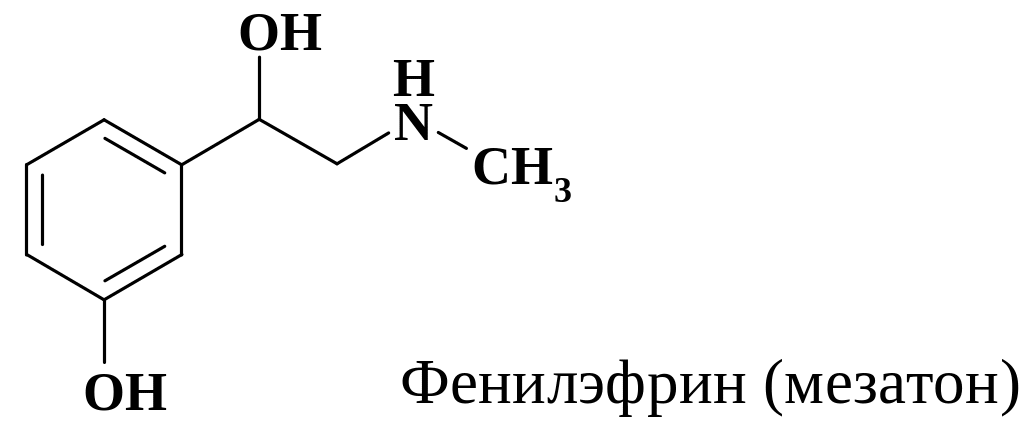
Фенилэфрин (мезатон) отличается от адреналина отсутствием одной из гидроксильных групп. Это отличие приводит к большей стойкости препарата, повышение артериального давления происходит менее резко, но эффект более длителен. Субстанция препарата фенилэфрин входит в качестве одной из компонент в комбинированный препарат «Колдрекс».
К -адреноблокаторам относится ряд препаратов: альфузозин, бутироксан, доксазозин, ницерголин, пророксан, фентоламин и другие. В качестве примеров рассмотрим два препарата:
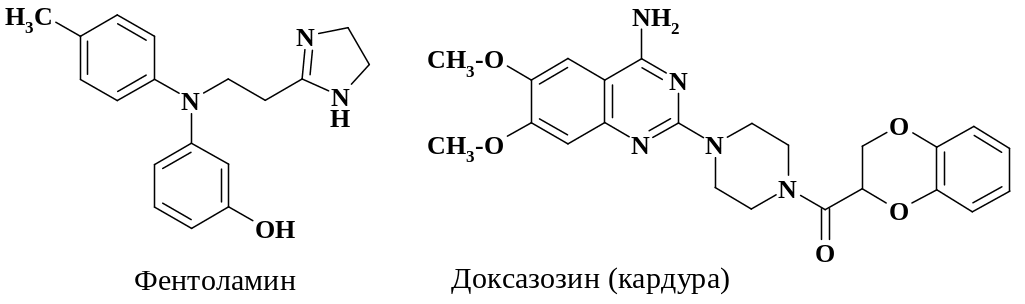
-Адреноблокатор фентоламин (регитин) блокирует 1- и 2-рецепторы, передачу нервных импульсов, сужающих сосуды; снимает спазм, расширяет периферические кровеносные сосуды, особенно артериолы, улучшает кровоснабжение. Структура препарата имеет отдельные фрагменты метаболита, но их расположение в пространстве отличается. Тем самым осуществляется более прочное взаимодействие с -рецепторами адреналина и их блокада. Препарат доксазозин селективно блокирует 1-рецепторы, обладает гипотензивным, сосудорасширяющим, спазмолитическим действием. Восстанавливает уровень холестерина, подавляет синтез коллагена в сосудистой стенке. Используют его для лечения артериальной гипертензии и начальных стадий доброкачественной гиперплазии (аденомы) предстательной железы. Структура этого лекарственного средства не похожа на адреналин, однако наблюдается длительное ингибирование рецепторов.
Стимуляторами -адренорецепторов являются изопреналин (стимулятор 1- и 2-рецепторов), добутамин (1-рецепторов) и сальбутамол (2-рецеп-торов). Структура препаратов приведена на схеме:
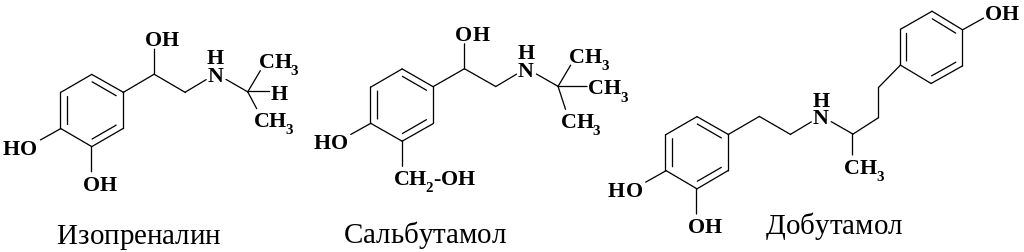
Изопреналин активирует аденилатциклазу, что приводит к накоплению в клетках ц-АМФ. Это препятствует сокращению гладкой мускулатуры и способствует расслаблению бронхов. Препарат обладает бронхолитическими свойствами, вызывает учащение и усиление сокращений сердца, повышает потребление сердцем кислорода. Сальбутамол активирует аденилатциклазу, селективно стимулирует 2-рецепторы. Используют его для предупреждения и купирования бронхоспазмов. Добутамин активирует 1-рецепторы селективно, обладает кардиотоническим действием. Препараты имеют определенное сходство со структурой адреналина, но вместо метильной группы имеют объемистый гидрофобный заместитель.
К группе препаратов -адреноблокаторов относятся атенолол, ацебуталол, бетаксалол, метопролол, талинолол и др. Рассмотрим один из них.
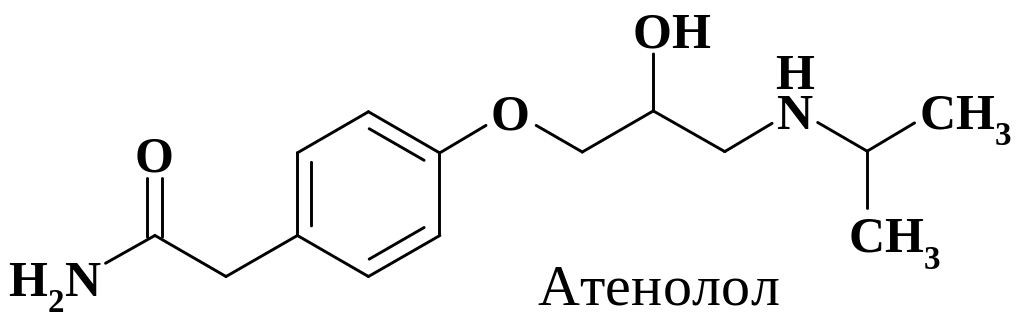
Атенолол – кардиоселективный препарат, является -адреноблокатором. Применяется при лечении стенокардии и расстройствах сердечного ритма, лечении гипертонической болезни (в сочетании с диуретиками). Препарат также имеет определенное сходство по структуре с адреналином, но группы другие и действует уже на -рецепторы.
Рассмотрим еще один из химических факторов (медиаторов), участвующих в регуляции жизненных функций организма, гистамин:
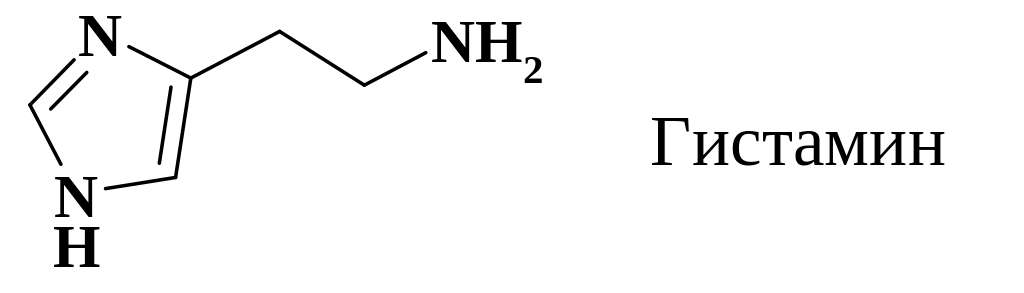
В обычных условиях гистамин находится в связанном, неактивном состоянии. При некоторых патологических состояниях (анафилактический шок, ожоги, отморожения, крапивница и другие аллергические заболевания) количество свободного гистамина увеличивается. Это вызывает спазм гладкой мускулатуры, в т. ч. мускулатуры бронхов, расширение капилляров, увеличение проницаемости их стенок, что и вызывает отек окружающих тканей. Гистамин вызывает усиление секреции желудочного сока. Некоторое количество гистамина содержится в ЦНС, где он исполняет роль нейромедиатора. Данный метаболит специфично связывается с рецепторами. Найдены два их типа – Н1 и Н2.
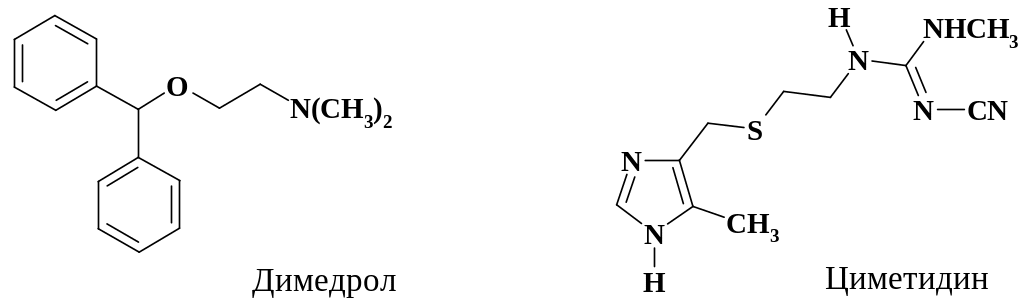
Антигистаминные препараты – блокаторы Н1 рецепторов (димедрол, дифенгидрамин; кетотифен; супрастин) – обладают антиаллергическим действием. Блокаторы Н2 рецепторов – циметидин, фамотитин, ранитидин применяются – при лечении язвенной болезни желудка. Структуры димедрола и циметидина приведены на схеме.
Еще одним нейромедиатором является ацетилхолин (АЦХ), играющий важную роль в проведении нервного импульса.

В нервных окончаниях имеются два типа рецепторов АЦХ – мускаринового типа (м-рецепторы) и никотинового типа (н-рецепторы). К антихолинэргическим (холинолитическим) средствам относят препараты, препятствующие взаимодействию АЦХ с рецепторами. Некоторые холинолитики проникают через гематоэнцефалический барьер, их называют центральными холиноблокаторами. В качестве м-холинолитика можно привести арпенал – спазмолитик, применяющийся для снятия печеночной, почечной колик, для лечения пилороспазма, язвенной болезни желудка и двенадцатиперстной кишки.
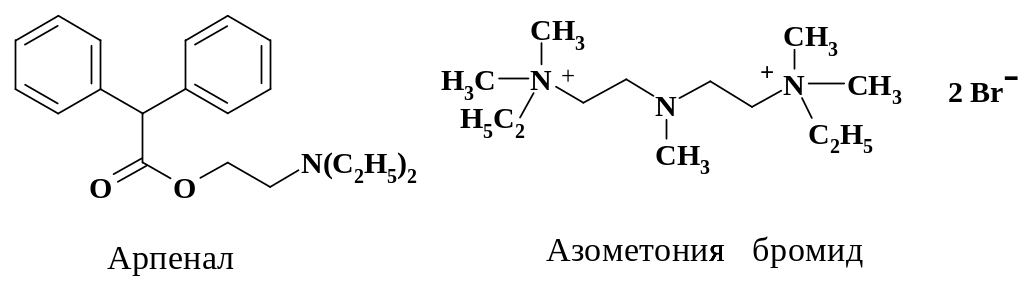
Препарат блокирует также центральные и н-рецепторы. Препараты, взаимодействующие с н-рецепторами, обладают ганглиоблокирующим, спазмолитическим действием. В качестве примера можно привести препарат азаметония бромид (пентамин), блокирующий н-рецепторы вегетативных ганглиев. Препарат тормозит передачу нервного возбуждения, обладает спазмолитическим и гипотензивным действием. Применяют при гипертоническом кризе, болевом синдроме язвенной болезни, отеке легких, отеке головного мозга, приступах облитерирующего эндартериита, атеросклероза и др.
Для лечения заболеваний, вызванных нарушениями функционирования центральной нервной системы, в настоящее время ведется активный поиск активаторов и блокаторов серотониновых рецепторов 5-НТ1, 5-НТ2, 5-НТ3 и 5-НТ4. Селективно возбуждает 5-НТ1B/1D рецепторы препарат наратриптан, использующийся для лечения мигрени. Также активирует 5-НТ1D рецепторы суматриптан, который останавливает развитие приступа мигрени и при этом не обладает анальгезирующим действием. Структура этих препаратов имеет определенное сходство с метаболитом – серотонином, который также является нейромедиатором. Формулы препаратов приведены на схеме:
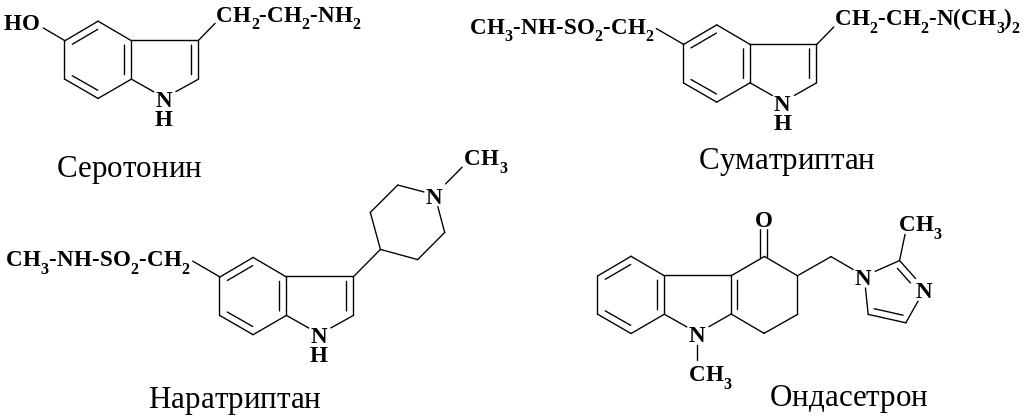
Внесенные в молекулу метаболита изменения позволяют более прочно связываться с рецепторами. Селективным блокатором центральных и периферических 5-НТ3 рецепторов является препарат ондасетрон. Это лекарственное средство подавляет рвотный рефлекс, устраняет и подавляет рвоту, вызванную освобождением серотонина при лечении онкологических больных цитостатиками и при лучевой терапии.
Тормозным химическим медиатором является -аминомасляная кислота (ГАМК). Она содержится в ЦНС и принимает участие в обменных процессах головного мозга. При ее действии усиливаются энергетические процессы головного мозга, улучшается кровоснабжение и утилизация глюкозы. Улучшает мыслительные процессы, память, оказывает мягкое психостимулирующее действие.
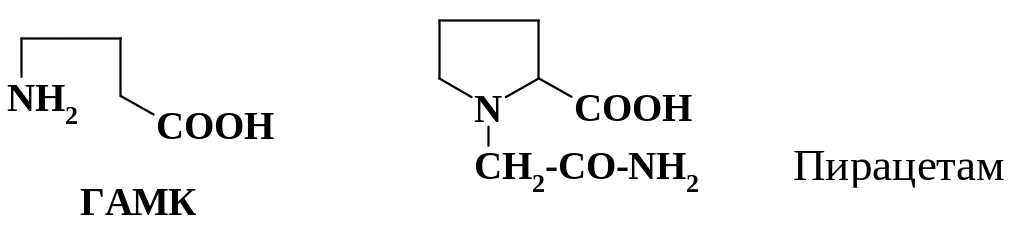
Пирацетам (ноотропил) относится к ноотропам и имеет близкую к ГАМК структуру, однако не связывается с рецепторами этого соединения. Препарат активирует ассоциативные процессы головного мозга, улучшает память, настроение, интеллектуальную активность, восстанавливает нарушенные функции мозга. Близко к рецепторам ГАМК расположены бензодиазепиновые рецепторы.
Хорошо известна роль фолиевой кислоты (ФК) в метаболизме клетки – биосинтез пуринов, пиримидинов, синтез таких аминокислот, как метионин, гистидин и глицин. Недостаток этого витамина приводит к нарушению роста и различным формам анемии. Сама ФК не является коферментом, но при восстановлении дает активную форму – кофермент тетрагидрофолиевую кислоту (ТГФК). На последней стадии метаболитического процесса дигидроФК превращается с помощью фермента дигидрофолатредуктазы (ДГФР) в ТГФК. Для ФК константа Михаэлиса Км = 1 10 –6. Модификация молекулы ФК с помощью замены карбонильной группы в птеридиновом цикле на аминогруппу (аминоптерин) приводит к более прочному связыванию полученного соединения с ДГФР, Км = 110 –8. Дополнительное введение метильной группы в фрагмент п-аминобензойной кислоты дает практически необратимое ингибирование фермента, Км = 110 –11. Блокирование ДГФР приводит к прекращению синтеза нуклеиновых кислот.
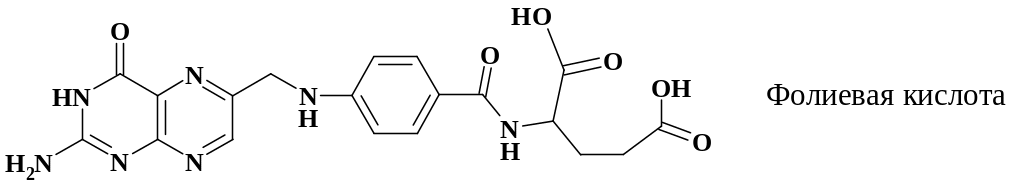

В клинической онкологической практике препарат метотрексат является одним из основных и входит в различные комбинации. В монохимиотерапии используют для лечения хорионкарциномы матки, хориоаденомы, острого лимфолейкоза, рака груди, остеосаркомы и др.
Если ФК является метаболитом, то аминоптерин и метотрексат – антиметаболиты. Антиметаболит – соединение, близкое по структуре к метаболиту, но блокирующее превращение метаболита в клетке. Понятие антиметаболит было введено Вулли в 1951 г. К антиметаболитам относятся противораковые препараты меркаптопурин, фторурацил (см. разделы 2.3 и 2.7), а также сульфаниламидные препараты, пенициллины и цефалоспорины. Более подробно рассмотрим классический пример механизма действия сульфаниламидных препаратов (синтез этих ЛС приведен в разделе 2.1.4).
Для млекопитающих витамином является ФК, а в клетках чувствительных микроорганизмов ФК синтезируется и витамином служит п-аминобен-зойная кислота (ПАБК) – существенное отличие! Если бактерия получит вещество, похожее по геометрии на ПАБК, но другого строения, она не сможет размножаться и, в конечном итоге, погибнет.
Основной стратегией получения многих антибактериальных средств является задержка развития инфекции на 5 – 7 дней, после чего включаются иммунные силы организма.
Если R = H, то препарат – стрептоцид. В современных препаратах этого класса группа R является гетероциклом, который моделирует остаток глутаминовой кислоты. По геометрии сульфаниламидная группа близка к карбоксигруппе, величина рКа NH группы также близка к величине рКа карбоксигруппы в ПАБК.
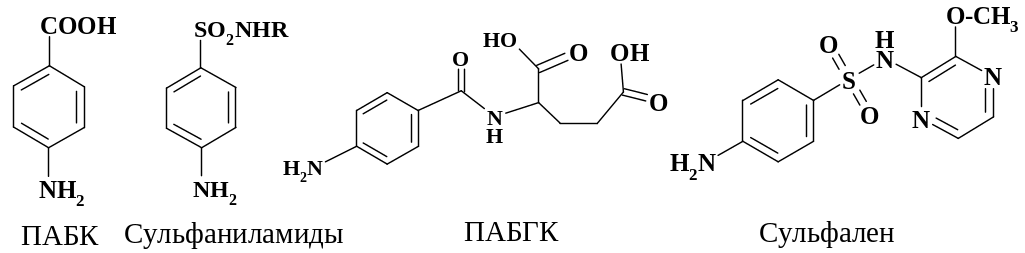
В качестве примера на схеме приведены п-аминобензоилглутаминовая кислота и препарат сульфален.
Совершенно другой механизм действия имеют известные и широко использующиеся антибактериальные средства – пенициллины и цефалоспорины. По геометрии и расположению полярных и гидрофобных групп они похожи на N-ацетилмурамовую кислоту – компонент клеточной оболочки бактерий. Препараты ингибируют полимеразу пептидогликана и транспептидазу. При этом нарушаются поздние этапы синтеза клеточной оболочки микроорганизмов. Возникающие дефекты приводят к осмотической неустойчивости бактерии и вызывают ее гибель. Препараты преимущественно воздействуют на бактериальную клетку, а не на растущие клетки хозяина, т. к. в структуру клеточной стенки эукариот входят производные нейраминовой кислоты, а не мурамовой.
Современным классом антибактериальных препаратов являются фторхинолоны, приведена общая формула препаратов:
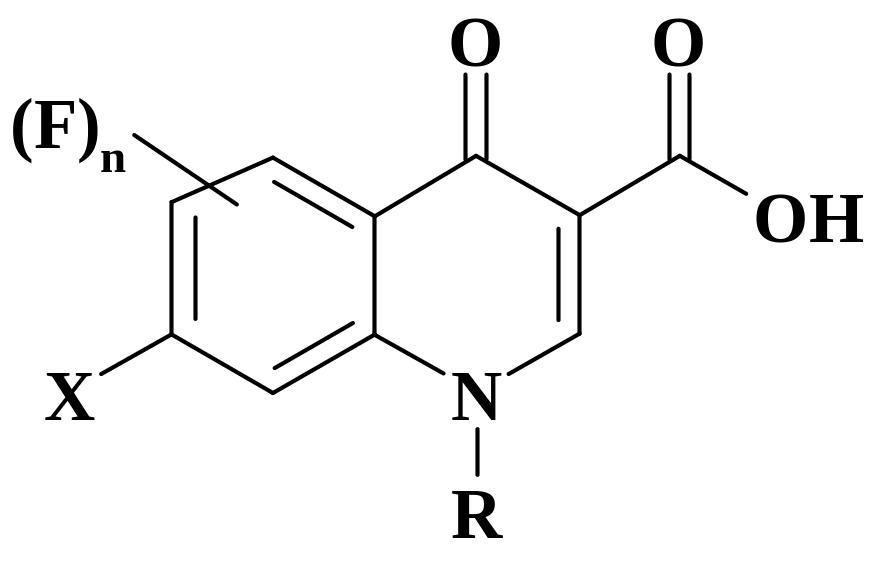
Подробный перечень препаратов приведен в разделе 2.3. Их механизм действия отличен от сульфаниламидов и пенициллинов. Они ингибируют ДНК-гиразу – фермент, вызывающий суперспирализацию ДНК за участком, в котором открыты (свободны для транскрипции) 10 нуклеиновых оснований. Без суперспирализации в молекуле ДНК возникают существенные напряжения, которые потребовали бы увеличения числа оснований, приходящихся на один виток, до 11. Фермент найден только в клетках прокариот. В клетках эукариот имеются ферменты, которые могут разрезать одну или обе нити ДНК (ДНК-топоизомеразы I или II) и тем самым снимать в спирали напряжение при генной экспрессии. Однако активные центры этих ферментов существенно отличаются от такового в ДНК-гиразе. Ингибирование ДНК-гиразы приводит к блокированию синтеза РНК на матрице ДНК, что ведет к гибели клетки. Специфическое действие фторхинолонов на бактерии заключается в том, что они ингибируют ДНК-гиразу бактерий, но не связываются с ДНК топоизомеразами клеток хозяина.
Рассмотренные антибактериальные препараты приближаются к «волшебной пуле Эрлиха» (Пауль Эрлих, 1854-1915 гг., Нобелевская премия совместно с И.И. Мечниковым в 1908 г.): препарат должен поражать определенный биологический объект микроорганизма или самого организма не нанося вреда другим жизненно важным функциям больного. Эрлихом доказана возможность целенаправленного синтеза химиотерапевтических средств, им введен в практику противосифилитический препарат сальварсан.
Примером ингибитора ферментов нуклеинового обмена может служить флуороурацил (5-фторурацил), который вошел в клиническую онкологическую практику еще в 60-е гг. ХХ века. Препарат является антиметаболитом урацила, конкурирует с ним за тимидилатсинтетазу и нарушает образование ДНК. Останавливает превращение дезоксиуридиловой кислоты в тимидиловую кислоту за счет того, что энергия связи C-F выше, чем связи С-Н. Дефицит тимидина приводит к гибели быстроделящихся клеток злокачественных опухолей молочной железы, желудка, поджелудочной железы и отделов толстого кишечника. Тогда же был создан 6-меркаптопурин – препарат, применяющийся для лечения острого лимфолейкоза, миелолейкоза, лимфобластного лейкоза и других заболеваний. Замена карбонильной группы в гипоксантине на тиокарбонильную приводит к ингибированию биосинтеза пуриновых нуклеозидтрифосфатов. Препарат превращается в меркаптопуринфосфорибозид, который не может превратиться в АМФ и ГМФ. Накопление инозинмонофосфата приводит к аллостерическому ингибированию фермента глутамин-5-фосфорибозилпирофосфатамидотрансферазы. Недавно был получен препарат флударабин, ингибирующий ДНК-полимеразу. В молекулу этого препарата введен остаток арабинозы вместо рибозы в аденозине, а во второе положение пуринового цикла – атом фтора.
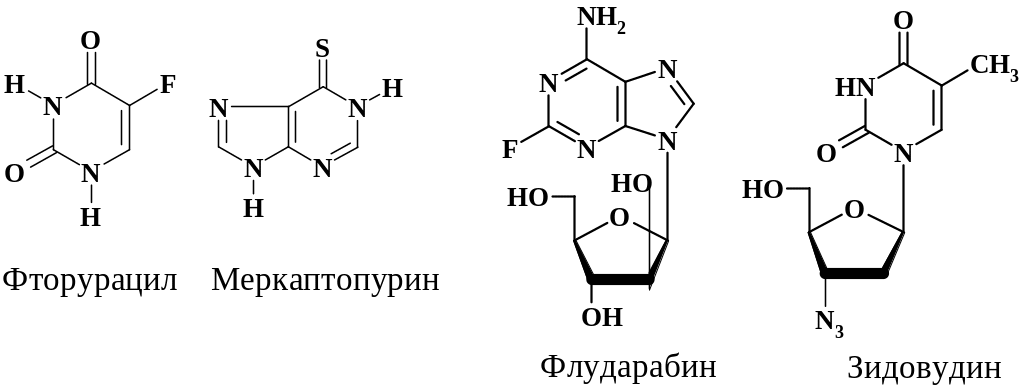
Применяют флударабин при лечении хронического лимфолейкоза и лимфомы. Тот же принцип применен при получении препарата зидовудин (азидотимидин, АЗТ), который используют для лечения поздних стадий ВИЧ-инфи-цированных больных. Замена гидроксигруппы в тимидине на азидную приводит к ингибированию вирусной ДНК-полимеразы (обратной транскриптазы). При действии АЗТ понижается репликация вирусов, т. к. обратная транскриптаза вируса в 20 – 30 раз более чувствительна к действию этого лекарственного средства, чем ДНК-полимераза клеток млекопитающих.
Цитостатическим действием (блокирующим деление клеток) обладают препараты, алкилирующие ДНК за счет наличия в молекуле азотипритной группировки или этилениминной. В качестве примеров можно привести препараты тиотепа (тиотэф) и мелфалан. Эти лекарственные средства алкилируют ДНК, нарушают обмен нуклеиновых кислот и блокируют митотическое деление преимущественно клеток злокачественных опухолей.
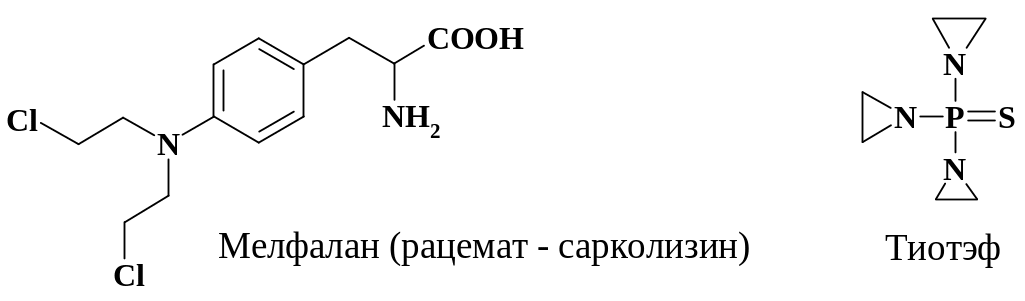
В данном разделе рассмотрены лишь некоторые принципы действия ограниченного числа препаратов из всего их разнообразия. Биологическое действие ряда препаратов приведено при описании их синтеза.
Нахождение высокоэффективных препаратов, особенно антибактериальных, и внедрение их в медицинскую практику не позволяет прекращать поиск новых средств. Препараты сульфаниламидного и пенициллинового ряда произвели революцию в лечении бактериальных инфекций. Были спасены миллионы больных. Однако уже в 70-е гг. ХХ в. были изъяты из практики бензилпенициллин, стрептоцид, норсульфазол и сульфадимезин в связи с их малой эффективностью. Микроорганизмы «приспособились» к ним, возникли новые штаммы бактерий, которые либо обезвреживали эти лекарственные средства, либо не включали их в свой метаболизм. Возникла проблема лекарственной устойчивости (резистентности) бактерий. Причиной возникновения резистентности является вариабельность генетической информации микроорганизмов и «помощь» самих больных – при исчезновении симптомов заболевания очень часто больные прекращали прием препарата. Наиболее устойчивые клоны бактерий выживали и через десятилетия остались те, на которые препарат уже не действовал. При неэффективном лечении туберкулеза появились многочисленные случаи лекарственно устойчивого заболевания. Поэтому уже в известных рядах химических соединений ведется постоянный поиск новых ЛС. Стратегия поиска заключается в том, чтобы повысить период полувыведения препарата из организма и сделать его максимальным (получение так называемых пролонгов – препаратов длительного действия). При этом забывчивость и небрежность больного уже не приводит к отбору устойчивых микроорганизмов, т. к. в плазме крови концентрация препарата остается достаточно высокой, убивающей все клоны. Постоянный прием больным препаратов, блокирующих рецепторы или ферменты, может привести к включению компенсаторных механизмов организма, поэтому приходится менять препарат, подбирать лекарственное средство с другим механизмом действия. Поэтому также целесообразен поиск новых препаратов. Лекарственные средства, как уже отмечалось, обычно воздействуют на несколько метаболитических процессов. Наряду с полезным эффектом проявляется и вредное воздействие на организм – побочное действие. Препараты применяют для лечения в определенной дозе (терапевтическая доза – Т), при высоких дозировках может наблюдаться смертельный исход. Дозу, при которой гибнет 50 % животных, называют LD50 (полулетальная доза). Соотношение LD50 к терапевтической дозе называют терапевтическим индексом (It), II = LD50/T. Таким образом, LD50 должна быть существенно больше, чем Т, чем выше терапевтический индекс, тем безопаснее прием лекарства. Поиск ЛС с тем же механизмом действия, но имеющих более высокий It, является одним из перспективных направлений создания новых препаратов. И, наконец, перед химиками, биологами и биохимиками стоит проблема создание новых противораковых и противовирусных препаратов. Создание лекарственных средств для лечения ВИЧ-инфекции, которую называют чумой современности, является весьма актуальной проблемой.
