
- •Моносахариды. Строение, номенклатура. Стереохимия и конформация моносахаридов. Аномерный центр: его стереохимия, особые свойства гидроксильной группы.
- •Важнейшие производные моносахаридов: гексозы, дезоксисахара, аминосахара, уроновые кислоты, нейраминовая и сиаловые кислоты.
- •Химические свойства моносахаридов (алкилирование, ацилирование, восстановление, окисление, енолизация, гликозилирование).
- •Олигосахариды. Классификация, номенклатура, стереохимия.
- •Определение моносахаридного состава
- •Определение мест присоединения моносахаридных остатков друг к другу
- •Последовательность звеньев в молекуле гетероолигосахарида.
- •Метод Кенигса-Кнорра.
- •Ортоэфирный метод.
- •Оксазолированный метод
- •Стериоспецифичность
- •Трихлорацетимидатный метод
- •Полисахариды. Классификация. Гомополисахариды: крахмал, целлюлоза, гликоген, хитин, декстран. Гетерополисахариды: гемицеллюлоза, пектиновые вещества.
- •Общие принципы установления строения полисахаридов.
- •Группоспецифические вещества крови. Антигены и антитела, агглютинация.
- •Гликолипиды. Гликозилдиглицериды, цереброзиды. Ганглиозиды: классификация и биологическая роль.
- •Фосфолипиды. Строение и номенклатура. Глицерофосфолипиды. Полиглицерофосфаты, фосфоинозитиды.
- •Глицерофосфолипиды:
- •Полиглицерофосфаты:
- •Фосфоинозитиды:
- •Ферменты липидного обмена. Специфичность, использование в полусинтезе липидов.
- •Методы синтеза фосфолипидов. Использование фосфиттриэфирного и н-фосфонатного методов для образования фосфодиэфирной связи.
- •Фосфодиэфирный метод
- •Выделение липидов из природного сырья.
- •Сфинголипиды. Сфингозиновые основания, типы природных сфинголипидов. Сфингофосфосфолипиды.
- •Липиды и биологические мембраны
- •Фазовые состояния липидных агрегатов, фазовые переходы. Динамическое состояние липидов в бислое. Понятие о жидкокристаллическом состоянии. Латеральная диффузия и флип-флоп.
- •Витамины и кофакторы ферментов. Общая характеристика витаминов группы в. Другие водорастворимые витамины.
- •Биологическая роль оксидоредуктаз.
- •Витамин в1 (тиамин). Нахождение в природе, биологическая роль тиаминпирофосфата (кокарбоксилазы) как кофермента альдегиддегидрогеназ и дегидрогеназ.
- •Витамин в2 (рибофлавин), флавинмононуклеотид (фмн) и флавинадениндинуклеотид (фад).
- •Витамин в3 (пантотеновая кислота). Строение, биологическая роль как части кофермента а.
- •Витамин рр (никотиновая кислота и никотинамид). Принципы биологического действия: понятие о над- и фад-зависимых ферментах.
- •Витамин в6 (пиридоксаль). Биологическая роль пиридоксаля как кофермента трансаминаз.
- •Витамин Вс (фолиевая кислота). Биологическая роль в переносе одноуглеродных фрагментов.
- •Витамины группы в12 (цианкобаламин, оксикобаламин). Строение и биологическое действие.
- •Витамин н (биотин). Строение, биологическое действие.
- •Витамин n (липоевая кислота). Биологическая роль в процессах окислительного декарбоксилирования.
- •Витамин с (аскорбиновая кислота).
- •Витамины группы а. Витамин а1 (ретинол) и витамин а2 (дегидроретинол), их роль в зрительном процессе. Β-Каротин - провитамин а.
- •Витамины группы к, убихиноны. Роль в системе свертывания крови.
- •Витамины группы е (токоферолы). Биологическое действие.
- •Незаменимые ненасыщенные кислоты (витамины группы f). Эйкозаноиды. Каскад арахидоновой кислоты. Понятие о простагландинах и лейкотриенах.
- •Каскад арахидоновой кислоты
- •Витамины группы d, строение, биологическое действие. Холестерин как предшественник витаминов группы d.
- •Понятие о способах и механизме межклеточной сигнализации. Локальные химические медиаторы, гормоны, нейромедиаторы. Механизмы действия водорастворимых и жирорастворимых сигнальных молекул.
- •Общее представление о механизме действия стероидов на молекулярном уровне.
-
Ортоэфирный метод.
Кочетковым предложено использовать в роли гликозилирующих агентов в синтезе 1,2-гранс-гликозидов 1,2-ортоэфиры сахаров с применением в качестве катализатора перхлората 2,6-диметилпиридиния. При замене катализатора (например, на я-толуол сульфокислоту) и растворителя реакция протекает по другому направлению, в сторону переэтерификации.


-
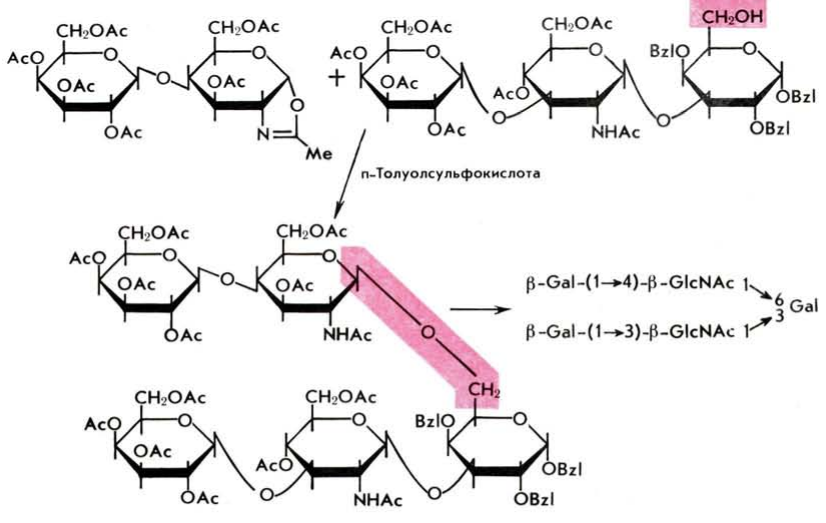
Оксазолированный метод
Гликозилгалогениды ацилированных 2-амино-2-дезоксисахаров чрезвычайно неустойчивы и легко превращаются в соответствующие 1,3-оксазолиновы производные. Последние в присутствии кислых катализаторов легка реагируют с гидроксилсодержащими соединениями с образованием 1,2-гранс-гликозидной связи.

-
Стериоспецифичность
И в случае гликозилгалогенидов, и в случае ортоэфиров сахаров истинным гликозилирующим агентам являются образующиеся на промежуточной стадии гликозил-катион или ацилоксониевый ион
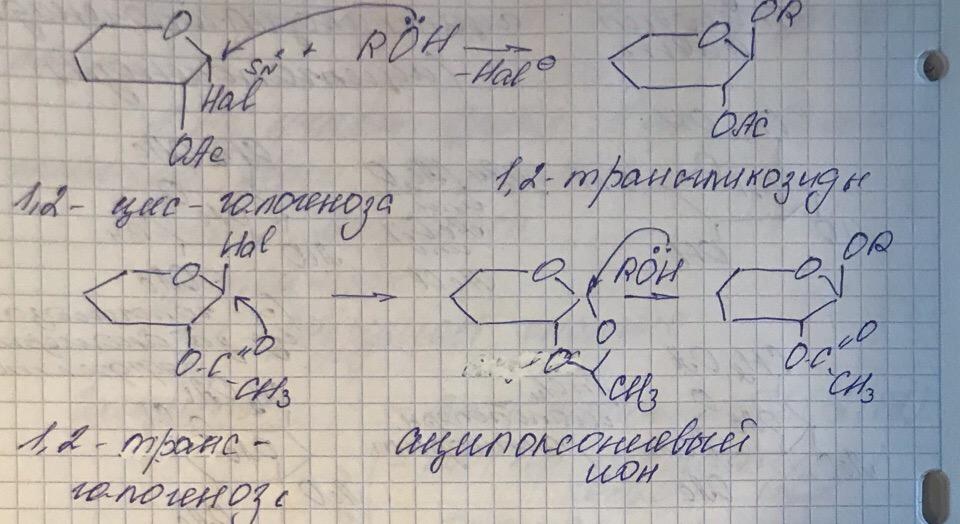
Такие реакции приводят к 1,2-гранс-гликозидам из-за «соучастия» ацильной группы при С-2 (взаимодействие кислородного атом карбоксил ацильной группы с углеродным атомом аномерного центра).

Значительно большие затруднения вызывает синтез 1,2-цисгликозидов, и их удается получить лишь с использованием производных сахаров, имеющих при С-2 заместитель, не способный к «эффекту соучастия».
-
Трихлорацетимидатный метод
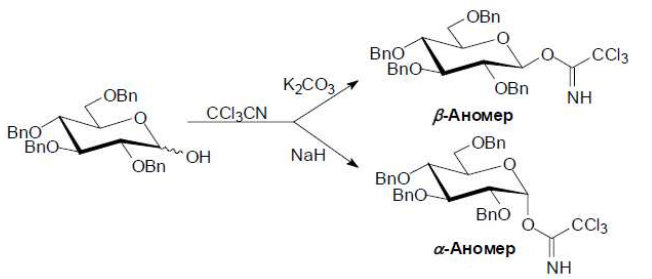
Разделение хроматографией:
-
Полисахариды. Классификация. Гомополисахариды: крахмал, целлюлоза, гликоген, хитин, декстран. Гетерополисахариды: гемицеллюлоза, пектиновые вещества.
Полисахариды (гликаны) представляют собой высокомолекулярные соединения, образующиеся при поликонденсации моносахаридов.
Классификация:
-
Гомополисахариды.
-
Целлюлоза (β-D-Glc-(1→4)):
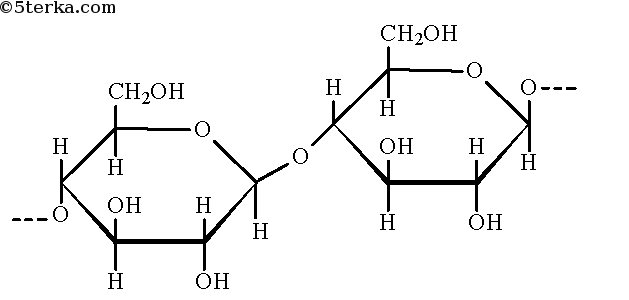 n=1:
целлобиоза
n=1:
целлобиоза
-
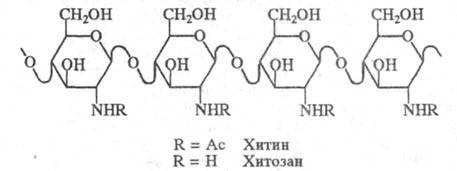
Хитин (β-D-GlcNAc-(1→4)):
-
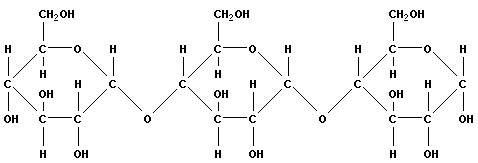
Крахмал (α-D-Glc-(1→4)):
 n=1:
мальтоза
n=1:
мальтоза
-
Гликоген:
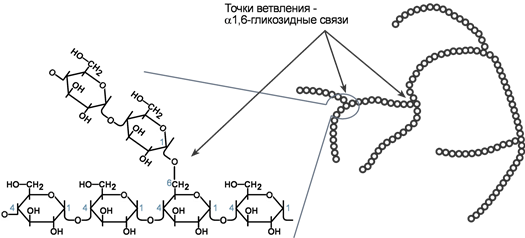
α-D-Glc-(1→4)
α-D-Glc-(1→6)
-
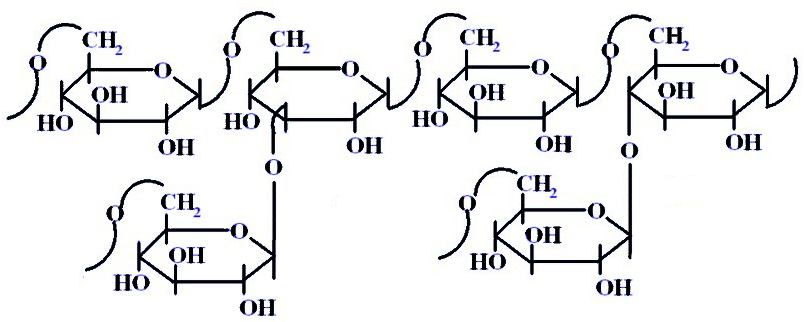
Декстран. Заменитель плазмы крови:
-
Гетерополисахариды. В основном растительные источники. В животном мире связаны с белками:
-
Гемицеллюлоза,
-
Ксилан (ксилоза, арабиноза),
-
Общие принципы установления строения полисахаридов.
Необходимо охарактеризовать полимерные молекулы в целом с учетом регулярности и построения и определить молекулярную массу. Основным способом выяснения структуры полисахарида является расщепление полимера на олигосахаридные фрагменты, установление строения каждого фрагмента и воссоздание на их основе структур исходного полимера. Большинство полисахаридов построены из повторяющихся олигосахаридных блоков: в этом случае задач сводится к расщеплению полисахаридной цепи, выделению повторяющегося звена и анализ его структуры.
В структурном анализе полисахаридов широк используются полный и частичный кислотный гидролизы. В связи с различной устойчивостью гликозидных связей к кислотному гидролизу и с различной растворимостью полисахаридов условия гидролиза существенно варьируются.
При частичном гидролизе гомополисахаридов в зависимости от условий получается набор олигосахаридов различной длины. В случае гетерополисахаридов нередко удается подобрать условия, при которых наблюдается предпочтительный гидролиз определенного типа связи, что приводит к образованию характеристических олигосахаридных фрагментов; такие фрагменты получаются, в частности, при гидролизе полисахаридов, состоящих из чередующихся остатков нейтральных сахаров и уроновых кислот.
Важным методом частичного расщепления полисахаридов является ферментативный гидролиз; при этом используются эндо ферменты, расщепляющие полисахариды в середине цепи. Наиболее известный из таких ферментов — лизоцим, расщепляющий β(1→4)-гликозидные связи между остатками N-ацетилмурамовой кислоты и N-ацетилглюкозаминов в полисахариде (муреине) клеточной стенки бактерий.
Наилучший результат дает метилирование по Хакомори. Часто используемым вариантом гидролиза метилированных полисахаридов, помимо метанолиза, является частичны гидролиз 90%-ной муравьиной кислотой с последующим гидролизом серной кислотой в более мягких условиях, чем это требовалось бы для расщепления интактного метилированного полисахарида.
Современная ЯМР-спектроскопия является мощным инструментом аналиаз структуры полисахаридов и используется в подавляющем большинстве исследований. Этот метод позволяет определять как состав, места замещения и последовательность моносахаридных остатков биополимера, так и его пространственное строение.
-
Углевод-белковые конъюгаты. Гликопротеины. Типы связей углеводов с белком. Гетерополиаминосахариды - белковые комплексы соединительной ткани. Гепарин, его антикоагулянтная активность. Гиалуроновая кислота, строение, биологическая роль. Хондроитинсульфаты и их роль в кальцификации тканей.
Углеводородные белковые конъюгаты:
-
протеогликаны
гликопротеины
Углеводородный фрагмент:
70-80%
10-40%
Строение углеводорода
регулярное
нерегулярное
Сульфатированы
часто
нет
Связь белка и углеводорода
Ковалентная или электростатическая
Гликопротеинами называются смешанные биополимеры, в которых молекулы белка содержит ковалентно присоединенные олигосахаридные цепи. Длина олигосахаридных цепей и их число в гликопротеинах варьируются в широких пределах.
При выделении гликопротеинов из природных источников используется набор хроматографических и электрофоретических методов, характерных для химии белков.
Наиболее распространенным типом связи в животных гликопротеинах является N-гликозидная связь, образуемая остатками N-ацетилглюкозамина и β-амидной группой аспарагина
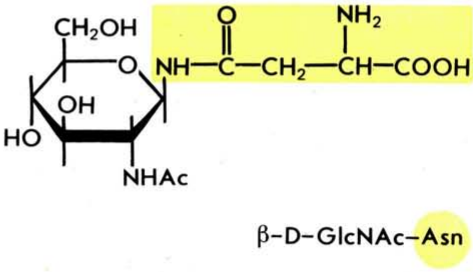
N-Гликозиламидная связь относительно устойчива в мягких щелочных и кислотных условиях, но расщепляется при более жестком гидролизе (2 н. НС1, 100 °С, 10 — 12 мин или 0,2 — 2 н. NaOH, 100 °С, 16 ч).
Другим типом связи в животных гликопротеинах является О-гликозидная связь между остатками N-ацетилгалактозамина и гидроксильной группой серина или треонина. О-Гликозидная связь может быть расщеплена в мягких щелочных условиях (0,1 н. NaOH, 37 °С).

Гетерополиаминосахариды. Протеогликаны соединительной ткани. мукополисахариды:
Обеспечивают эластичность/упругость различных тканей и органов.
-
На поверхности клетки создают дополнительную оболочку из заряженных групп (сульфо, карбокси). Выполняют роль молекулярного сита, обеспечивают транспорт нужных веществ, защищают от проникновения чужеродных объектов.
-
Гепарин:

На 4 остатка моносахаридных звеньев – 5 остатков серной кислоты. Связан с белками плазмы. Эффективный антикоагулянт.
-
Гиалуроновая кислота;
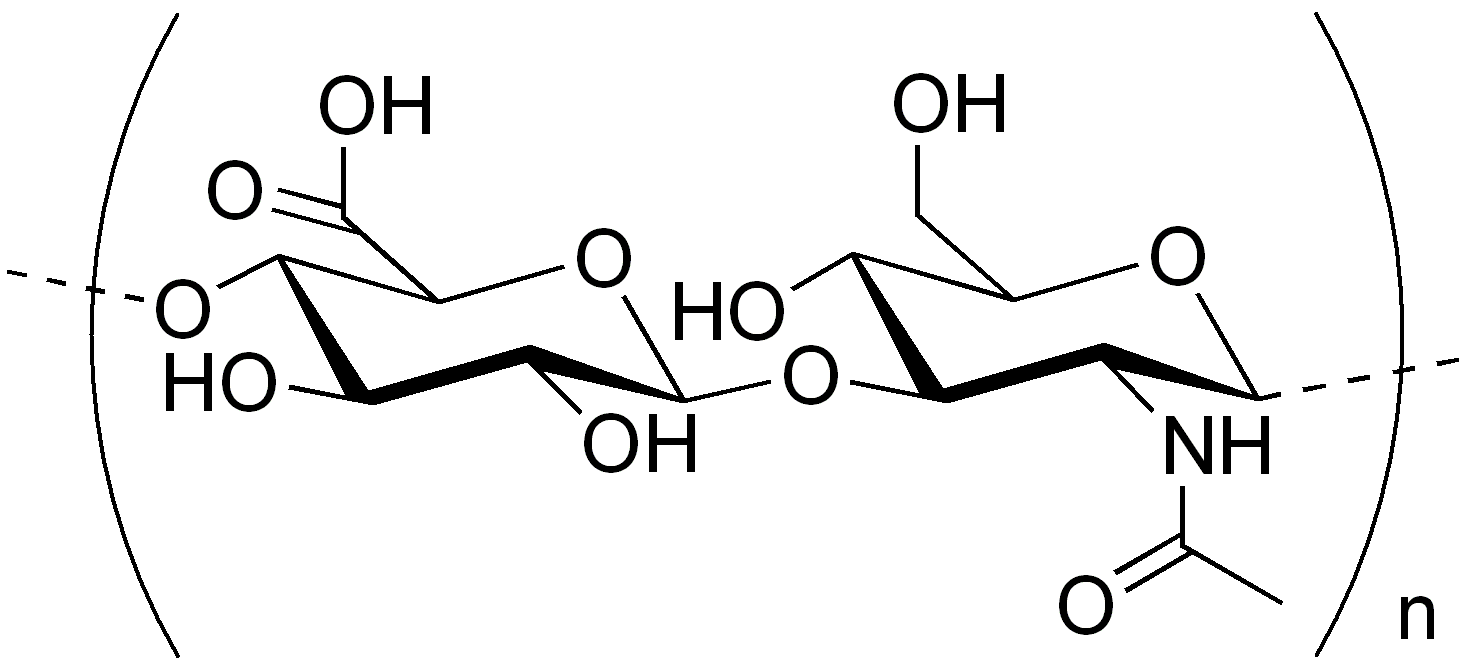 β-D-GlcA-(1→4)- D-GlcN
β-D-GlcA-(1→4)- D-GlcN
Связь электростатическая между белком и углеводом. Повторяющиеся дисахариды входят в состав гиалуроновой кислоты.
Функции: барьерная, связывает большое количество жидкости, применяется в медицине.
-
Хондроитинсульфаты:
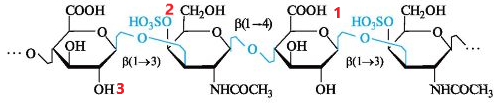
-
Хондроитинсульфат С
-
Хондроитинсульфат А
-
Хондроитинсульфат В
Функции: барьерная, нарушение обмена приводит к кальцификации тканей. Снижает потерю Ca2+. Улучшает фосфорно-кальциевый обмен в хрящевой ткани, ускоряет процессы её восстановления.
